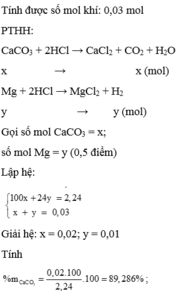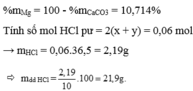Cho hỗn hợp nặng 2,46 gam gồm nhôm và đồng. Đem hổn hợp này phản ứng với lượng dư dd HCl 10%. Sau phản ứng, ta thu được 0,672 lít khí ở đktc. Tìm khối lượng mỗi kim loại trong hỗn hợp đầu. Tìm khối lượng dd HCl cần để phản ứng. Tìm nồng độ phần trăm của dd muối thu được sau phản ứng nếu lượng axit chỉ dùng vừa đủ.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{H2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,03 0,06 0,03 0,03
\(MgO+2HCl\rightarrow MgCl_2+H_2O|\)
1 2 1 1
0,03 0,06 0,03
a) \(n_{Mg}=\dfrac{0,03.1}{1}=0,03\left(mol\right)\)
\(m_{Mg}=0,03.24=0,72\left(g\right)\)
\(m_{MgO}=1,92-0,72=1,2\left(g\right)\)
b) Có : \(m_{MgO}=1,2\left(g\right)\)
\(n_{MgO}=\dfrac{1,12}{40}=0,03\left(mol\right)\)
\(n_{HCl\left(tổng\right)}=0,06+0,06=0,12\left(mol\right)\)
400ml = 0,4l
\(C_{M_{ddHCl}}=\dfrac{0,12}{0,4}=0,3\left(l\right)\)
c) \(n_{MgCl2\left(tổng\right)}=0,03+0,03=0,06\left(mol\right)\)
\(C_{M_{MgCl2}}=\dfrac{0,06}{0,4}=0,15\left(M\right)\)
Chúc bạn học tốt

a) PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\) (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\) (2)
b) Ta có: \(\Sigma n_{H_2}=\dfrac{3,024}{22,4}=0,135\left(mol\right)\)
Gọi số mol của Fe là \(a\) \(\Rightarrow n_{H_2\left(1\right)}=a\)
Gọi số mol của Al là \(b\) \(\Rightarrow n_{H_2\left(2\right)}=\dfrac{3}{2}b\)
Ta lập được hệ phương trình:
\(\left\{{}\begin{matrix}a+\dfrac{3}{2}b=0,135\\56b+27b=4,14\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,045\\b=0,06\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,045\cdot56=2,52\left(g\right)\\m_{Al}=1,62\left(g\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{2,52}{4,14}\cdot100\%\approx60,87\%\\\%m_{Al}=39,13\%\end{matrix}\right.\)
c) PTHH: \(FeCl_2+2NaOH\rightarrow2NaCl+Fe\left(OH\right)_2\downarrow\)
\(AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3\downarrow+3NaCl\)
\(4Fe\left(OH\right)_2+O_2\underrightarrow{t^o}2Fe_2O_3+4H_2O\)
\(2Al\left(OH\right)_3\underrightarrow{t^o}Al_2O_3+3H_2O\)
Theo các PTHH: \(\left\{{}\begin{matrix}n_{Fe\left(OH\right)_2}=n_{FeCl_2}=0,045mol\\n_{Al\left(OH\right)_3}=n_{AlCl_3}=0,06mol\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe_2O_3}=0,0225mol\\n_{Al_2O_3}=0,03mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe_2O_3}=0,0225\cdot160=3,6\left(g\right)\\m_{Al_2O_3}=0,03\cdot102=3,06\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{chấtrắn}=3,06+3,6=6,66\left(g\right)\)

a) Gọi `n_{Al} = a (mol); n_{Fe} = b (mol)`
PTHH:
`2Al + 3H_2SO_4 -> Al_2(SO_4)_3 + 3H_2`
`Fe + H_2SO_4 -> FeSO_4 + H_`
b) `n_{H_2} = (0,56)/(22,4) = 0,025 (mol)`
Theo PT: `n_{H_2} = n_{Fe} + 3/2 n_{Al}`
`=> b + 1,5a = 0,025`
Giải hpt \(\left\{{}\begin{matrix}27a+56b=0,83\\1,5a+b=0,025\end{matrix}\right.\Leftrightarrow a=b=0,01\)
=> \(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,01.27}{0,83}.100\%=32,53\%\\\%m_{Fe}=100\%-32,53\%=67,47\%\end{matrix}\right.\)

Ta có: 27nAl + 56nFe = 13,8 (1)
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
Theo ĐLBT e, có: 3nAl + 2nFe = 2nH2 = 0,9 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,2\left(mol\right)\\n_{Fe}=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,2.27=5,4\left(g\right)\\m_{Fe}=0,15.56=8,4\left(g\right)\end{matrix}\right.\)