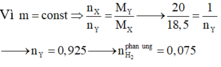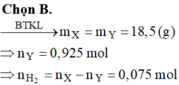Hỗn hợp khí X gồm O2 và SO2 có tỉ khối hơi so với H2 là 28. Cho 4,48l (đktc) hỗn hợp khí X vào bình kín có V2O5 rồi đung nóng đến 450 độ C. Sau một thời gian pư làm nguội bình rồi cho toàn bộ các chất thu được qua dd BaCl2 (dư). Sau khí kết thúc pư thu được 17,475 g kết tủa. Tính hiệu suất của pư oxi hóa SO2 thành SO3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(\overline{M}=24\cdot2=48\)
\(\dfrac{n_{SO_2}}{n_{O_2}}=\dfrac{64-48}{48-32}=1\)
\(n_{hh}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(\Rightarrow n_{SO_2}=n_{O_2}=0.15\left(mol\right)\)
\(2SO_2+O_2\underrightarrow{^{t^0,V_2O_5}}2SO_3\)
Bđ:0.15....0.15
Pư: x..........0.5x......x
KT: 0.15-x..0.15-0.5x..x
\(n_{hh}=0.15-x+0.15-0.5x+x=0.3-0.5x\left(mol\right)\)
\(m=\left(0.15-x\right)\cdot64+\left(0.15-0.5x\right)\cdot32+80x=\left(0.3-0.5x\right)\cdot2\cdot26\)
\(\Rightarrow x=\dfrac{3}{65}\)
\(H\%=\dfrac{\dfrac{3}{65}}{0.15}\cdot100\%=30.7\%\)

Có \(A\left\{{}\begin{matrix}n_{SO_2}+n_{O_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\\dfrac{64.n_{SO_2}+32.n_{O_2}}{n_{SO_2}+n_{O_2}}=25,6.2=51,2\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}n_{SO_2}=0,3\left(mol\right)\\n_{O_2}=0,2\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%V_{SO_2}=\dfrac{0,3}{0,5}.100\%=60\%\\\%V_{O_2}=\dfrac{0,2}{0,5}.100\%=40\%\end{matrix}\right.\)
Gọi số mol SO2 phản ứng là x (mol)
PTHH: 2SO2 + O2 --> 2SO3
Trc pư: 0,3 0,2 0
Pư: x------>0,5x------>x
Sau pư: (0,3-x) (0,2-0,5x) x
=> \(M_B=\dfrac{m_B}{n_B}=\dfrac{m_A}{n_B}=\dfrac{25,6}{\left(0,3-x\right)+\left(0,2-0,5x\right)+x}=32.2=64\)
=> x = 0,2
=> \(B\left\{{}\begin{matrix}SO_2:0,1\left(mol\right)\\O_2:0,1\left(mol\right)\\SO_3:0,2\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%V_{SO_2}=\dfrac{0,1}{0,1+0,1+0,2}.100\%=25\%\\\%V_{O_2}=\dfrac{0,1}{0,1+0,1+0,2}.100\%=25\%\\\%V_{SO_3}=\dfrac{0,2}{0,1+0,1+0,2}.100\%=50\%\end{matrix}\right.\)
- Xét hỗn hợp khí A:
Gọi x,y lần lượt là số mol của SO2 và O2 trong hỗn hợp. (x,y>0) (mol)
\(x+y=\dfrac{11,2}{22,4}=0,5\left(1\right)\\ Mà:M_A=25,6.M_{H_2}=25,6.2=51,2\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow\dfrac{64x+32y}{0,5}=51,2\\ \Leftrightarrow64x+32y=25,6\left(2\right)\\ \left(1\right),\left(2\right)\Rightarrow\left\{{}\begin{matrix}x+y=0,5\\64x+32y=25,6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,3\\y=0,2\end{matrix}\right.\\ \Rightarrow\%V_{\dfrac{SO_2}{A}}=\dfrac{0,3}{0,5}.100=60\%\Rightarrow\%V_{\dfrac{O_2}{A}}=100\%-60\%=40\%\)
- Xét hỗn hợp khí B:
Gọi a là số mol SO3 được tạo thành trong hhB (mol) (a,b>0)
\(PTHH:2SO_2+O_2\rightarrow\left(xt,t^o\right)2SO_3\\ \Rightarrow n_{SO_2\left(hhB\right)}=0,3-a\left(mol\right)\\ n_{O_2\left(hhB\right)}=0,2-0,5a\left(mol\right)\\ M_{hhB}=32.M_{H_2}=32.2=64\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow\dfrac{80a+\left(0,2-0,5a\right).32+\left(0,3-a\right).64}{a+\left(0,2-0,5a\right)+\left(0,3-a\right)}=64\\ \Leftrightarrow a=0,2\\ \Rightarrow hhB\left\{{}\begin{matrix}SO_3:0,2\left(mol\right)\\SO_2:0,1\left(mol\right)\\O_2:0,1\left(mol\right)\end{matrix}\right.\\ \Rightarrow\%V_{\dfrac{SO_3}{hhB}}=\dfrac{0,2}{0,2+0,1+0,1}.100=50\%\\ \%V_{\dfrac{SO_2}{hhB}}=\%V_{\dfrac{O_2}{hhB}}=\dfrac{0,1}{0,2+0,1+0,1}.100=25\%\)
Em xem có gì không hiểu thì hỏi lại nhá!

Đáp án C
Hướng dẫn
mX = 18,5.1 = 18,5 g; nY = 18,5/20 = 0,925 mol => nH2 pư = 1 – 0,925 = 0,075 mol