Cho 0,896 lít CO2 (đktc) hấp thụ hoàn toàn bởi 200ml dung dịch Ba(OH)2 a mol/l thì thu được 3,94g kết tủa. Tính a?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn D
nCO2 dùng ở 2 thí nghiệm là như nhau nhưng TN2 cho nhiều BaCO3 hơn TN1
Þ Trong dung dịch sau phản ứng của TN1 còn Ba2+ cùng với CO32− hoặc HCO3-
Þ Dung dịch sau phản ứng của TN1 chỉ có Ba(HCO3)2.
Vậy ở TN1 bản chất là giống thí nghiệm 1 tạo ra 0,1 mol BaCO3 và dung dịch có a – 0,1 mol Ba(HCO3)2
Lượng NaOH thêm vào là a > nBa(HCO3)2 Þ Toàn bộ Ba2+ đã kết tủa
Þ a – 0,1 = 0,1 Þ a = 0,2; BTNT.C Þ nCO2 = 0,1 + 0,1.2 = 0,3 Þ V = 6,72.

Ba(OH)2 + CO2 -> BaCO3 + H2O (1)
BaCO3 + CO2 + H2O -> Ba(HCO3)2 (2)
TN1: 2,464 lít CO2 (đktc) vào 200ml dung dịch X thì thu được 3a gam kết tủa.
TN2: 3,136 lít CO2 (đktc) vào 200ml dung dịch X thì thu được 2a gam kết tủa
=> Lượng CO2 ở TN2 tăng mà kết tủa lại giảm
*TN1: Chỉ xảy ra (1)
nCO2 = 0,11 mol
nBa(OH)2 = 0,2x mol
=> nBaCO3 (1) = 0,2 x mol
=> 3a = 0,2x . 197 = 39,2 x (I)
* TN2: Xảy ra cả (1)(2)
nCO2 = 0,14 mol
=> nCO2 (2) = 0,14 - 0,11 = 0,3 mol
=> nBaCO3 (2) = 0,3 mol
=> nBaCO3 còn lại = 0,2 x - 0,3 mol
=> 2a = (0,2 x - 0,3).197 = 39,2x - 59,1
=> 3a = (39,2x - 59,1). 1,5 = 58,8x - 88,65 (II)
Từ (I) và (II) => 39,2 x = 58,8x - 88,65
=> x = 4,5 M

Đáp án B
nCO2 = 0,07; nNaOH = 0,08; nBaCl2 = 0,04; nBa(OH)2 = 0,25a; nBaCO3 = 0,02 = 0,08 + 0,5a
Ba2+ + CO32- → BaCO3↓
0,02 ← 0,02 ← 0,02
CO2 + 2OH-→ CO32- + H2O
0,02 ← 0,04 ← 0,02
CO2còn dư + OH- → HCO3-
0,05 → 0,05
= 0,08 + 0,5a = 0,04 + 0,05 a = 0,02

1.
\(n_{CO_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=0.075\left(mol\right)\)
\(T=\dfrac{0.1}{0.075}=1.33\)
=> Tạo ra 2 muối
\(n_{CaCO_3}=a\left(mol\right),n_{Ca\left(HCO_3\right)_2}=b\left(mol\right)\)
Khi đó :
\(a+b=0.075\)
\(a+2b=0.1\)
\(\Rightarrow\left\{{}\begin{matrix}a=0.05\\b=0.025\end{matrix}\right.\)
\(m_{sp}=0.05\cdot100+0.025\cdot162=9.05\left(g\right)\)
2.
\(n_{CO_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0.2\cdot0.2=0.04\left(mol\right)\)
\(T=\dfrac{0.005}{0.04}=1.25\)
=> Tạo ra 2 muối
\(n_{BaCO_3}=a\left(mol\right),n_{Ba\left(HCO_3\right)_2}=b\left(mol\right)\)
Ta có :
\(a+b=0.04\)
\(a+2b=0.05\)
\(\Rightarrow\left\{{}\begin{matrix}a=0.03\\b=0.01\end{matrix}\right.\)
\(m_{BaCO_3}=0.03\cdot197=5.91\left(g\right)\)

Đáp án D
Ta có: n C O 2 = 0,12 mol; n B a ( O H ) 2 = 2,5 a mol ; n B a C O 3 = 0,08 mol
Ta có n C O 2 > n B a C O 3 nên xảy ra các PTHH sau :
CO2+ Ba(OH)2 → BaCO3↓+ H2O
0,08 0,08 ← 0,08 mol
2CO2+ Ba(OH)2 → Ba(HCO3)2
(0,12-0,08)→ 0,02 mol
Tổng số mol Ba(OH)2 là n B a ( O H ) 2 = 0,08 + 0,02 = 0,1 mol = 2,5a
→a = 0,04M

Đáp án A
Có nCO2 = 0,07 mol ; nNaOH= 0,08 mol
=> nCO32-=0,01 mol ; nHCO3- = 0,06 mol
Y gồm 0,04 mol BaCl2 ; 0,25a mol Ba(OH)2
=>để tạo 3,94 g kết tủa hay 0,02 mol BaCO3 th́ HCO3- + OH- → CO32-
0,01 <- 0,01(mol)
=> 0,5a=0,01 => a=0,02M



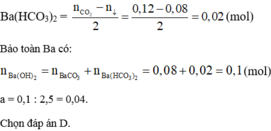
$n_{CO_2}= 0,04(mol) > n_{BaCO_3} = 0,02(mol)$ nên có tạo muối axit
CO2 + Ba(OH)2 → BaCO3 + H2O
0,02........0,02...........0,02.................(mol)
2CO2 + Ba(OH)2 → Ba(HCO3)2
0,02........0,01......................................(mol)
$n_{Ba(OH)_2} = 0,02 + 0,01 = 0,03(mol)$
$a = \dfrac{0,03}{0,2} = 0,15(M)$
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
\(0.02..........0.02............0.02\)
\(Ba\left(OH\right)_2+2CO_2\rightarrow Ba\left(HCO_3\right)_2\)
\(0.01........0.04-0.02\)
\(n_{Ba\left(OH\right)_2}=0.02+0.01=0.03\left(mol\right)\)
\(C_{M_{Ba\left(OH\right)_2}}=\dfrac{0.03}{0.2}=0.15\left(M\right)\)