Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 1:
a) nP=6,2/31=0,2(mol); nO2= 6,72/22,4=0,3(mol)
PTHH: 4P + 5 O2 -to-> 2 P2O5
Ta có: 0,2/4 < 0,3/5
=> P hết, O2 dư, tính theo nP
=> nO2(p.ứ)= 5/4. nP= 5/4. 0,2=0,25(mol)
=> mO2(dư)=0,3- 0,25=0,05(mol)
=> mO2(dư)=0,05.32=1,6(g)
b) nP2O5= nP/2= 0,2/2=0,1(mol)
=>mP2O5=0,1.142=14,2(g)

\(n_P=\dfrac{m}{M}=\dfrac{6,2}{31}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
PTHH:\(4P+5O_2\rightarrow2P_2O_5\)
tpứ: 0,2 0,35
pứ: 0,2 0,25 0,1
spứ: 0 0,1 0,1
a)chất còn dư là oxi
\(m_{O_2dư}=n.M\)=0,1.32=3,2(g)
b)\(m_{P_2O_5}=n.M\)=0,1.142=14,2(g)

Theo gt ta có: $n_{SO_2}=0,05(mol)$
Bảo toàn e ta có: $n_{FeO}=0,05(mol)$
$\Rightarrow n_{CuO}=0,145(mol)$
$\Rightarrow \%m_{FeO}=23,68\%;\%m_{CuO}=76,32\%$
Bảo toàn Fe và Cu ta có: $n_{Fe_2O_3}=0,025(mol);n_{CuO}=0,145(mol)$
$\Rightarrow m=15,6(g)$
Ta có: \(n_{SO_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Bảo toàn electron: \(n_{FeO}=2n_{SO_2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{FeO}=\dfrac{0,1\cdot72}{15,2}\cdot100\%\approx47,37\%\\\%m_{Cu}=100\%-47,37\%=52,63\%\end{matrix}\right.\)
Mặt khác: \(n_{CuO}=\dfrac{15,2-7,2}{80}=0,1\left(mol\right)\)
Bảo toàn nguyên tố: \(\left\{{}\begin{matrix}n_{FeO}=n_{Fe\left(OH\right)_3}=0,1\left(mol\right)\\n_{CuO}=n_{Cu\left(OH\right)_2}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{kết.tủa}=m_{Fe\left(OH\right)_3}+m_{Cu\left(OH\right)_2}=0,1\cdot160+0,1\cdot98=25,8\left(g\right)\)
Bảo toàn nguyên tố: \(\left\{{}\begin{matrix}n_{CuO}=0,1\left(mol\right)\\n_{Fe_2O_3}=\dfrac{1}{2}n_{FeO}=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{rắn}=m_{Fe_2O_3}+m_{CuO}=0,1\cdot80+0,05\cdot160=16\left(g\right)\)



a) Gọi số mol của FeCO3: x (mol) ;
số mol của FeS2: y (mol)
4FeCO3 + O2 → Fe2O3 + 4CO2↑
x → 0,25x → x (mol)
4FeS2 +11O2 → 2Fe2O3 + 8SO2↑
y → 2,75y → 2y (mol)
∑ nO2 = 0,25x + 2,75y (mol)
Cùng điều kiện về nhiệt độ và áp suất nên tỉ lệ về thể tích = tỉ lệ về số mol
=> nN2 = 4nO2 = 4(0,25x + 2,75y)
=> nN2 = x + 11y (mol)
Vậy hỗn hợp Y gồm:

Khối lượng Fe có trong Z là:

Vì H = 80% => nFe2O3 (trong X) = 0,12. 100% : 80% = 0,15 (mol)
nFe2O3 dư (trong Z) = 0,15 – 0,12 = 0,03 (mol)
Khối lượng tạp chất trong Z = 27,96 – mFe – mFe2O3 dư = 27,96 – 0,24.56 – 0,03.160 = 9,72 (g)
Bảo toàn nguyên tố Fe => nFeCO3 + nFeS2 = 2nFe2O3(trong X)
=> x + y = 0,3 (2)
Từ (1) và (2) => x = 0,18 và y = 0,12 (mol)
Áp dụng công thức PV = nRT ( với n = nCO2 + nSO2 + nN2 = 0,18 + 2. 0,12 + 0,18 +11.0,12 = 1,92)
=> P.10 = 1,92.0,082. (136,5 +273)
=> P = 6,447 ( atm) ≈ 6,5 (atm)
Ta có: mA = mFeCO3 + mFeS2 + mtạp chất = 0,18.116 + 0,12.120 + 9,72 = 45 (g)
![]()
b) hỗn hợp Y gồm:

Cho hỗn hợp Y qua O2 ( xúc tác V2O5 ) có phản ứng sau:

Khối lượng dd sau: mdd sau = mSO3 + mH2O = 0,24. 80 + 592,8 = 612 (g)


PTHH: \(Fe_3O_4+8HCl\rightarrow FeCl_2+2FeCl_3+4H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\\n_{HCl}=\dfrac{300\cdot3,65\%}{36,5}=0,3\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,3}{8}\) \(\Rightarrow\) Fe3O4 còn dư, HCl p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe_3O_4\left(dư\right)}=0,0625\left(mol\right)\\n_{FeCl_2}=0,0375\left(mol\right)\\m_{FeCl_3}=0,075\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe_3O_4\left(dư\right)}=0,0625\cdot232=14,5\left(g\right)\\m_{muối}=0,0375\cdot127+0,075\cdot162,5=16,95\left(g\right)\end{matrix}\right.\)
nFe3O4= 23,2/232=0,1(mol); nHCl = (300.3,65%)/36,5= 0,3(mol)
a) PTHH: Fe3O4 + 8 HCl -> 2 FeCl3 + FeCl2 + 4 H2O
b) Ta có: 0,3/8 < 0,1/1
=> Fe3O4 dư, HCl hết, tính theo nHCl.
=> nFe3O4(p.ứ)= nFeCl2= nHCl/8=0,3/8= 0,0375(mol)
=> mFe3O4(dư)= (0,1- 0,0375).232=14,5(g)
c) nFeCl3= 2/8. 0,3= 0,075(mol)
=> mFeCl3= 0,075.162,5=12,1875(g)
mFeCl2= 0,0375. 127=4,7625(g)
=>m(muối)= 12,1875+ 4,7625= 16,95(g)

A tác dụng với NaHCO3 cho khí CO2 → A: axit CH3COOH
BTKL: m + mO2 = mCO2 + mH2O => m = 1,8
=> nCH3COOH = 0,03
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
0,03 0,02 0,0125
=> H = 62,5%

Câu 1 :
\(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
Pt : \(4P+5O_2\underrightarrow{t^o}2P_2O_5|\)
4 5 2
0,4 0,2
\(n_{P2O5}=\dfrac{0,4.2}{4}=0,2\left(mol\right)\)
⇒ \(m_{P2O5}=0,2.142=28,4\left(g\right)\)
Chúc bạn học tốt
Câu 2 :
\(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
\(n_{O2\left(dktc\right)}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Pt : \(4P+5O_2\underrightarrow{t^o}2P_2O_5|\)
4 5 2
0,4 0,25 0,1
Lập tỉ số só sánh : \(\dfrac{0,4}{4}>\dfrac{0,25}{5}\)
⇒ P dư , O2 phản ứng hết
⇒ Tính toán dựa vào số mol của O2
\(n_{P2O5}=\dfrac{0,25.2}{5}=0,1\left(mol\right)\)
⇒ \(m_{P2O5}=0,1.142=14,2\left(g\right)\)
\(n_{P\left(dư\right)}=0,4-\left(\dfrac{0,25.4}{5}\right)=0,2\left(mol\right)\)
⇒ \(m_{P\left(dư\right)}=0,2.31=6,2\left(g\right)\)
\(m_{rắn}=14,2+6,2=20,4\left(g\right)\)
Chúc bạn học tốt

\(n_{hh}=\dfrac{11,2}{22,4}=0,5mol\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\\n_{C_2H_4}=y\end{matrix}\right.\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
x x ( mol )
\(C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\)
y 2y ( mol )
\(n_{CaCO_3}=\dfrac{80}{100}=0,8mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow\left(t^o\right)CaCO_3+H_2O\)
0,8 0,8 ( mol )
Ta có:
\(\left\{{}\begin{matrix}x+y=0,5\\x+2y=0,8\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,3\end{matrix}\right.\)
\(\%V_{CH_4}=\dfrac{0,2}{0,5}.100=40\%\)
\(\%V_{C_2H_4}=100\%-40\%=60\%\)
\(m_{tăng}=m_{Ca\left(OH\right)_2}+m_{CaCO_3}=0,8.\left(74+100\right)=139,2g\)

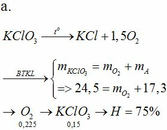
b.
4P + 5O2 → 2P2O5
0,16→ 0,2
Dư: 0,025
Sau pứ m(bình 1) = mP2O5 = 11,36 (g)
O2 + 2C → 2CO
0,025→ 0,05 0,05
Dư: 0,25
Sau pứ m(bình 2) = mCdư = 3 (g)
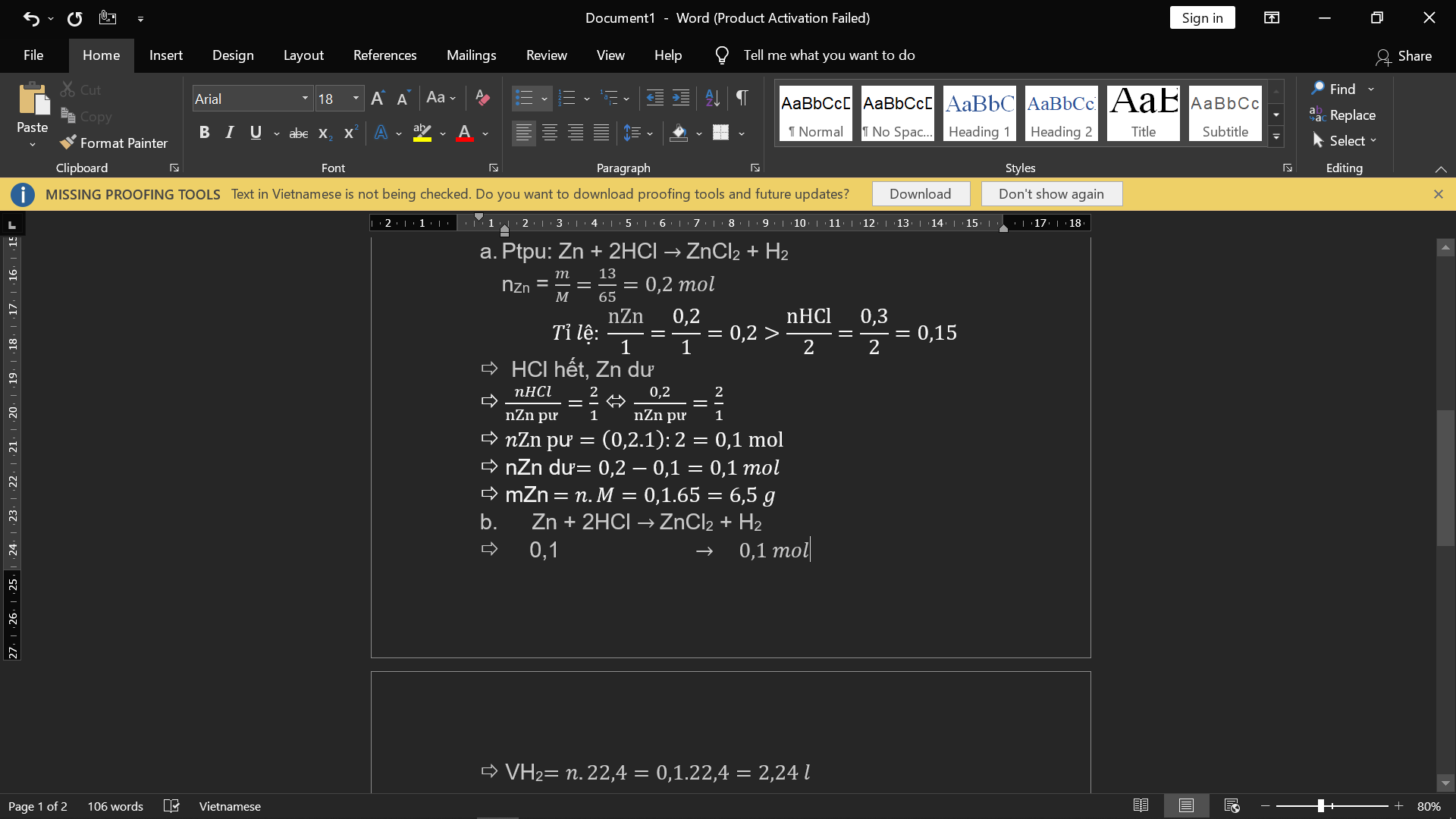
Câu 6
a)4P+5O2--->2P2O5
sản phẩm thu dc là oxit axit
b) n P=1,55/31=0,05(mol)
n O2=1,12/22,4=0,05(mol)
Lập tỉ số
n P=0,05/4
n O2=0,05/5
-->P dư
Theo pthh
n P=4/5n O2=0,04(mol)
n P dư=0,05-0,04=0,01(mol)
m P dư=0,01.31=0,31(g)
c) Theo pthh
n P2O5=2/5n P=0,02(mol)
m P2O5=0,02.142=2,84(g)
Câu 7 hình như còn thiếu nhỉ
Chúc bạn học tốt
b)