Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tổng số proton trong MX2 là 58 hạt → ZM + 2.ZX = 58
Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt → -ZM + NM = 4
Trong hạt nhân X, số notron bằng số proton → ZX = NX
MA =ZM + NM + 2.ZX + 2.NX = (ZM + 2.ZX ) + NM + 2NX= 58 + NM + 58 - ZM = 116 + NM- ZM
M chiếm 46,67% về khối lượng → ZM + NM =
7
15
. (116 + NM- ZM ) → 22ZM + 8NM = 812
Ta có hệ
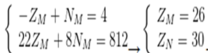
M là Fe
→ ZX =
58
-
26
2
= 16 → X là S
Công thức của A là FeS2.
Đáp án A.

Đáp án A
Tổng số proton trong MX2 là 58 hạt → ZM + 2.ZX = 58
Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt → -ZM + NM = 4
Trong hạt nhân X, số notron bằng số proton → ZX = NX
MA =ZM + NM + 2.ZX + 2.NX = (ZM + 2.ZX ) + NM + 2NX
= 58 + NM + 58 - ZM = 116 + NM - ZM
M chiếm 46,67% về khối lượng
![]()
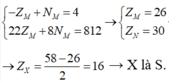
=> M là Fe

Theo đề ta có
2Z(R)+N(R)+3[2Z(X)+N(X)]=120
2Z(R)+3.2Z(X)-[N(R)+3N(X)]=40
=> Z(R)+3Z(X)=40
N(R)+ 3N(X)=40
=> khối lượng phân tử RX3
M= Z(R)+N(R)+3Z(X) +3N(X)=80
a) Trong hợp chất ta có :
\(\left\{{}\begin{matrix}2Z+N=120\\2Z-N=40\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}Z=40\\N=40\end{matrix}\right.\)
Vậy : \(A_{RX_3}=Z+N=40+40=80\)
b) Ta có : \(\left\{{}\begin{matrix}Z_R+3Z_X=40\\N_R+3N_X=40\\Z_R=N_R\\\end{matrix}\right.\)
=>40-3ZX=40-3NX
=> ZX=ZN

\(\left\{{}\begin{matrix}2Z_A+N_A=140\\2Z_A=65,714\%.140\end{matrix}\right.\)
=>\(\left\{{}\begin{matrix}Z_A=46\\N_A=48\end{matrix}\right.\)
Hợp chất A tạo thành từ ion M+ và X2-
=> CT A: M2X
\(\left\{{}\begin{matrix}2Z_M+2N_M+Z_X+N_X=46+48\\Z_M+N_M-\left(Z_X+N_X\right)=23\end{matrix}\right.\)
=> \(3Z_M+3N_M=117\)
=> \(Z_M+N_M=39\)
Ta có A\(\approx\) MM
=> M là Kali (Z=19)
Ta có : \(2Z_M+2N_M+Z_X+N_X=94\)
=> \(2.39+Z_X+N_X=94\)
=> \(Z_X+N_X=16\)
=> X là O
=> CT của A : K2O

a.Tổng số hạt cơ bản của X gồm proton (+1) , notron không mang điện và electron (-1) ký hiệu lần lượt là ( P, N ,E ) và vì nguyên tử luôn trung hòa về điện nên tích dương và âm phải bằng nhau tức số proton và electron của 1 phân tử cũng luôn bằng nhau.
Theo đề bài ta có hệ pt
==> P + N + E = 48 <=> 2P + N = 48(1)
2P = 2N (2)
Từ (1), (2) ==> P= N = E =16
Hạt nhân gồm proton (+1) và notron không mang điện, nên proton làm cho hạt nhân mang điện và điện tích hạt nhân bằng số lượng proton = +16
b. cấu hình eletron : 1s22s22p63s23p4
c. Số eletron ở từng lớp:
Lớp 1s : 2 electron 2s : 2 electron 2p : 6 electron
Lớp 3s : 2 electron 3p : 4 electron

M chiếm 46,67% về khối lượng:

Quan sát – phân tích: Hệ 5 ẩn gồm 4 phương trình không thể giải thông thường để tìm nghiện vì ta cần phải rút gọn nghiệm: Phương trình (2) chứa ẩn ZM và x. ZA từ phương trình (1); (3); (4) ta có thể đưa về 1 phương trình chứa 2 ẩn ZM và x
Z A → Đưa về hệ phương trình 2 ẩn.
Ta đưa được về hệ sau
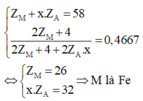
M là Fe nên x sẽ nhận giá trị từ 1 đến 3.
Từ x.ZA = 32 ta có các giá trị của ZA

Vậy H là FeS2
Đáp án A.

Đáp án A.
Gọi số hạt proton, nơtron, electron của nguyên tử X là p, n, e và của Y là p’, n’, e’.
Theo bài : p = n = e và p’ = n’ = e’.
Trong hợp chất XY2, X chiếm 50% về khối lượng nên:
M X 2 M Y = 50 50 ⇒ p + n 2 ( p ' + n ' ) = 1 ⇒ p = 2 p '
Tổng số proton trong phân tử XY2 là 32 nên p + 2p’ = 32.
Từ đây tìm được: p = 16 (S) và p’ = 8 (O). Hợp chất cần tìm là SO2.
Cấu hình electron của S: 1s22s22p63s23p4