Hòa tan hoàn toàn hỗn hợp A gồm Mg Cu và một lượng vừa đủ dung dịch H2 SO4 70% thu được 1,2 lít khí SO2 và dung dịch B cho dung dịch B tác dụng với NaOH dư được kết tủa C lung C đến khối lượng không đổi được hỗn hợp chất rắn A Cho A tác dụng với lượng dư H2 ai thu được 2,72 g hỗn hợp chất rắn f tính số gam Mg cu có trong hỗn hợp a hai cho thêm 6,8 gam nước vào dung dịch B thu được dung dịch B Tính nồng độ phần trăm các chất trong dung dịch
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Gọi a, b và c lần lượt là số mol của Mg, Fe3O4 và Fe(NO3)2.
Hỗn hợp khí Y gồm NO (0,07 mol) và H2 (0,03 mol).
Cho 8,66 gam X tác dụng với dung dịch hỗn hợp HCl và HNO3 thì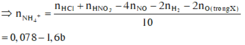
Cho Y tác dụng với NaOH, lọc kết tủa đun nóng thu được 10,4 gam hỗn hợp rắn gồm MgO (a mol) và Fe2O3 (1,5b + 0,5c) mol. Từ dữ kiện đề bài ta có hệ sau
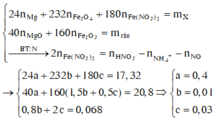

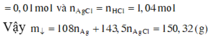

Đáp án A
Sơ đồ:
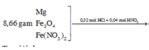
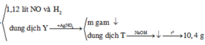
Ta giải được: ![]()
Do có sinh ra khí H2 nên dung dịch Y coi như đã hết NO 3 - .
Gọi a, b, c lần lượt là số mol 3 chất trong X
![]()
T tác dụng với NaOH lọc kết tủa rồi nung thu được 10,4 gam rắn gồm MgO và Fe2O3.
![]()
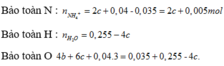
Giải hệ :a=0,2 ;b=0,005; c=0,015.
Kết tủa khi cho AgNO3 vào gồm AgCl 0,52 mol và Ag
Bảo toàn e:
![]()
→ m = 75,16 gam

Đáp án A
Sơ đồ:
8 , 66 g a m M g F e 3 O 4 F e ( N O 3 ) 2 → 0 , 52 m o l H C l + 0 , 04 m o l H N O 3 1 , 12 l i t N O v à H 2 d u n g d ị c h Y → + A g N O 3 m g a m ↓ d u n g d ị c h T → N a O H ↓ → t 0 10 , 4 g a m
Ta giải được:
![]()
Do có sinh ra khí H2 nên dung dịch Y coi như đã hết N O - 3 .
Gọi a, b, c lần lượt là số mol 3 chất trong X
=> 24a + 232b + 180c = 8,66
T tác dụng với NaOH lọc kết tủa rồi nung thu được 10,4 gam rắn gồm MgO và Fe2O3.
=> 40a + 240b + 80c = 10,4
Bảo toàn N :
n N H + 4 = 2c + 0,04 - 0,035 = 2c + 0,005 mol
Bảo toàn H : n H 2 O = 0 , 255 - 4 c
Bảo toàn O 4b + 6c + 0,04.3 = 0,035 + 0,255 - 4c
Giải hệ :a=0,2 ;b=0,005; c=0,015.
Kết tủa khi cho AgNO3 vào gồm AgCl 0,52 mol và Ag
Bảo toàn e:
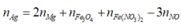
![]()
=> m = 75,16 gam

Đáp án A
Đặt số mol Mg, F e 3 O 4 v à F e ( N O 3 ) 2 lần lượt là x, y , z mol
Hỗn hợp khí có 30 > M > 21,6 > 2 và có 1 khí hóa nâu => Z gồm NO: a mol và H 2 : b mol
Khi đó ta có hệ 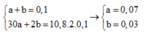
Vì sinh ra H 2 nên toàn bộ lượng N O 3 - trong F e ( N O 3 ) 2 v à H N O 3 chuyển hóa thành NO: 0,07 mol và N H 4 +
Bảo toàn nguyên tố N ![]()
Luôn có ![]()
![]()
![]()
![]()
Trong 20,8 gam chất rắn gồm MgO: x mol và ![]()
Ta có hệ 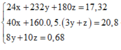
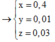
Bảo toàn electron cho toàn bộ quá trình ![]()
![]()
=>Kết tủa thu được AgCl: 1,04 mol, Ag: 0,01 mol ![]() = 150,32 gam
= 150,32 gam

Đáp án A
· Có n Al ( B ) = 2 3 . n H 2 = 2 3 . 0 , 672 22 , 4 = 0 , 02 mol
· Chất rắn thu được sau khi nung là Al2O3:
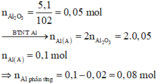
· Quy đổi A tương đương với hỗn hợp gồm 0,1 mol Al, a mol Fe, b mol O
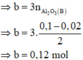
· Phần không tan D gồm Fe và oxit sắt + H2SO4 ® Dung dịch E + 0,12 mol SO2
Dung dịch E chứa một muối sắt duy nhất và không hòa tan được bột Cu
Þ Muối sắt là FeSO4.
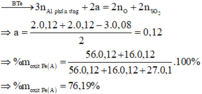









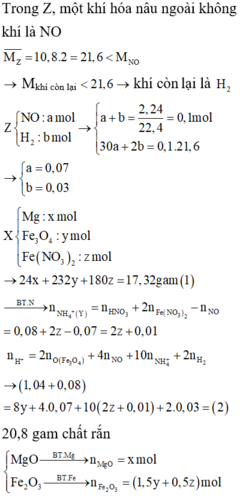


"Cho phép tôi sửa lại đề" : Hòa tan hoàn toàn hỗn hợp A gồm 2 kim loại Mg, Cu vào một lượng vừa đủ dung dịch H2SO4 70 %, đun nóng . Sau phản ứng thu được 1,12 lít khí SO2 và dung dịch B . Cho dung dịch B tác dụng với NaOH dư thu được kết tủa C. Nung kết tủa C đến khối lượng không đổi được hỗn hợp rắn D . Cho D tác dụng với lượng H2 dư đến phản ứng hoàn toàn thu được 2,72 gam hỗn hợp chất rắn F .
1) Tính khối lượng của Mg và Cu có trong hỗn hợp A
2)Khi cho 6,8 gam nước vào dung dịch B thu được dung dịch H . Tính nồng độ phần trăm các chất trong dung dịch H
BÀI GIẢI :
1) Đặt nMg = a (mol) ; nCu = b (mol)
Vì dung dịch H2SO4 có nồng độ 70% nên đây là một acid đã có độ đặc cao
Mg + 2H2SO4đ → MgSO4 + SO2↑ + 2H2O (to) (1)
a................2a.......................a...............a.................(mol)
Cu + 2H2SO4đ → CuSO4 + SO2↑ + 2H2O (to)(2)
b.................2b........................b...............b................(mol)
nSO2 = 1,12 / 22,4 = 0,05 (mol)
Ta có : nSO2 = a + b = 0,05 (I)
Dung dịch B có a mol MgSO4 , b mol CuSO4
MgSO4 + 2NaOH → Mg(OH)2↓ + Na2SO4 (3)
a..................................................a (mol)
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4 (4)
b.....................................................b (mol)
kết tủa C là Mg(OH)2 : a mol và Cu(OH)2 : b mol
Nung C :
Mg(OH)2 → MgO + H2O (to) (5)
a........................a..............(mol)
Cu(OH)2 → CuO + H2O (to) (6)
b...............................b (mol)
rắn D gồm : a mol MgO , b mol CuO
Rắn D + H2 (dư)
MgO + H2 → (không pư ) (7)
CuO + H2 → Cu + H2O (to) (8)
b........................b (mol)
rắn F gồm a mol MgO và b mol Cu
Ta có : mF = mMgO + mCu
<=> 40a + 64b = 2,72 (II)
Giair hệ pt (I ) và (II) ta được
a = 0,02 (mol)
b = 0,03 (mol)
Vậy : mMg = 24 * 0,02 = 0,48 (gam)
mCu = 64*0,03 = 1,92 (gam)
2) từ các phương trình (1) , (2)
=> nH2SO4(bđ) = 2a + 2b
= 2*0,02 + 2*0,03
= 0,1 (mol)
=> mH2SO4 = 0,1 * 98 = 9,8 (gam)
=> m(ddH2SO4) = \(\frac{mH2SO4\cdot100\%}{C\%}\) = \(\frac{9,8\cdot100\%}{70\%}\) = 14 (gam)
m(hh đầu) = mA = mMg + mCu = 0,48 + 1,92 = 2,4 (gam)
m(ddB) = m(hh đầu) + m(ddH2SO4) - mSO2
= 2,4 + 14 - 0,05 *64 (số mol SO2 ở I)
= 13,2 (gam)
m(ddsaukhithemnuoc) = m(ddB) + m(H2O)
= 13,2 + 6,8
= 20 (gam)
Vậy : C%\(_{MgSO4}\) = \(\frac{mMgSO4}{m\left(ddsaukhithemnuoc\right)}\) = \(\frac{120a}{20}\cdot100\%\) = \(\frac{120\cdot0,02}{20}\cdot100\%\) = 12 (%) C%\(_{CuSO4}\) = \(\frac{mCuSO4}{m\left(ddsaukhithemnuoc\right)}\cdot100\%\) = \(\frac{160b}{20}\cdot100\%\) = \(\frac{160\cdot0,03}{20}\cdot100\%\)
= 24 (%)