cho 1,41g hỗn hợp 2 kim loại Al và Mg tác dụng với dung dịch H2SO4 dư phản ứng xong thu được 1568ml khí đktc .Tính thành phần phần trăm theo khối lượng và theo số mol của mỗi kim loại trong hỗn hợp đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


2Al + 3H2SO4 -> Al2(SO4)3 + 3H2 (1)
2 3 1 3 ( mol)
2x 3x x 3x
Mg + H2SO4 -> MgSO4 +H2 (2)
1 1 1 1
y y y y
Gọi số mol của Al là x
=> nAl = 2x, nH2SO4 = 3x, nAl2(SO4)3= x , nH2= 3x
Gọi số mol của Mg là y
=> nMg = y, nH2SO4 = y, nMgSO4 = y, nH2= y
Ta có:
mhh = mAl + mMg
1,41= 27.2x + 24y
1,41= 54x + 24y
V H2 (1) + V H2 (2) = 1,568 (1568ml = 1,568 l)
22,4 . 3x + 22,4y = 1,568
67,2x + 22.4y = 1,568
Có : - 54x + 24y=1,41
- 67,2x + 22.4y = 1,568
Bấm máy tính => x = 0,015
y = 0,025
mAl = 54x = 54 . 0,015 = 0,81 9(g)
mMg = 1,41 - 0,81 = 0,6 (g)
%mAl = 0,81 . 100 / 1,41 = 57,45%
%mMg = 100% - 57,45% = 42,55%

Gọi số mol Al, Mg là a, b
=> 27a + 24b = 1,41
\(n_{H_2}=\dfrac{1,568}{22,4}=0,07\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
_____a-------------------------------->1,5a
Mg + 2HCl --> MgCl2 + H2
b----------------------->b
=> 1,5a + b = 0,07
=> a=0,03 ; b = 0,025
=> \(\left\{{}\begin{matrix}\%Al=\dfrac{27.0,03}{1,41}.100\%=57,447\%\\\%Mg=\dfrac{0,025.24}{1,41}.100\%=42,553\%\%\end{matrix}\right.\)

PTHH:
Zn + H2SO4 ---> ZnSO4 + H2 (1)
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2 (2)
Ta có: \(n_{H_2}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
Gọi x, y lần lượt là số mol của Zn và Al
a. Theo PT(1): \(n_{H_2}=n_{Zn}=x\left(mol\right)\)
Theo PT(2): \(n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}y\left(mol\right)\)
=> \(x+\dfrac{3}{2}y=0,8\) (*)
Theo đề, ta có: 65x + 27y = 3,79 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}x+\dfrac{3}{2}y=0,8\\65x+27y=3,79\end{matrix}\right.\)
(Ra số âm, bn xem lại đề nhé.)

Gọi số mol Zn, AL là a, b (mol)
=> 65a + 27b = 3,79 (1)
\(n_{H_2}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
PTHH: Zn + H2SO4 --> ZnSO4 + H2
a---->a------------------->a
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
b---->1,5b-------------------->1,5b
=> a + 1,5b = 0,08 (2)
(1)(2) => a = 0,05; b = 0,02
=> \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,05.65}{3,79}.100\%=85,752\%\\\%m_{Al}=\dfrac{0,02.27}{3,79}.100\%=14,248\%\end{matrix}\right.\)
\(n_{H_2SO_4}=a+1,5b=0,08\left(mol\right)\)
=> \(m_{H_2SO_4}=0,08.98=7,84\left(g\right)\)
Zn + H2SO4 -> ZnSO4 + H2
a -> a
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
b -> 1.5b
HPT: 65a+27b=3.79
a + 1.5b = 1.792/22.4= 0.08
Giải HPT ta được a=0.05 b=0.02
mZn = 0.05*65=3.25 (g)
mAl= 0.02*27=0.54 (g)

a) Gọi `n_{Al} = a (mol); n_{Fe} = b (mol)`
PTHH:
`2Al + 3H_2SO_4 -> Al_2(SO_4)_3 + 3H_2`
`Fe + H_2SO_4 -> FeSO_4 + H_`
b) `n_{H_2} = (0,56)/(22,4) = 0,025 (mol)`
Theo PT: `n_{H_2} = n_{Fe} + 3/2 n_{Al}`
`=> b + 1,5a = 0,025`
Giải hpt \(\left\{{}\begin{matrix}27a+56b=0,83\\1,5a+b=0,025\end{matrix}\right.\Leftrightarrow a=b=0,01\)
=> \(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,01.27}{0,83}.100\%=32,53\%\\\%m_{Fe}=100\%-32,53\%=67,47\%\end{matrix}\right.\)

2Al + 6HCl → 2 A l C l 3 + 3 H 2
a……….3/2.a (mol)
Mg + 2HCl → M g C l 2 + H 2
b....................b (mol)
4 gam rắn không tan là Cu, gọi số mol của Al và Mg lần lượt là a và b (mol). Ta có:
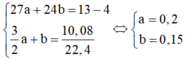
⇒ % m C u = 4 13 .100 = 30,77 % ⇒ % m A l = 0,2.27 13 .100 = 41,54 % ⇒ % m M g = 100 % − 30,77 % − 41,54 % = 27,69 %
⇒ Chọn C.

Mg+2HCl->MgCl2+H2
x x
2Al+6HCl->2AlCl3+3H2
y 3/2 y
mMg+mAl=23.4
->24x+27y=23.4
nH2=1.2(mol)
x+3/2 y=1.2
x=0.3(mol)->mMg=7.2(g)
y=0.6(mol)_>mAl=16.2(g)
Bạn tự tính % nhé ^^

Bài 1: Sửa đề: 1,53g hỗn hợp 2 kim loại
Khí sinh ra: H2
Gọi nAl = x, nMg = y
=> 27x + 24y = 1,53 (1)
Bảo toàn e
3x + 2y = 2.\(\dfrac{1,68}{22,4}=0,15mol\)(2)
Từ (1) + (2) => x = 0,03, y = 0,03
%mAl = \(\dfrac{0,03.27}{1,53}.100\%=52,94\%\)
%mMg = 47,06%

a)\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Mol: x 1,5x
PTHH: Mg + H2SO4 → MgSO4 + H2
Mol: y y
Ta có: \(\left\{{}\begin{matrix}27x+24y=5,1\\1,5x+y=0,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{0,1.27.100\%}{5,1}=52,94\%;\%m_{Mg}=100-52,94=47,06\%\)
b)
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Mol: 0,1 0,15 0,05
PTHH: Mg + H2SO4 → MgSO4 + H2
Mol: 0,1 0,1 0,1
\(m_{ddH_2SO_4}=\dfrac{\left(0,1+0,15\right).98.100}{9,8}=250\left(g\right)\)
mdd sau pứ = 5,1+250-0,15.2 = 254,8(g)
\(C\%_{ddAl_2\left(SO_4\right)_3}=\dfrac{0,05.342.100\%}{254,8}=6,71\%\)
\(C\%_{ddMgSO_4}=\dfrac{0,1.120.100\%}{254,8}=4,71\%\)
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2 (1)
2 3 1 3 ( mol)
2x 3x x 3x
Mg + H2SO4 -> MgSO4 +H2 (2)
1 1 1 1
y y y y
Gọi số mol của Al là x
=> nAl = 2x, nH2SO4 = 3x, nAl2(SO4)3= x , nH2= 3x
Gọi số mol của Mg là y
=> nMg = y, nH2SO4 = y, nMgSO4 = y, nH2= y
Ta có:
mhh = mAl + mMg
1,41= 27.2x + 24y
1,41= 54x + 24y
V H2 (1) + V H2 (2) = 1,568 (1568ml = 1,568 l)
22,4 . 3x + 22,4y = 1,568
67,2x + 22.4y = 1,568
Có : - 54x + 24y=1,41
- 67,2x + 22.4y = 1,568
Bấm máy tính => x = 0,015
y = 0,025
mAl = 54x = 54 . 0,015 = 0,81 9(g)
mMg = 1,41 - 0,81 = 0,6 (g)
%mAl = 0,81 . 100 / 1,41 = 57,45%
%mMg = 100% - 57,45% = 42,55%
nH2 = 0,07 mol
Đặt nAl = x ( mol ); nMg = y ( mol ); ( x,y > 0 )
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2 (1)
Mg + 2HCl \(\rightarrow\) MgCl2 + H2 (2)
Từ (1)(2) ta có hệ pt
\(\left\{{}\begin{matrix}27x+24y=1,41\\1,5x+y=0,07\end{matrix}\right.\)
\(\Rightarrow\) \(\left\{{}\begin{matrix}x=0,03\\y=0,025\end{matrix}\right.\)
\(\Rightarrow\) %mAl = \(\dfrac{0,03.27.100}{1,41}\) \(\approx\) 57,4%
\(\Rightarrow\) %mMg = \(\dfrac{0,025.24.100}{1,41}\) \(\approx\) 42,5%
\(\Rightarrow\) %nAl = \(\dfrac{0,03.100}{0,03+0,025}\)\(\approx\) 54,5%
\(\Rightarrow\) %nMg = \(\dfrac{0,025.100}{0,03+0,025}\) \(\approx\) 45,5%