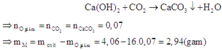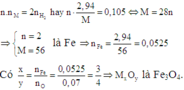Nhờ mn giải giúp mik mấy bài hóa HSG này vs, mik đag rất cần,mik tks nhiều:
Câu 1: Khử hoàn toàn 8,12g một ôxit kim loại bằng khí CO ở nhiệt độ cao. Dẫn toàn bộ khí sinh ra vào bình đựng dd Ca(OH)2 dư thấy tạo thành 14g kết tủa. Nếu lấy lượng kim loại sinh ra hòa tan hết vào dd HCl dư thì thu đc 2,352l khí ở đktc. Xác định công thức của ôxit kim loại.
Câu 2: Cho 13,12g tinh thể Al2(SO4)3. 18H2O hòa tan vào nước đc dd A. Cko 250ml dd KOH PƯ hết với dd A thu đc 1,17g kết tủa. Tính nồng độ mol của dd KOH có thể sử dụng để tạo kết tủa trên.
Câu 3: Trộn 100g dd chứa muối Sunfát của một kin loại kiềm, nồng độ 16,4% với 100g dd KHCO3 4,4%. Sau khi PƯ kết thức thu đc dd A có khối lượng < 200g. Cho 200g dd BaCl2 6,24% vào dd C thu đc dd D. dd D còn có thể PƯ đc vs dd H2SO4. Hãy Xác định công thức muối sunfát kim loại kiềm ban đầu.
Câu 4: Đun nóng 16,8l khí hiđro (đktc) với Cacbon ở 500 độ C và có Ni làm xúc tác, thu đc hh khí gồm CH4 và H2. Tỷ khối hơi của hh khí so vs hiđo bằng 4,5. Đốt cháy hoàn toàn hh khí đó rồi cho sản phẩm hấp thụ vào 200ml dd NaOH 8% (d=1,1g/ml).
1- Tính hiệu suất PƯ giữa hiđro và Cacbon
2- Tính nồng độ mol/lít của dd thu đc sau PƯ đốt cháy hh