Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Các phản ứng xảy ra:
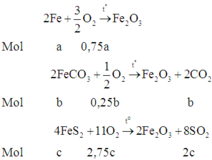
Vì áp suất trước và sau phản ứng không đổi nên số mol khí phản ứng bằng số mol khí sinh ra (tổng thể tích khí trong bình không thay đổi).
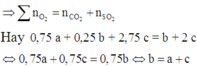

Đáp án D
Sơ đồ quá trình phản ứng:
C + H2O → hh X = {H2; CO; CO2} || X + a mol Fe3O4; b mol CuO → 25,92 gam hh Y.
(2a + 0,5b) mol H2 + hh Y → {Fe; Cu} + H2O.
Gọi số mol {CO; H2} trong X là z mol → cần đúng z mol O trong oxit đề → {CO2; H2O}.
→ 160a + 80b = 25,92 + 16z (1). Lại có để chuyển hết (3a + b) mol O trong oxit → {CO2; H2O}
thì cần vừa đủ z + 2a + 0,5b mol hh {CO; H2} → 3a + b = z + 2a + 0,5b ↔ a + 0,5b = z (2).
Từ (1) và (2) ta có z = 0,18 mol. Đến đây có 2 hướng xử lí:
cách 1: thường các bạn sẽ tìm mối ràng buộc nữa thì C + H2O → CO + H2 || C + 2H2O → CO2 + 2H2.
Bằng cách gọi số mol C ở các pt lần lượt là x, y mol → 2x + 3y = 0,2 mol
và 2x + 2y = nhh CO + H2 0,18 mol. Giải tìm ra đáp án C. ♣.
Theo hướng này có thể nhanh hơn như sau: nCO2 = 0,2 - z = 0,02 mol.
Thay vào 2 phương trình trên cũng ra kết quả tương tự.
cách 2: có thể đi theo hướng sau: hiểu rõ vấn đề + rút gọn suy nghĩ, cần hình dung:
C + H2O →....→.... cuối cùng sẽ thu được CO2 + H2O.
như vậy 0,18 mol O là ở trong CO2 luôn → có 0,09 mol C.
→ trong Y có 0,09 mol CO và CO2 (bảo toàn C) → có 0,11 mol H2O
→ mY = 0,09 × 44 + 0,11 × 18 - 0,18 × 16 = 3,06 gam. → dY/H2 = 3,06 ÷ 0,2 ÷ 2 = 7,65.
Chọn đáp án C.
p/s: bài toán này khai thác điểm đặc biệt Fe2O3 và CuO có M = 160 và 80 + bản chất CO và H2 cùng nhận 1 O.

1. Giả sử hỗn hợp A có X mol C n H 2 n + 2 và y mol C m H 2 m + 2 :
(14n + 2)x + (14m + 2)y = 1,36 ⇒ 14(nx + my) + 2(x + y) = 1,36 (1)
Khi đốt hỗn hợp A:
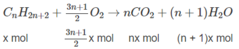
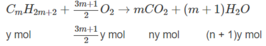
n C O 2 = n C a C O 3 = 0,09(mol)
⇒ nx + my = 0,09 (2)
Từ (1) và (2), tìm được x + y = 0,05.
Số mol O 2 trước phản ứng: n O 2 = 0,2(mol).
Tổng số mol khi trước phản ứng: 0,2 + 0,05 = 0,25 (mol).
Nếu ở đktc thì V O = 0,25.22,4 = 5,6 (lít).
Thực tế V 1 = 11,2 (lít)
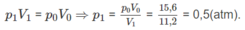
Số mol hơi nước: (n + 1)x + (m + 1)y = nx + my + x + y = 0,14
Số mol O 2 dự phản ứng:
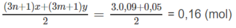
Số mol O 2 còn dư: 0,2 - 0,16 = 0,04 (mol).
Tổng số mol khí sau phản ứng: 0,09 + 0,14 + 0,04 = 0,27 (mol).
Nếu ở đktc thì V ' O = 0,27.22,4 = 6,048 (lít)
Thực tế V 2 = 11,20 (lít)
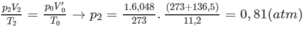
2) Nếu n < m thì x = 1,5y;
Vậy x = 0,03; y = 0,02
0,03n + 0,02m = 0,09 ⇒ 3n + 2m = 9
3n = 9 - 2m 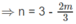
n và m nguyên dương nên m = 3 và n = 1.
C H 4 chiếm 60% thể tích hỗn hợp.
C 3 H 8 chiếm 40% thể tích hỗn hợp.

Xét `a<b->H` tính theo `Fe.`
`Fe+S` $\xrightarrow{t^o}$ `FeS`
`0,5a->0,5a->0,5a(mol)`
Có `n_{Fe\ pu}=0,5a(mol)`
`Y` gồm `Fe:0,5a(mol);S:b-0,5a(mol);FeS:0,5a(mol)`
`FeS+2HCl->FeCl_2+H_2S`
`Fe+2HCl->FeCl_2+H_2`
Theo PT: `n_{H_2S}=n_{FeS}=0,5a(mol);n_{H_2}=n_{Fe}=0,5a(mol)`
`->{n_{H_2S}}/{n_{H_2}}={5.2-2}/{34-5.2}=1/3`
``->{0,5a}/{0,5a}=1/3` vô lí.
Xét `a>b->H` tính theo `S.`
`Fe+S` $\xrightarrow{t^o}$ `FeS`
`0,5b←0,5b->0,5b(mol)`
Có `n_{S\ pu}=0,5b(mol)`
`Y` gồm `Fe:a-0,5b(mol);S:0,5b(mol);FeS:0,5b(mol)`
`FeS+2HCl->FeCl_2+H_2S`
`Fe+2HCl->FeCl_2+H_2`
Theo PT: `n_{H_2S}=n_{FeS}=0,5b(mol);n_{H_2}=n_{Fe}=a-0,5b(mol)`
`->{n_{H_2S}}/{n_{H_2}}={5.2-2}/{34-5.2}=1/3`
``->{0,5b}/{a-0,5b}=1/3`
`->1,5b=a-0,5b`
`->a=2b`
`->a:b=2:1`





Chọn đáp án B