
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.




c, \(2H_2+O_2 \rightarrow2H_2O\)
\(n_{H_2}=\dfrac{33,6}{22,4}=1,5(mol) \Rightarrow n_{O_2}=0,75(mol)\)
\(V_{O_2}=22,4.0,75=16,8(l)\)
\(n_{H_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\)
a. PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Theo PTHH: \(n_{Fe}=n_{H_2}=1,5\left(mol\right)\)
\(\Rightarrow m_{Fe}=56\cdot1,5=84\left(g\right)\)
b. Đổi: \(500ml=0,5l\)
\(CM_{H_2SO_4}=\dfrac{1,5}{0,5}=3M\)
c. \(2H_2+O_2\rightarrow2H_2O\)
Theo PTHH: \(n_{O_2}=\dfrac{1}{2}n_{H_2}=\dfrac{1}{2}\cdot1,5=0,75\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,75\cdot22,4=16,8\left(l\right)\)

Caai 7 :
a) C2H4 + Br2 $\to$ C2H4Br2
b) Theo PTHH : n C2H4 = n Br2 = 8/160 = 0,05(mol)
%V C2H4 = 0,05.22,4/2,24 .100% = 50%
%V CH4 = 100% -50% = 50%
Câu 8 :
a) C2H5OH = a(mol) => n CH3COOH = 2a(mol)
$C_2H_5OH + Na \to C_2H_5OH + \dfrac{1}{2}H_2$
$CH_3COOH + Na \to CH_3COONa + \dfrac{1}{2}H_2$
Theo PTHH :
n H2 = 1/2 n C2H5OH + 1/2 n CH3COOH = 0,5a + a = 3,36/22,4 = 0,15
=> a = 0,1
=> m = 0,1.46 + 0,1.2.60 = 16,6(gam)
b)
$C_2H_5OH + CH_3COOH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_3COOC_2H_5 + H_2O$
Ta thấy : n C2H5OH < n CH3COOH nên hiệu suất tính theo số mol C2H5OH
n CH3COOC2H5 = n C2H5OH pư = 0,1.80% = 0,08(mol)
m este = 0,08.88 = 7,04(gam)

$a)PTHH:ZnCl_2+2AgNO_3\to Zn(NO_3)_2+2AgCl\downarrow$
$b)n_{ZnCl_2}=\dfrac{200.13,6\%}{136}=0,2(mol)$
Theo PT: $n_{AgNO_3}=2n_{ZnCl_2}=0,4(mol)$
$\Rightarrow C\%_{AgNO_3}=\dfrac{0,4.170}{200}.100\%=34\%$
$c)$ Theo PT: $n_{AgCl}=0,4(mol);n_{Zn(NO_3)_2}=0,2(mol)$
$\Rightarrow m_{AgCl}=0,4.143,5=57,4(g)$
$m_{Zn(NO_3)_2}=0,2.189=37,8(g)$
$\Rightarrow C\%_{Zn(NO_3)_2}=\dfrac{37,8}{200+200-57,4}.100\%\approx 11,03\%$
a) \(ZnCl_2+2AgNO_3\rightarrow Zn\left(NO_3\right)_2+2AgCl\)
b) \(m_{ZnCl_2}=\dfrac{200.13,6}{100}=27,2\left(g\right)\)
=> \(n_{ZnCl_2}=\dfrac{27,2}{136}=0,2\left(mol\right)\)
PTHH: ZnCl2 + 2AgNO3 --> Zn(NO3)2 + 2AgCl
0,2------>0,4--------->0,2-------->0,4
=> \(C\%\left(AgNO_3\right)=\dfrac{0,4.170}{200}.100\%=34\%\)
c)
mdd sau pư = 200 + 200 - 0,4.143,5 = 342,6(g)
=> \(C\%\left(Zn\left(NO_3\right)_2\right)=\dfrac{0,2.189}{342,6}.100\%=11,03\%\)

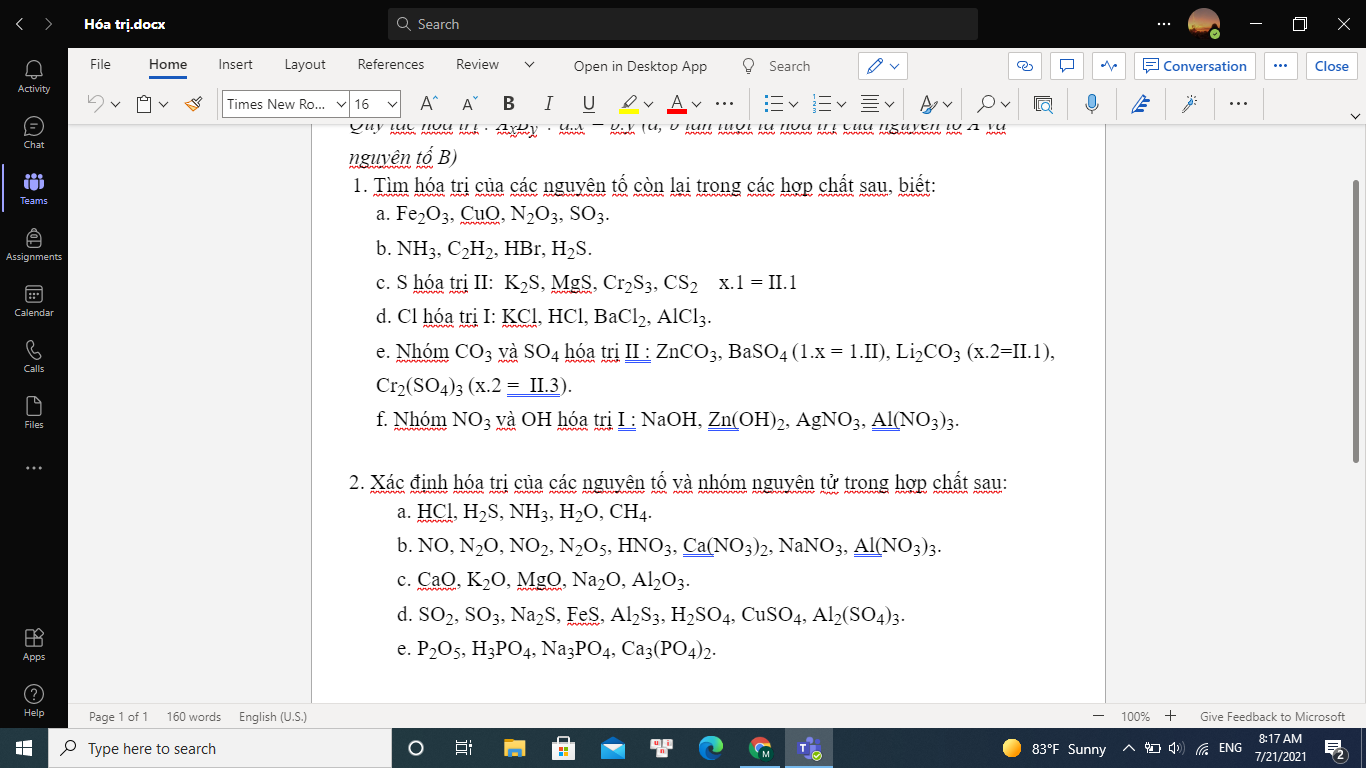
1/ Gọi x là hóa trị của nguyên tố cần tìm. Áp dụng quy tắc hóa trị:
a) Fe2O3 : x.2=II.3 => x=III
CuO : x.1=II.1 => x=II
N2O3 : x.2=II.3 => x=III
SO3: x.1=II.3 => x= VI
b) NH3 : x.1=I.3 => x=III
C2H2 : C hóa trị IV, H hóa trị I ( do trong hợp chất hữu cơ, hóa trị của C luôn là IV)
HBr : I.1=x.1 => x=I
H2S: I.2=x.1 => x=II
c)K2S: x.2=II.1 => x=I
MgS : x.1=II.1 => x=II
Cr2S3 : x.2=II.3 => x=III
CS2: x.1=II.2=> x=IV
d) KCl: x.1=I.1=> x=I
HCl: x.1= 1.I => x=I
BaCl2 : x.1=I.2 => x=II
AlCl3 : x.1=I.3 => x=III
e) ZnCO3 : x.2=II.1 => x=II
BaSO4 : x.1=II.1 => x=II
Li2CO3 : x.2=II.1 => x=I
Cr2(SO4)3 : x.2=II.3 => x=III
f) NaOH : x.1=1.I => x=I
Zn(OH)2 : x.1=I.2 => x=II
AgNO3 : x.1=I.1 => x=I
Al(NO3)3 : x.1=I.3 => x=III
2.a) HCl : H(I), Cl(I)
H2S: H(I), S(II)
NH3 : N(III), H(I)
H2O : H(I), O(II)
CH4: C(IV), H(I)
b) NO: N(II), O(II)
N2O: N(I), O(II)
NO2: N(IV), O(II)
N2O5: N(V), O(II)
HNO3 : H(I), NO3 (I)
Ca(NO3)2 : Ca(II), NO3 (I)
NaNO3: Na(I), NO3 (I)
Al(NO3)3: Al (III),NO3 (I)
c) CaO: Ca(II), O(II)
K2O: K(I), O(II)
MgO : Mg(II), O(II)
Na2O: Na(I), O(II)
Al2O3: Al(III), O(II)
d) SO2: S(IV) ,O(II)
SO3: S(VI), O(II)
Na2S: Na(I), S(II)
FeS: Fe(II), S(II)
Al2S3: Al(III), S(II)
H2SO4: H(I), SO4(II)
CuSO4: Cu(II), SO4(II)
Al2(SO4)3: Al(III), SO4(II)
e) P2O5: P(V), O(II)
H3PO4: H(I), PO4(III)
Na3PO4: Na(I), PO4(III)
Ca3(PO4)2: Ca(II), PO4(III)

Câu 2.
\(n_{Cu}=\dfrac{3,2}{64}=0,05mol\)
\(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\)
0,05 0,1 0,05 0,1
\(C_{M_{AgNO_3}}=\dfrac{0,1}{0,2}=0,5M\)
Câu 1:
a.Chất cháy được trong không khí là H² vì Fe tác dụng với HCl tạo H² không màu và cháy được trong không khí
PT: Fe + 2HCl --> FeCl² +H²
b.Chất làm đục nước vôi trong là CaO
PT:CaO + 2HCl --> CaCl² + H²O
c.Dung dịch có màu xanh là Cu
PT: Cu + 2HCl --> CuCl² + H²
d.Dung dịch không màu và nước là CaCO³
PT: CaCO³ + HCl --> CaCl² + CO² + H²O ( vì HCO³ là dung dịch yếu nên không tồn tại lâu vậy đã tách ra thành CO² và H²O)

a)
$CH_3COOH + KOH \to CH_3COOK + H_2O$
n CH3COOH = n KOH = 0,1(mol)
$CH_3COOH + 2O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O$
$C_2H_5OH + 3O_2 \xrightarrow{t^o} 2CO_2 + 3H_2O$
$CO_2 +C a(OH)_2 \to CaCO_3 + H_2O$
2n C2H5OH + 2n CH3COOH = n CO2 = n CaCO3 = 60/100 = 0,6(mol)
=> n C2H5OH = (0,6 - 0,1.2)/2 = 0,2(mol)
=> n O2 = 2n CH3COOH + 3n C2H5OH = 0,1.2 + 0,2.3 = 0,8(mol)
=> V O2 = 0,8.22,4 = 17,92 lít
b) m = 0,1.60 + 0,2.46 = 15,2 gam
%m CH3COOH = 0,1.60/15,2 .100% = 39,47%
%m C2H5OH = 100%- 39,47% = 60,53%
 giúp mình câu 8 với
giúp mình câu 8 với

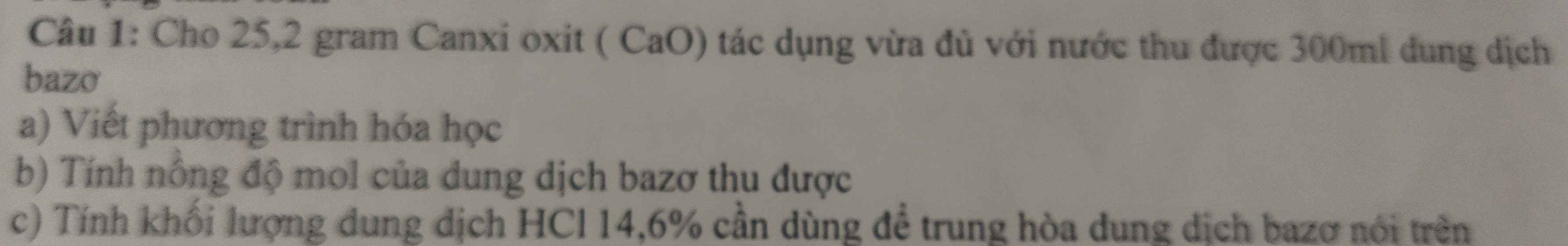
 giúp mình câu c với ạ, 2 câu trên mình biết làm rồi
giúp mình câu c với ạ, 2 câu trên mình biết làm rồi


Câu 8:
a, \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Ta có: \(n_{CH_4}+n_{C_2H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\left(1\right)\)
Theo PT: \(n_{O_2}=2n_{CH_4}+\dfrac{5}{2}n_{C_2H_2}=\dfrac{20,8}{32}=0,65\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,2\left(mol\right)\\n_{C_2H_2}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,2.22,4}{6,72}.100\%\approx66,67\%\\\%V_{C_2H_2}\approx33,33\%\end{matrix}\right.\)
b, Theo PT: \(n_{CO_2}=n_{CH_4}+2n_{C_2H_2}=0,4\left(mol\right)\Rightarrow V_{CO_2}=0,4.22,4=8,96\left(l\right)\)