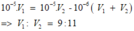Tính tỉ lệ V1 : V2
a/ Trộn V1 (ml) dd HNO3 (pH = 1) với V2 (ml) dd HNO3 (pH = 3) để được dd có pH = 2.
b/ Pha thêm V1(ml) nước vào V2 (ml) dd NaOH (pH = 13) để được dd có pH = 12
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
pH lúc sau = 3 ⇒ [H+] đầu = 10[H+]M lúc sau
⇒ V2 + V1 = 10V1 ⇒ V2 = 9V1
Đáp án A.

nHCl(cuối)=0,04.2=0,08(mol)
Ta có: 10V1=0,08
<=>V1=0,008(l)=8(ml)
Mặt khác: V1+V2=40
<=>8+V2=40
<=>V2=32(ml)
Vậy: V1=8(ml); V2=32(ml)
Chúc em học tốt!
mk có chỗ thắc mắc ạ: số mol cuối thì liên quan ntn đến V1 ạ mk tưởng số mol cuối =mol sau khi trộn thêm nước.

Đáp án D
Cách 1: pH=8 => KOH dư
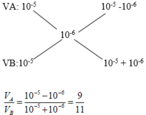
Cách 2: Do O H - dư nên ta có: