Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích: Đáp án C
R là: Na : x (mol)
M là: Al : y (mol)
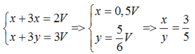

Giải thích:
Gọi số mol của Na và Al trong mỗi phần lần lượt là x và y mol
Nhận xét: Vì hai phần lượng khí H2 thu được chênh lệch nhau và phần 2 nhiều hơn phần 1 => ở phần 1 nhôm phản ứng dư. Mọi tính toán theo số mol của Na
Phần 1:
Na + H2O → NaOH + 0,5H2↑
x →x →0,5x (mol)
Al + NaOH + H2O → NaAlO2 + H2↑
x → 1,5x (mol)
Phần 2:
Na + H2O → NaOH + 0,5H2↑
x →x →0,5x (mol)
Al + NaOH dư + H2O → NaAlO2 + 1,5H2↑
y → 1,5y
Ta có: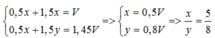
Đáp án A

Phần hai :
$2NaOH+ 2Al + 2H_2O \to 2NaAlO_2 + 3H_2$
$n_{H_2} = \dfrac{10,08}{22,4} = 0,45(mol)$
Theo PTHH : $n_{Al} = \dfrac{2}{3}n_{H_2} = 0,3(ol)$
Phần một :
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Fe + 2HCl \to FeCl_2 + H_2$
$n_{H_2} = \dfrac{13,44}{22,4} = 0,6(mol)$
Theo PTHH : $n_{H_2} = \dfrac{3}{2}n_{Al} + n_{Fe}$
$\Rightarrow n_{Fe} = 0,15(mol)$
$\Rightarrow m = 2(0,3.27 + 0,15.56) = 33(gam)$

Đáp án C
Cr2O3 + 2Al → t 0 Al2O3 + 2Cr
Phần 2: + NaOH đặc nóng → 0,075 mol H2
![]()
Phần 1: + HCl loãng, nóng → 0,15 mol H2
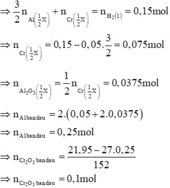
Có 0 , 1 1 < 0 , 25 2 => tính hiệu suất theo lượng Cr2O3 phản ứng.
![]()

Giải thích:
Ở phần 1 khi cho tác dụng với NaOH có sinh ra khí H2 => nhôm dư
Phần 1
nH2 = 0,0525 mol => nAl dư = 0,035 mol
chất rắn không tan tác dụng với HCl => nH2 = 0,045 mol => nFe = 0,045 mol
Phần 2
nH2 = 0,2925 mol
Giả sử phần 2 = k. phần 1
Bảo toàn e ở phần 2 ta có (3 . 0,035 + 2 . 0,045) . k = 2 . 0,2925 => k = 3
Có mA = mB = 4 khối lượng phần 1
=> tổng lượng H2 ở thí nghiệm 1 = 4 . (0,0525 + 0,045 ) = 0,39
=> nFe3O4 = (4 . 0,045) : 3 = 0,06 mol
=> 3nAl = 2.nFe3O4 + 2nH2 => nAl = 0,3 mol
=> mA = 0,3 . 27 + 0,06 . 232 = 22,02 mol
%Al = 37% và %Fe3O4 = 63%
Đáp án A
Chọn đáp án C
R là Natri (Na) và M là Nhôm (Al). Do số mol H2 ở 2 thí nghiệm khác nhau.
• phần 1: Al dư. Quy V lít về V mol. Xét phần 1 : Do Al dư ⇒ nAl phản ứng = nNa
⇒ Bảo toàn electron: nNa + 3nNa = 2nH2 ⇒ nNa = 2V ÷ 4 = 0,5V mol.
• Phần 2: NaOH dư ⇒ Al phản ứng hết. Bảo toàn electron:
nNa + 3nAl = 2nH2 ⇒ 0,5V + 3nAl = 2 × 1,45V ⇒ nAl = 0,8V mol.
⇒ nR : nM = 0,5 : 0,8 = 5 : 8.