Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
7,2 gam MCO3 + HCl → CO2 + 0,09 mol Ba(OH)2 → 0,08 mol BaCO3↓
• CO2 + Ba(OH)2 → BaCO3↓ + H2O(*)
BaCO3 + CO2 + H2O → Ba(HCO3)2 (**)
Theo (*) nCO2(*) = 0,09 mol; nBaCO3 (*) = 0,09 mol
Theo (**) nBaCO3 (**) dư = 0,08 mol → nBaCO3 (**) phản ứng = 0,09 - 0,08 = 0,01 mol
→ nCO2 (**) = 0,01 mol → ∑nCO2 = 0,1 mol
• MCO3 + 2HCl → MCl2 + CO2 + H2O
nMCO3 = nCO2 = 0,1 mol → MMCO3 = 7,2 : 0,1 = 72 → MM = 12 → Be và Mg (9 < 20 < 24)

Đáp án B
M2CO3 C → + H C l O2 + dumg dịch X → d u C a ( O H ) 2 0,2 mol CaCO3
Ta có nCO2 
Nhận thấy khi cho dung dịch Ca(OH)2 dư vào dung dịch X tạo kết tủa → trong X có chứa HCO3-
Bảo toàn nguyên tố C → nM2CO3 = nCaCO3 + nCO2 = 0,3 mol
Vậy Mtb muối =
35
0
,
3
= 116,67 → Mtb kim loại = 28,33 mà hai kim loại ở chu kì kế tiếp → Na, K. Đáp án B

Đáp án C
Gọi công thức của hai muối trong hỗn hợp ban đầu là A2CO3 và BCO3.
Có các phản ứng:
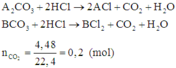
Quan sát phản ứng thấy khi cho hỗn hợp phản ứng với dung dịch HCl thì mỗi gốc C O 3 2 - trong muối được thay thế bởi hai gốc Cl-.
Có 1 mol C O 3 2 - bị thay thế bởi 2 mol Cl- thì khối lượng của muối tăng: (2.35,5 -60) = 11(gam)
Do đó khối lượng muối khan thu được khi cô cạn dung dịch là:
mmuối clorua = mmuối cacbonat + 0,2.11 = 23,8 + 0,2.11= 26 (gam)

Đáp án B
Gọi công thức trung bình của hai muối ACO3 và BCO3 là MCO3
MCO3 → MO + CO2
n C O 2 = 3,36 /22,4 = 0,15 mol → n M C O 3 = 0,15 mol
Hỗn hợp Y gồm MCO3 dư và MO
MCO3 + 2HCl → MCl2 + CO2 + H2O
MO + 2HCl → MCl2 + H2O
CO2 + Ca(OH)2 dư → CaCO3 ↓ + H2O
n C a C O 3 = 15/100 = 0,15 mol
→ n M C O 3 dư = 0,15 mol
n M C O 3 ban đầu = 0,15 + 0,15 = 0,3 mol
Bảo toàn kim loại M có:
n M C O 3 = n M C l 2 = 0,3 (mol)
Bảo toàn khối lượng có:
m M C O 3 = m M C l 2 - 0,3.(71- 60) = 29,2 (gam)

Gọi công thức trung bình của hai muối là: M ¯ 2 CO 3
Cho từ từ hỗn hợp muối cacbonat nên ta có phản ứng:
CO 3 2 - + 2 H + → CO 2 + H 2 O
Sau khi phản ứng với dung dịch axit, thêm Ba(OH)2 dư vào Y thấy xuất hiện kết tủa H+ hết và dư CO 3 2 -
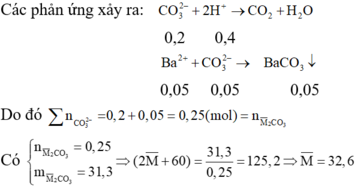
Vậy hai kim loại cần tìm là Na và K
Đáp án B.

Đáp án B
Gọi công thức trung bình của hai muối là: M2CO3.
Sau khi phản ứng với dung dịch axit, thêm Ba(OH)2 dư vào Y thấy xuất hiện kết tủa à H+ hết và dư CO32-
Các phản ứng xảy ra: CO32- + 2H+ → CO2 + H2O
0,2 0,4
CO32-dư + Ba2+ → BaCO3
0,05 0,05 0,05


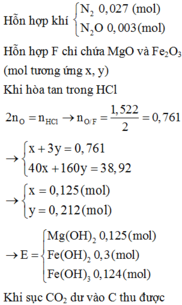

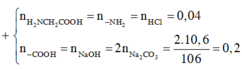

Gọi công thức chung của 2 KL là MCO3
=> MCO3 + 2HCl → MCl2 + H2O + CO2
=> nHCl = 2nCO2 = 0,3 mol; nH2O = nCO2 = 0,15 mol
Áp dụng BTKL => m muối = mMCO3 + mHCl - mH2O - mCO2
=> m muối = 14,2 + 0,3*36,5 - 0,15*18 - 0,15*44 =...
b. nMCO3 = nCO2 = 0,15 mol
=> MMCO3 = 14,2/0,15 = 94,6 =MM + MCO3
=> MM = 34,6 => 2 Kim loại là Mg (24) và Ca (40).
câu c em tự làm nhé.
d. Xét tỉ lệ nNaOH/nCO2 = 0,25/0,15 = 1,6
=> 2 muối là NaHCO3 và Na2CO3
NaOH + CO2 → NaHCO3
2NaOH + CO2 → Na2CO3 + H2O
Gọi nNaHCO3 = a mol, nNa2CO3 = b mol
BTNT Na có: nNaOH = nNaHCO3 + 2nNa2CO3 <=> 0,25=a+2b
BTNT Cacbon có nCO2 = nNaHCO3 + nNa2CO3 <=> 0,15 =a+b
=> em tự giải hệ làm nố tnhé
Đầy đủ đây nhé bạn :
1) Gọi CT chung của 2 muối cacbonat là XCO3
XCO3 + 2HCl → XCl2 + CO2↑ + H2O
nCO2 = \(\frac{3,36}{22,4}\) = 0,15 mol
nCO3 2- = nXCO3 = nCO2 = 0,15 mol
nCl- = 2nXCl2 = 2nCO2 = 0,3 mol
mXCO3 = mX 2++ mCO3 2-
→mX2+ = 14,2 - 0,15 . 60 = 5,2 (g)
mXCl2 = mX2+ + mCl- = 5,2 + 0,3 . 35,5 = 15,85 (g)
2) M XCO3 = \(\frac{14,2}{0,15}\) = 94,67
→ Mx = 34,67
2 kim loại thuộc 2 chu kì liên tiếp nhau trong bảng tuần hoàn → magie, canxi
3) Gọi số mol MgCO3, CaCO3 lần lượt là x, y
Ta có hpt:\(\left\{{}\begin{matrix}x+y=0,15\\84x+100y=14,2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,1\end{matrix}\right.\)
\(\%m_{MgCO3}=\frac{84.0,05}{14,2}.100\%=29,58\%\)
\(\%m_{CaCO3}=100\%-29,58\%=70,42\%\)
4. nCO2 = 0,15 mol
nNaOH = 0,25 . 1 = 0,25 mol
\(1< \frac{nNaOH}{nCO2}=\frac{0,25}{0,15}=1,67< 2\)
→ Phản ứng tạo hỗn hợp NaHCO3 và Na2CO3
Gọi số mol NaHCO3, Na2CO3 là a, b
CO2 + NaOH → NaHCO3
a______a_______a
CO2 + 2NaOH → Na2CO3 + H2O
b ← 2b ← b
Ta có hpt: \(\left\{{}\begin{matrix}a+b=0,15\\a+2b=0,25\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,05\\b=0,1\end{matrix}\right.\)
\(\%m_{NaHCO3}=0,05.84=4,2g\)
\(\%m_{Na2CO3}=0,1.106=10,6g\)
→ m muối = 14,8 (g)