Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a/n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\\ CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\\ n_{CO_2}=n_{CaCO_3}=0,2mol\\ m_{CaCO_3}=0,2.100=20g\\ b/BTNT\left(O\right):2n_{CO_2}=n_{H_2O}\\ \Rightarrow n_{H_2O}=0,2.2=0,4mol\\ BTNT\left(H\right):2n_{H_2O}=n_{HCl}\\ n_{HCl}=0,4.2=0,8mol\\ V_{HCl}=\dfrac{0,8}{0,4}=2l\)

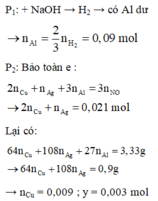
Trong 6,66g B có : 0,018 mol Cu ; 0,006 mol Ag ; 0,18 mol Al
Dung dịch C + HCl không tạo kết tủa → không có Ag+
+) Dung dịch D + thanh Fe
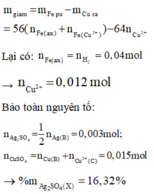
Đáp án A

Đáp án C.
Cứ 278 g FeSO4.7H2O có 152 g FeSO4
→ 55,6 g FeSO4.7H2O có x (g) FeSO4
Khối lượng FeSO4 là 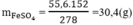
Số mol FeSO4: 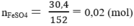
Fe + H2SO4 → FeSO4 + H2
nH2 = nFeSO4 = 0,2 (mol) ⇒ VH2 = 0,2.22,4 = 4,48 (lit)

Đáp án A
Có
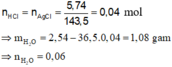
Khí thoát ra khỏi bình là CO2.
CO2 + 0,1 mol Ca(OH)2 → CaCO3 + dung dịch
Dung dịch thu được + Ba(OH)2 dư → BaCO3
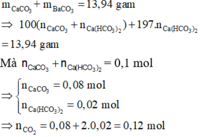
Áp dụng định luật bảo toàn khối lượng có:
mO(X) = 4,3 – 12.0,12 – 1.(2.0,06 + 0,04) – 35,5.0,04 = 1,28 gam
nO(X) = 0,08 mol
nC : nH : nO : nCl = 0,12 : 0,16 : 0,08 : 0,04 = 3:4:2:1
X có dạng C3nH4nO2nCln 107,5n < 230 n < 2,13 mà tổng số nguyên tử H và Cl phải là số chẵn n = 2
Trong phân tử X chứa 4 nguyên tử O

Chọn đáp án B
Ta có: 1 mol dung dịch X chứa x+2y mol OH-
+ Ta có 1 mol dung dịch Y chứa y+2x mol OH-
+ Vì khi cho SO42- vào vẫn còn kết tủa nên lượng kết tủa tính trong bài hoàn toàn tính theo CO32-
+ Hấp thụ hết 0,04 mol CO2 vào 200 ml dung dịch X, thu được dung dịch M và 1,97 gam kết tủa
⇒ nOH– = 0,2×(x+2y)
⇒ nBaCO3 = 0,01, nBa(HCO3)2 = 0 , 04 - 0 , 01 2 = 0,015 mol
⇒ nOH– = 0,01×2 + 0,015×2 = 0,05 mol.
⇒ x + 2y = 0,25.
+ Nếu hấp thụ hết 0,0325 mol CO2 vào 200 ml dung dịch Y thì thu được dung dịch B và 1,4775 gam kết tủa.
nBaCO3 = 0,0075 ⇒ nHCO3– = 0,0325 – 0,0075 = 0,025.
⇒ nOH– = 0,2×(2x + y) = 0,025 + 0,0075×2 = 0,04 → 2x + y = 0,2.
⇒ x = 0,05 và y = 0,1

PTHH
Fe + 2HCl --->FeCl2 + H2
0.5==1======0.5====0.5
2H2 + 02 ---->2H20
0.5========0.5
nH20=0.5
nHCl=2 =>nHCl dư=1mol
PTHH:
10FeCl2 + 6KMnO4 + 24H2SO4 ----> 3K2SO4 + 5Fe2(SO4)3 + 6MnSO4 + 10Cl2 + 24H2O
0.25======0.15========================...
2KMnO4 + 16HCl --> 2MnCl2 + 5Cl2 + 2KCl + 8H2O
0.0625=====0.5===========0.15625
Cl2 + 2FeCl2 ----->2FeCl3
=====0.25======0.25
nKMn04=0.2125mol
VKMn04=0.425
mFeCl3=40.625g
Nếu sửa nồng độ HCl thành 0.65 :
nHCl dư=1.6 mol
2KMnO4 + 16HCl --> 2MnCl2 + 5Cl2 + 2KCl + 8H2O
0.1=======0.8
nKMn04=0.25 mol
=>VKMn04=0.5 (l)
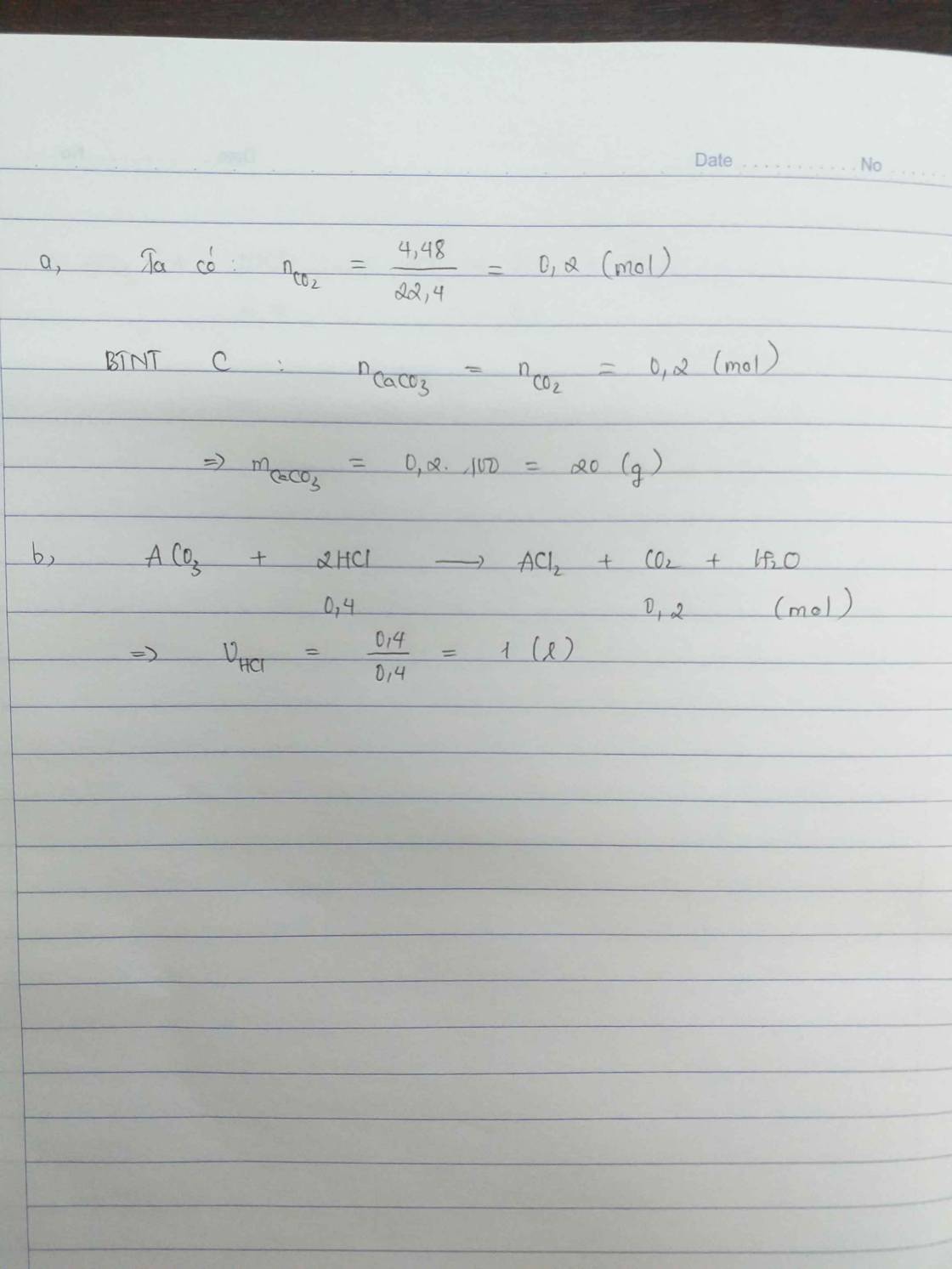
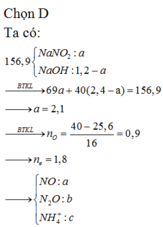
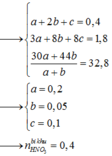
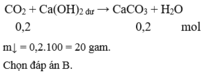
tui cảm ơn nhiều nha <3