Trong phản ứng tổng hợp Hêli. 3 7 L i + 1 1 H → 2 2 4 H e + 17 , 3 M e V . Nếu tổng hợp được 1gam Hêli thì năng lượng tỏa ra có thể đun sôi được bao nhiêu kg nước từ 0 0 C . Cho biết N A = 6 , 02 . 10 23 m o l – 1 ; C = 4 , 18 k J . k g – 1 . k – 1 M e V
A. 6 , 89 . 10 5 k g
B. 4 , 98 . 10 5 k g
C. 2 , 89 . 10 5 k g
D. 9 , 96 . 10 5 k g

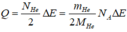
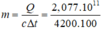
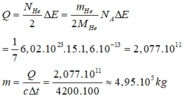

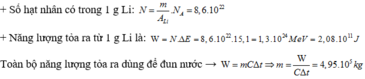
Chọn B