Hòa tan 10 gam hỗn hợp gồm Fe và FexOy bằng HCl thu được 1,12 lít H2 (đktc). Cũng lượng hỗn hợp này nếu hòa tan hết bằng dung dịch HNO3 đặc nóng thu được 5,6 lít NO2 (đktc). Công thức FexOy là
A. FeO
B. Fe3O4
C. Fe2O3
D. Fe3O4 hay FeO
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
n Fe ( NO 3 ) 3 = 0 , 4 ; n HNO 3 = 1 , 5
Áp dụng định luật bảo toàn nguyên tố cho N, ta có:
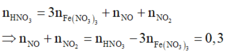
Vậy V = 0,3.22,4 = 6,72 (lít)

Quy hỗn hợp X gồm có a mol Fe, b mol Cu và c mol O
Ta có 56a + 64b + 16c= 2,44
Bảo toàn nguyên tố Fe và Cu có nFe(NO3)3= nFe= a mol;nCu(NO3)2= nCu= b mol
Khối lượng muối nitrat là
mmuối= mFe(NO3)3+ mCu(NO3)2=242a + 188b= 7,93 gam
QT cho e:
Fe→ Fe3++ 3e
a 3amol
Cu → Cu2++ 2e
b 2b
QT nhận e :
O+ 2e→ O-2
c 2c
N+5+ 3e → NO
0,045← 0,015
Theo ĐL BT electron thì : ne cho= ne nhận nên 3a+ 2b= 2c+ 0,045 (3)
Giải hệ gồm (1), (2) và (3) có a= 0,025; b= 0,01 và c= 0,025
→%mCu= 0,01.64.100%/2,44=26,23%
Đáp án C

M g + 2 F e C l 3 → M g C l 2 + 2 F e C l 2 (1)
M g + 2 H C l → M g C l 2 + H 2 (2)
Từ phản ứng (2) ta có:
n M g = n H 2 = 2,688/22,4 = 0,12 mol
Dung dịch Y gồm 3 muối ⇒ M g C l 2 , F e C l 2 , F e C l 3 ⇒ F e C l 3 sau phản ứng (1) còn dư.
⇒ n F e C l 3 (1) = 2.nMg = 2.0,12 = 0,24g
F e + 2 F e C l 3 → 3 F e C l 2 (3)
⇒ n F e C l 3 (3) = 2 n F e = 0,04 mol
⇒ n F e C l 3 b d = n F e C l 3 ( 3 ) + n F e C l 3 ( 1 )
= 0,04+0,24 = 0,28g
⇒ m X = 0,12.24 + 0,28.(56+35,5.3) = 48,3g
⇒ Chọn C.

Câu 1

Áp dụng định luật bảo toàn nguyên
tố H ta có:
nHCl = 2nH2 = 2.0,045 = 0,09 mol
Áp dụng định luật bảo toàn khối lượng
ta có: mA + mHCl = m muối + mH2
=> m = m muối + mH2 – mA = 4,575 + 0,045.2 – 0,09.36,5 = 1,38 (gam)
Câu 2

Do cho kim loại phản ứng với H2SO4 đặc và HNO3 đặc nên khí sinh ra là SO2 và NO2.
Áp dụng phương pháp đường chéo ta có:
SO2: 64 4,5
50,5
NO2: 46 13,5
→nSO2=nNO2=4,513,5=13

Đặt số mol của Fe và M lần lượt là x và y (mol)
- Khi cho hỗn hợp tác dụng với HCl:
Fe + 2HCl → FeCl2 + H2
x x (mol)
M + nHCl → MCln + 0,5nH2
y 0,5ny (mol)
nH2 = 0,045 => x + 0,5ny = 0,045 (1)
- Khi cho hỗn hợp tác dụng với HNO3 đặc và H2SO4 đặc:
Ta có các bán phản ứng oxi hóa – khử:
Fe → Fe3+ + 3e
x 3x
M → Mn+ + ne
y ny
S+6 + 2e → S+4 (SO2)
0,021 0,042
N+5 + 1e → N+4 (NO2)
0,063 0,063
Áp dụng định luật bảo toàn electron ta có: 3x + ny = 0,042 + 0,063 hay 3x + ny = 0,105 (2)
Từ (1) và (2) ta có hệ phương trình sau:

Mặt khác: mA = mFe + mM => 1,38 = 0,015.56 + My => My = 0,54(4)
Từ (3) và (4) suy ra M = 9n
Ta có bảng sau:
| n |
1 |
2 |
3 |
| M |
9 (loại) |
18 (loại) |
27 (nhận) |
Vậy kim loại M là nhôm, kí hiệu là Al.