Hoà tan hoàn toàn m gam Fe trong 200 ml dung dịch H 2 SO 4 loãng (dư), thu được dung dịch X và 2,24 lít khí H 2 (đktc). Thêm 100 ml dung dịch Ba OH 2 1M vào X, thu được 28,7 gam kết tủa. Nồng độ mol của dung dịch H 2 SO 4 ban đầu là
A. 0,7M
B. 1,4M
C. 0,8M
D. 1,0M

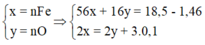
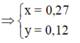
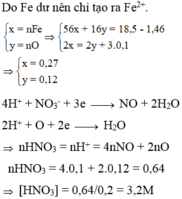

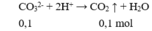
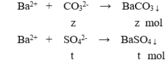
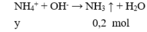
Đáp án A