Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{NH_4NO_2}=\dfrac{80}{64}=1.25\left(mol\right)\)
=> \(n_{NH_4NO_3\left(pư\right)}=\dfrac{1,25.75}{100}=0,9375\left(mol\right)\)
PTHH: NH4NO2 -to-> N2 + 2H2O
_____0,9375------>0,9375
=> VN2 = 0,9375.22,4 = 21(l)

- Đáp án A
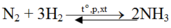
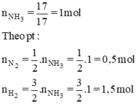
Do hiệu suất 25% nên
nN2cần dùng = 2( mol) và nH2cần dùng = 6(mol).
⇒VN2 = 2. 22,4 = 44,8 (lit) và VH2 = 22,4. 6= 134,4 (lit).

$n_{NH_3} = \dfrac{17}{17} = 1(mol)$
$N_2 + 3H_2 \xrightarrow{t^o} 2NH_3$
Theo PTHH :
$n_{N_2\ pư} = \dfrac{1}{2}n_{NH_3} = 0,5(mol)$
$n_{H_2\ pư} = \dfrac{3}{2}n_{NH_3} = 1,5(mol)$
Suy ra :
$n_{N_2\ đã\ dùng} = \dfrac{0,5}{25\%} = 2(mol)$
$n_{H_2\ đã\ dùng} = \dfrac{1,5}{25\%} = 6(mol)$
Vậy :
$V_{N_2} = 2.22,4 = 44,8(lít)$
$V_{H_2} = 6.22,4 = 134,4(lít)$

Gọi nAl = x mol ; nSn = y mol → 27x + 119y = 14,6 (1) ; nH2 = 0,25 mol
- Khi X tác dụng với dung dịch HCl:
quá trình oxi hóa:
Al -> Al3 + +3e
x -> 3x
Sn -> Sn2+ +2e
y -> 2y
Qúa trình khử
2H+ + 2e -> H2
0,5<- 0,25
=> 3x+2y=0,5 (2)
(1)(2) => x=y=0,1mol
- Khi X tác dụng O2
quá trình oxi hóa
Al -> Al3 + +3e
x -> 3x
Sn -> Sn4+ +4e
y -> 4y
Qúa trình khử
O2 + 4e -> 2O2-
VO2 = ((3x +4y)/4).22,4 = ((3.0,1+4.0,1)/4).22,4 = 3,92l => D

Chọn đáp án D
NH4NO2![]() N2 + 2H2O
N2 + 2H2O
⇒ nN2 = nNH4NO2 = 0,25 mol
⇒ VN2 = 5,6 lít

\(n_{CO_2}=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=1.0,1=0,1\left(mol\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
______0,1------->0,1--------->0,1
CaCO3 + CO2 + H2O --> Ca(HCO3)2
_0,02<--0,02
=> mCaCO3 = (0,1-0,02).100 = 8(g)

Đáp án C
NH4NO2 -> N2 + 2H2O
0,625 -> 0,625 mol
=> VN2 = 14 lit