Đem 2.6g rắn A gồm FeS, FeS2 tan hết trong dd HNO3 vừa đủ đun nóng chỉ thu được a mol NO thoát ra và dd A chứa 1 chất tan Fe2(SO4)3. Tính a
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


bảo toàn e :
( Cu2S) 0-----> 2Cu+2 + S+6 + 10e
a...........................................................10a
( FeS2)0 -----> Fe +3 + 2S+6 + 15e
b.....................................................................15b
N+5 + 3e ----> N+2
0.66 0.22
N+5 + 1e ----> N+4
0.3 0.3
Bảo toàn e: 10a+ 15b = 0.96 (1)
Bảo toàn nguyên tố :
Cu2S ---> Cu( NO3)2----> CuO
a.............................................2a
FeS2----> Fe2(SO4)3 ----> Fe2O3
b...........................................b/2
Ta đc pt: 160a+ 80b= 6.4(2)
giải (1) & (2) ----> a=0.012
b= 0.056
mdd X = 20.32 -----> B

Đáp án D
Ta có :
Fe → Fe3+ + 3e
S → S+6 + 6e
S+6 + 2e → S+4
Do đó số mol SO2 là (0,05 . 3 + 0,07.6 ) / 2= 0,285 mol
5SO2 + 2H2O + 2KMnO4 → K2SO4 + 2 MnSO4 + 2H2SO4
Nên số mol H2SO4 tạo ra là 0,114 mol
=> [H+] = 0,228 : V =0,01 => V =22,8 l

Cách 1: Quy đổi số oxi hóa
Sau toàn bộ quá trình, số oxi hóa cuối cùng của lưu huỳnh là +4 (trong SO2).
Giả sử S trong FeS2 và FeS đều là S + 4 .
Khi đó, có các quá trình nhường và nhận electron như sau:
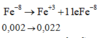
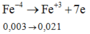
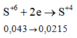

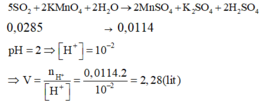
Đáp án D

Đáp án : D
Coi hỗn hợp gồm : 0,12 mol Fe ; 2x mol Cu và ( 0,24 + x) mol S
Sau phản ứng chỉ tạo muối sunfat : CuSO4 và Fe2(SO4)3
=> Bảo toàn điện tích : 3nFe + 2nCu = 2nSO4
=> 3.0,12 + 2.2x = 2.( 0,24 + x)
=> x = 0,06 mol

Vì dung dịch chỉ chứa 2 muối sunfat nên S chuyển hóa hết thành SO4(2-)
FeS2>>Fe(+3)+ 2SO4(2-)
0,12 0,12 0,24
Cu2S>>2Cu(2+) +SO4(2-)
a 2a a
Áp dụng định luật bảo toàn điện tích với các ion :Fe(3+);Cu(2+);SO4(2-)
>>0,12-3+2a*2=0,24*2+a*2>>
2a=0,12>>a=0,06mol
>>Trong dung dịch có 0,12mol Fe(+3);0,12mol Cu(+2);0,24+0,06=0,3mol SO4(2-)
>>m(muối)=m(ion)
=0,12*56+0,12*64+0,3*96=43,2g
cách nè nx
Fe2 +5NO3- + 4H+ -----> Fe3+ + 2SO42 - + 5NO +2H2O (x6)
3Cu2S + 10NO3- + 16H+ -----> 6Cu2+ + 3SO42- + 10NO + 8H2O (x1)
6FeS2 + 3Cu2S + 40H+ + 40NO3- ----->6Fe3+ +6Cu2+ +15SO42- +40NO + 20H2O
0.12----->0.06------------------------...
m= mFe3+ + mCu2+ + mSO42- = 0.12*56 + 0.12*64 + 0.3*96=43.2g


Đặt số mol của FeS và FeS2 lần lượt là x, y (mol)
+ m hỗn hợp = 88x + 120y = 2,6 (1)
+ BTNT Fe: nFe2(SO4)3 = 0,5(nFeS + nFeS2) = 0,5x + 0,5y (mol)
BTNT S: nFeS + 2nFeS2 = 3nFe2(SO4)3 => x + 2y = 3.(0,5x + 0,5y) (2)
Giải hệ (1) và (2) được x = y = 0,0125 mol => nFe2(SO4)3 = 0,0125 mol
BTNT N: nHNO3 = nNO = a (mol)
BTNT H: nH2O = 0,5.nHNO3 = 0,5a (mol)
BTNT O: 3nHNO3 = 12nFe2(SO4)3 + nNO + nH2O
=> 3a = 12.0,0125 + a + 0,5a => a = 0,1 mol
Đặt số mol của FeS và FeS2 lần lượt là x, y (mol)
+ m hỗn hợp\(\text{= 88x + 120y = 2,6 (1)}\)
+ BTNT Fe: nFe2(SO4)3 \(\text{= 0,5(nFeS + nFeS2) = 0,5x + 0,5y (mol)}\)
+ BTNT S: \(\text{nFeS + 2nFeS2 = 3nFe2(SO4)3 }\)
\(\Rightarrow\text{ x + 2y = 3.(0,5x + 0,5y) (2)}\)
Giải hệ (1) và (2) được x = y = 0,0125 mol
\(\Rightarrow\text{nFe2(SO4)3 = 0,0125 mol}\)
BTNT N: nHNO3 = nNO = a (mol)
BTNT H: nH2O = 0,5.nHNO3 = 0,5a (mol)
BTNT O: 3nHNO3 = 12nFe2(SO4)3 + nNO + nH2O
\(\text{=> 3a = 12.0,0125 + a + 0,5a => a = 0,1 mol}\)