Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ah... thí nghiệm #3 mình được làm rồi nè :3
Đầu tiên lấy que đũa chấm vào dung dịch H2SO4 đặc, sau đó chấm cái nữa vào KMnO4 khan rồi quẹt qua đèn cồn và bùm... lửa từ đâu xuất hiện :v
Giải thích thì phản ứng KMnO4 + H2SO4 đặc toả nhiều nhiệt. Khi cho qua đèn cồn thì cháy :))

Hỗn hợp X chứa x mol Fe và y mol Cu.
\(\Rightarrow56x+64y=8,8\)
Sau cùng muối thu được gồm Fe2(SO4)3 và CuSO4
Bảo toàn các nguyên tố kim loại:
\(n_{Fe2\left(SO4\right)3}=\frac{1}{2}n_{Fe}=0,5x\)
\(n_{CuSO4}=n_{Cu}=y\)
\(\Rightarrow400.0,5x+160y=23,2\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,02\\y=0,12\end{matrix}\right.\)
\(m_{Fe}=0,02.56=1,12\left(g\right)\)
\(\Rightarrow\%m_{Fe}=\frac{1,12}{8,8}.100\%=12,73\%\)

Quy đổi X thành \(\left\{{}\begin{matrix}FeO:a\left(mol\right)\\Fe_2O_3:b\left(mol\right)\end{matrix}\right.\)
Phần 1: \(\left\{{}\begin{matrix}FeCl_2:0,5a\left(mol\right)\\FeCl_3:b\left(mol\right)\end{matrix}\right.\)
=> 127.0,5a + 162,5b = 74,15
=> 63,5a + 162,5b = 74,15 (1)
Phần 2: \(\left\{{}\begin{matrix}FeCl_2:0,5a\left(mol\right)\\FeCl_3:b\left(mol\right)\end{matrix}\right.\)
PTHH: 2FeCl2 + Cl2 --> 2FeCl3
0,5a------------>0,5a
=> 162,5(0,5a + b) = 81,25
=> 0,5a + b = 0,5 (2)
(1)(2) => a = 0,4 (mol); b = 0,3 (mol)
=> m = 0,4.72 + 0,3.160 = 76,8 (g)

- Chất rắn không tan trong HCL dư là S => m S dư = 3,8g
Kết tủa đen là CuS => n CuS = 0,1 = n H 2 S = nS phản ứng
m S phản ứng = 3,2g
0,2 mol Z gồm 0,1 mol H 2 S và 0,1 mol H 2
m ban đầu = 3,8 + 3,2 = 7g
Ta lại có
n Fe p / u = n S p / u = 0,1 mol
n Fe dư = n H 2 = 0,1 mol
n Fe ban đầu → m Fe ban đầu = 0,2 .56 = 1,12 g
Vậy m = 11,2 + 0,7 = 18,2 (gam)

Chất rắn không tan là Cu chưa pư.
⇒ mCu (dư) = 6 (g)
Ta có: 56nFe + 64nCu (pư) = 30 - 6 (1)
\(n_{HNO_3}=0,52.2=1,04\left(g\right)\Rightarrow n_{NO}=\dfrac{1,04}{4}=0,26\left(mol\right)\)
BT e, có: 2nFe + 2nCu (pư) = 3nNO = 0,78(2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,12\left(mol\right)\\n_{Cu\left(pư\right)}=0,27\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m_{Cu}=\dfrac{0,27.64+6}{30}.100\%=77,6\%\)

Đáp án B
Đặt
![]()
Khối lượng muối khan giảm là do đã xảy ra phản ứng thay thế các nguyên tử halogen trong muối.
Ta có hệ:
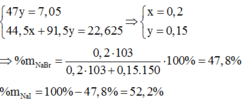
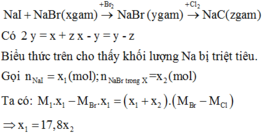
\(n_{H_2SO_4}=1,8\left(mol\right);n_{Ni}=0,16875\left(mol\right)\)
Đặt \(n_{F\text{e}}=x;n_{Cu}=y;n_{c\text{r}}=z\left(mol\right)\)
TN1: Cho Y td H2SO4
Fe3O4 + 8H+ -----> 2Fe3+ + Fe2+ + 4H2O
\(\frac{1}{3}x\)\(_{\rightarrow}\)______\(\frac{8}{3}x\)______\(\frac{2}{3}x\)_____\(\frac{1}{3}x\)
CuO + 2H+ -----> Cu2+ + H2O
y\(_{\rightarrow}\)______2y_______y
Cr2O3 + 6H+ -----> 2Cr3+ + 3H2O
0,5z\(_{\rightarrow}\)____3z________z
\(\Rightarrow n_{H^+}=\frac{8}{3}x+2y+3\text{z}=3,6\left(1\right)\)
TN2: Cho \(\frac{1}{4}\)Z td Ni
Ni + 2Fe3+ -----> Ni2+ + 2Fe2+
\(\frac{1}{12}x\)__\(_{\leftarrow}\frac{1}{6}x\)
Ni + Cu2+ -----> Ni2+ + Cu
\(\frac{y}{4}\)____\(_{\leftarrow}\frac{1}{4}y\)
\(\Rightarrow\frac{1}{12}x+\frac{1}{4}y=0,16875\)
\(\Rightarrow m_{KL}=56\text{x}+64y+52\text{z}=\frac{52}{3}\left(\frac{8}{3}x+2y+3\text{z}\right)+\frac{352}{3}\left(\frac{x}{12}+\frac{y}{4}\right)=82,2\left(g\right)\)
TN3: Cô cạn 3 phần còn lại
mchất rắn \(=\frac{3}{4}\left(m_{KL\left(Z\right)}+m_{SO_4^{2^-}\left(Z\right)}\right)=\frac{3}{4}\left(82,2+96\cdot1,8\right)=191,25\left(g\right)\)
True đấy nhưng về cách trình bày đừng doạ tao bằng ion mày ơi :)) Thu gọn ion thì thu gọn cho trót là O2-+H+ đi còn CuO+H+ :3