Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(\left\{{}\begin{matrix}n_{K+}+3n_{Al^{3+}}=n_{Cl^-}+2n_{SO^{2-}_4}\left(BTe\right)\\39n_{K^+}+27n_{Al^{3+}}+35,5n_{Cl^-}+96n_{SO^{2-}_4}=29,525\left(BTKL\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}0,15+3x=y+2\cdot0,2\\0,15\cdot39+27\cdot x+35,5\cdot y+96\cdot0,2=29,525\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}3x-y=0,25\\27x+35,5y=4,475\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)

Đáp án A
Áp dụng ĐLBT ĐT: Tổng số mol điện tích dương bằng tổng số mol điện tích âm ta có: 0,1.1+ 0,02.1=0,05.2+ nCl-
Suy ra nCl-= 0,02 mol
Khối lượng chất rắn thu được khi cô cạn dung dịch là:
0,1.18+ 0,02.39+ 96.0,05+ 0,02.35,5= 8,09 gam

Đáp án B
Ta thấy dung dịch tồn tại hỗn hợp 2 axit HNO3 và H2SO4
Vì H2SO4 là một axit khó bay hơi
Mặt khác khi cô cạn dung dịch muối cũng không bay hơi
Do đó chất bị bay hơi chỉ có thể là HNO3



Đáp án B
Bảo toàn điện tích: nCl- = 3nAl3+ + 2nCu2+ - 2nSO42- = 0,1
mmuối =mAl3+ + mCu2+ + mSO42- + mCl- = 31,85g
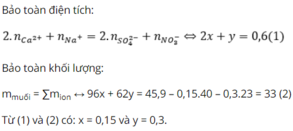

+Theo định luật bảo toàn điện tích:
\(n_{Na^+}+n_{K^+}=2n_{SO_4^-}+n_{NO_3^-}\)
\(\Rightarrow0,9+0,1=2.0,1+x\)
\(\Rightarrow x=0,8\) mol
+ Khối lượng chất rắn thu được khi cô cạn:
\(m_{\text{chất rắn}}=m_{Na^+}+m_{SO_4^{2-}}+m_{K^+}+m_{NO_3^-}\)
\(=23.0,9+96.0,1+39.0,1+62.0,8\)
= 83,8 gam