
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Pt hóa học thì em tự viết nhé vì đơn giản rồi. Thầy tóm tắt sơ đồ thôi.
\(\left\{{}\begin{matrix}C_3H_4O\\C_4H_6O_2\\C_3H_6O_3\end{matrix}\right.\) + O2 (kk) → \(\left\{{}\begin{matrix}CO_2\\H_2O\\N_2\end{matrix}\right.\) \(\underrightarrow{Ca\left(OH\right)_2}\) \(\left\{{}\begin{matrix}Ca\left(HCO_3\right)_2\\CaCO_3\\N_2\end{matrix}\right.\)
Khí duy nhất thoát ra là N2 = 19,264:22,4 = 0,86 mol
=> nO2 = nN2 :4 = 0,215 mol
nCa(OH)2 = 8,75.0,02 = 0,175 mol
nCaCO3 = 15: 100 = 0,15 mol
nCa(OH)2 > nCaCO3 nên có muối Ca(HCO3)2
BTNT Ca => nCa(HCO3)2 = 0,025 mol
Tiếp tục bảo toàn nguyên tố C => nCO2 = 0,2 mol
Gọi số mol H2O là a mol
Số mol C3H4O là x , C4H6O2 là y và C3H6O3 là z mol
Khi đốt cháy C3H6O3 thì số mol CO2 = nH2O
Khi đốt cháy C3H4O và C4H6O2 có dạng CnH2n-2Ox thì số mol CO2 > nH2O
=> nC3H4O + nC4H6O2 = nCO2 - nH2O
Ta được pt: x + y = 0,2 - a (1)
Pt về số mol H2O : 2x + 3y + 3z = a (2)
BTNT O => x + 2y + 3z + 0,215.2 = 0,2.2 + a
<=> x + 2y + 3z = a - 0,03 (3)
Từ (1) vad (3) => 2x + 3y + 3z = 0,17 = nH2O
BTKL => m + 0,215.32 = 0,2.44 + 0,17.18
<=> m = 4,98 gam

a) Trích mẫu thử :
Cho quỳ tím vào 3 mẫu thử :
+ Hóa đỏ : HCl , H2SO4
+ Hóa xanh : KOH
Cho dung dịch BaCl2 vào 2 mẫu thử làm quỳ tím hóa đỏ :
+ Chất nào xuất hiện kết tủa trắng không tan trong axit : H2SO4
Pt : \(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
Không hiện tượng : HCl
Chúc bạn học tốt
c) Trích mẫu thử :
Cho quỳ tím vào từng mẫu thử :
+ Hóa đỏ : HCl , H2SO4
+ không đổi màu : Na2SO4
Cho dung dịch BaCl2 vào 2 mẫu thử làm quỳ tím hóa đỏ :
+ Chất naò xuất hiện kết tủa trắng không tan trong axit : H2SO4
Pt : \(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
Không hiện tượng : HCl
Chúc bạn học tốt

Câu 37:
Ta có: \(n_K=\dfrac{15,6}{39}=0,4\left(mol\right)\)
\(n_{H_2O}=\dfrac{100}{18}=\dfrac{50}{9}\left(mol\right)\)
PT: \(2K+2H_2O\rightarrow2KOH+H_2\)
Xét tỉ lệ: \(\dfrac{0,4}{2}< \dfrac{\dfrac{50}{9}}{2}\), ta được H2O dư.
Theo PT: \(\left\{{}\begin{matrix}n_{KOH}=n_K=0,4\left(mol\right)\\n_{H_2}=\dfrac{1}{2}n_K=0,2\left(mol\right)\end{matrix}\right.\)
Ta có: m dd sau pư = mK + mH2O - mH2 = 15,6 + 100 - 0,2.2 = 115,2 (g)
\(\Rightarrow C\%_{KOH}=\dfrac{0,4.56}{115,2}.100\%\approx19,44\%\)
→ Đáp án: C
Câu 38:
Ta có: \(n_{Fe}=0,1\left(mol\right)\)
\(m_{HCl}=109,5.15\%=16,425\left(g\right)\Rightarrow n_{HCl}=0,45\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,45}{2}\), ta được HCl dư.
a, Theo PT: \(n_{H_2}=n_{Fe}=0,1\left(mol\right)\)
⇒ VH2 = 0,1.22,4 = 2,24 (l)
→ Đáp án: C
b, Theo PT: nFeCl2 = nFe = 0,1 (mol)
Ta có: m dd sau pư = 5,6 + 109,5 - 0,1.2 = 114,9 (g)
\(\Rightarrow C\%_{FeCl_2}=\dfrac{0,1.127}{114,9}.100\%\approx11,05\%\)
→ Đáp án: D
Bạn tham khảo nhé!
37. \(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\)
\(n_K=\dfrac{15,6}{39}=0,4\left(mol\right)\)
mdd sau phản ứng = 15,6+100 - 0,2.2 = 115,2 (g)
=> \(C\%_{KOH}=\dfrac{0,4.56}{115,2}.100=19,44\%\)
=>Chọn C

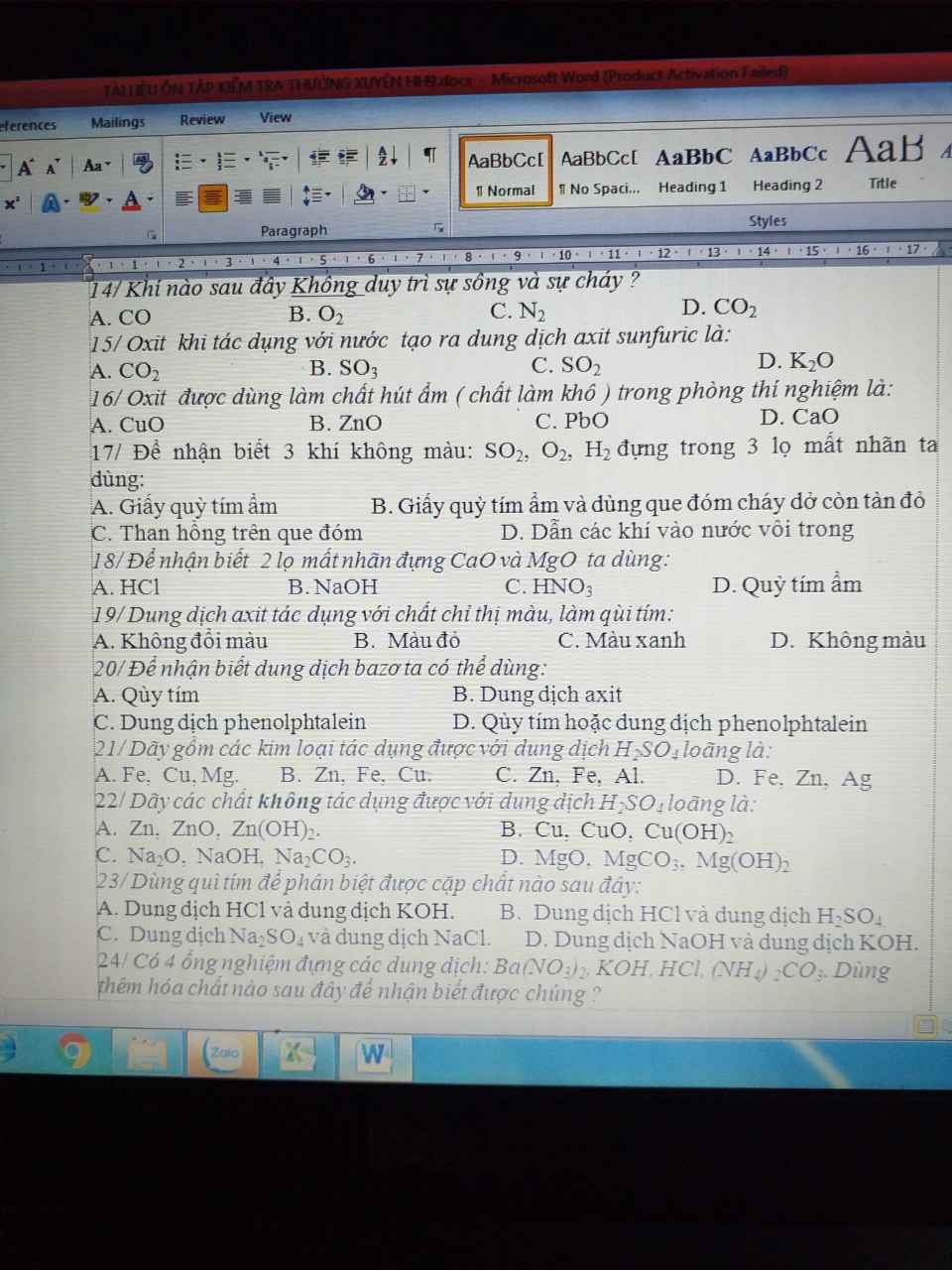






14c
15b
16d
17b
18d
19b
20d
21c
22b
23a