Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Na_2CO_3}=n_{Na_2CO_3\cdot10H_2O}=\dfrac{57.2}{106+18\cdot10}=0.2\left(mol\right)\)
\(C_{M_{Na_2CO_3}}=\dfrac{0.2}{0.4}=0.5\left(M\right)\)
\(m_{Na_2CO_3}=0.2\cdot106=21.2\left(g\right)\)
\(m_{dd}=400\cdot1.05=420\left(g\right)\)
\(C\%_{Na_2CO_3}=\dfrac{21.2}{420}\cdot100\%=5.04\%\)

\(n_{Na_2CO_3}=\dfrac{10,6}{106}=0,1\left(mol\right)\\ \rightarrow C_{M\left(Na_2CO_3\right)}=\dfrac{0,1}{0,2}=0,5M\)
Ta có: \(C\%=\dfrac{C_M.M}{10.D}\)
\(\rightarrow C\%=\dfrac{0,5.106}{10.1,05}=5,05\%\)

\(C\%=\dfrac{30}{170}.100\%=17,647\%\)
\(V_{\text{dd}}=\left(30+170\right)1,1=220ml\)
\(n_{NaCl}=\dfrac{30}{58,5}=0,513mol\)
\(C_M=\dfrac{0,513}{0,22}=0,696M\)
\(C\%_{NaCl}=\dfrac{30}{170+30}.100\%=15\%\\ C_M=C\%.\dfrac{10D}{M}=10.\dfrac{10.1,1}{58,5}=1,88M\)

Ta có: \(m_{dd}=300\cdot1,05=315\left(g\right)\) \(\Rightarrow C\%_{Na_2CO_3}=\dfrac{15,9}{315}\cdot100\%\approx5,05\%\)
Mặt khác: \(n_{Na_2CO_3}=\dfrac{15,9}{106}=0,15\left(mol\right)\) \(\Rightarrow C_{M_{Na_2CO_3}}=\dfrac{0,15}{0,3}=0,5\left(M\right)\)

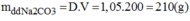
Nồng độ phần trăm của dung dịch pha chế:
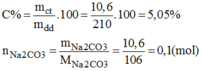
Nồng độ mol của dung dịch:
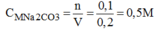

\(n_{Na_2CO_3}=\dfrac{21,2}{106}=0,2\left(mol\right)\)
=> \(C_M=\dfrac{0,2}{0,3}=0,667M\)
\(m_{dd}=300.1,05=315\left(g\right)\)
=> \(C\%=\dfrac{21,2}{315}.100\%=6,73\%\)

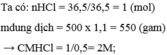

\(n_{Na_2CO_3.10H_2O}=\frac{143}{286}=0,5\left(mol\right)\)
Ta có: \(n_{Na_2CO_3}=n_{Na_2CO_3.10H_2O}=0,5\left(mol\right)\)
\(\Rightarrow m_{Na_2CO_3}=0,5\times106=53\left(g\right)\)
\(m_{H_2O}=200\times1=200\left(g\right)\)
\(m_{ddNa_2CO_3}mới=143+200=343\left(g\right)\)
\(C\%_{Na_2CO_3}mới=\frac{53}{343}\times100\%=15,45\%\)
\(C_{M_{Na_2CO_3}}mới=\frac{0,5}{0,2}=2,5\left(M\right)\)
\(D_{ddNa_2CO_3}mới=\frac{343}{200}=1,715\) (g/ml)
Ta có : \(n_{Na_2CO_3}_{.10H_2O}=n_{Na_2CO_3}=\frac{143}{286}=0,5mol\)
\(\Rightarrow m_{Na_2O_3}=0,5.106=53g\)
Khối lượng dung dịch thu được là 143 + 200 = 343 g
Vậy \(C\%=\frac{53}{343}.100\%=15,45\%\)
Khối lượng nước trong muối giải phóng khi hòa tan là :
\(5.18=90g=90ml\)
Tổng thể tích nước trong dung dịch thu được là :
200 + 90 = 290 ml
\(\Rightarrow V_{dd}=V_{H_2O}=290ml=0,29l\)
Vậy \(C_M=\frac{0,5}{0,29}=1,72mol/l\)
Áp dụng công thức \(C\%=\frac{C_M.M}{10.D}\Leftrightarrow D=\frac{C_M.M}{C\%.10}=\frac{1,72.106}{15,45.10}=1,18g/ml\)
Ko chắc đúng đâu nhé