Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nHCl=0.4x0.15=0.06mol => nH+=0.06mol
nNAOH=0.1x0.1=0.01mol =>nOH=0.01mol
Suy ra nH+ dư=0.06-0.01(phản ứng với OH)=0.05mol
Dung dịch sau phản ứng có [H+]=0.05/0.5=0.1M
pH=1
==>pH=-log(0.1)=1
\(n_{H^+}=0,4.0,15=0,06\left(mol\right);n_{OH^-}=0,1.0,1=0,01\left(mol\right)\)
PT ion rút gọn: \(H^++OH^-\rightarrow H_2O\)
0,01<---0,01
=> \(n_{H^+\left(d\text{ư}\right)}=0,06-0,01=0,05\left(mol\right)\)
=> \(\left[H^+\right]=\dfrac{0,05}{0,5}=0,1M\)
=> \(pH=-\log\left(0,1\right)=1\)
=> x = 1
Hình như đáp án bị sai?

Đáp án B
nOH- = 0,1.2.0,1 + 0,1.0,1 = 0,03
nH+ = 0,4.2.0,0375 + 0,4.0,0125 = 0,035
⇒ Trong X có H+ dư
⇒ nH+/X =0,035 – 0,03 = 0,005; VX = 100 + 400 = 500ml
⇒ [H+] = 0,01 ⇒ pH = 2.

Nhận thấy khi lượng NaOH tăng lên, lượng AlCl3 không đổi thì lượng kết tủa tăng lên → thí nghiệm 1 thì NaOH hết, AlCl3 còn dư ; thí nghiệm 2 cả NaOH và AlCl3 đều hết (xảy ra hiện tượng hòa tan kết tủa)
Thí nghiệm 1: Ta có 3× nkết tủa = nOH- = 0,6 mol → 0,2a= 0,6 → a= 3
Thí nghiệm 2:Ta có 4×nAl3+ = nOH- + nkết tủa → 4×0,5b= 0,4×3 + 0,3 → b= 0,75
Đáp án A

`100mL=0,1L`
`n_{H^+}=0,1.0,05.2+0,1.0,1=0,02(mol)`
`n_{SO_4^{2-}}=0,1.0,05=0,005(mol)`
`n_{OH^-}=0,1.0,2+0,1.0,1.2=0,04(mol)`
`n_{Ba^{2+}}=0,1.0,1=0,01(mol)`
`Ba^{2+}+SO_4^{2-}->BaSO_4`
Do `0,01>0,005->` Tính theo `SO_4^{2-}`
`n_{BaSO_4}=n_{SO_4^{2-}}=0,005(mol)`
`->m_↓=0,005.233=1,165(g)`
`H^{+}+OH^{-}->H_2O`
Do `0,02<0,04->OH^-` dư
`n_{OH^{-}\ pu}=n_{H^+}=0,02(mol)`
`->n_{OH^{-}\ du}=0,04-0,02=0,02(mol)`
Trong X: `[OH^-]={0,02}/{0,1+0,1}=0,1M`
`->pH=14-pOH=14+lg[OH^-]=13`

• 0,1 mol HCl + 0,02 mol Al2(SO4)3 → ddX
ddX + 0,125 mol Ba(OH)2 → ↓
• 2HCl + Ba(OH)2 → BaCl2 + 2H2O (*)
Al2(SO4)3 + 3Ba(OH)2 → 2Al(OH)3↓ + 3BaSO4↓ (**)
2Al(OH)3 + Ba(OH)2 → Ba(AlO2)2 + 4H2O (***)
Theo (*) nBa(OH)2 = 0,1 : 2 = 0,05 mol.
Theo (**) nBa(OH)2 = 0,02 × 3 = 0,06 mol; nAl(OH)3 = 0,04 mol; nBaSO4 = 0,06 mol.
Theo (***) nBa(OH)2 = 0,125 - 0,05 - 0,06 = 0,015 mol → nAl(OH)3 = 0,04 - 0,015 × 2 = 0,01 mol.
→ m↓ = mBaSO4 + mAl(OH)3 = 0,06 × 233 + 0,01 × 78 = 14,76 gam
→ Đáp án đúng là đáp án C

a, \(n_{Ba\left(OH\right)_2}=0,1.0,1=0,01\left(mol\right)=n_{Ba^{2+}}\)
\(\Rightarrow n_{OH^-}=2n_{Ba\left(OH\right)_2}=0,02\left(mol\right)\)
\(n_{NaOH}=0,1.0,1=0,01\left(mol\right)=n_{Na^+}=n_{OH^-}\)
⇒ ΣnOH- = 0,02 + 0,01 = 0,03 (mol)
\(n_{H_2SO_4}=0,4.0,0175=0,007\left(mol\right)=n_{SO_4^{2-}}\)
\(\Rightarrow n_{H^+}=2n_{H_2SO_4}=0,014\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
0,014___0,014 (mol) ⇒ nOH- dư = 0,03 - 0,014 = 0,016 (mol)
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\)
0,007____0,007_____0,007 (mol) ⇒ nBa2+ dư = 0,01 - 0,007 = 0,003 (mol)
⇒ m = 0,007.233 = 1,631 (g)
\(\left[OH^-\right]=\dfrac{0,016}{0,1+0,4}=0,032\left(M\right)\)
\(\left[Ba^{2+}\right]=\dfrac{0,003}{0,1+0,4}=0,006\left(M\right)\)
\(\left[Na^+\right]=\dfrac{0,01}{0,1+0,4}=0,02\left(M\right)\)
b, pH = 14 - (-log[OH-]) ≃ 12,505
\(n_{Ba^{2+}}=0,1.0,1=0,01\left(mol\right)\)
\(n_{SO_4^{2-}}=0,4.0,0175=7.10 ^{-3}\left(mol\right)\)
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\downarrow\)
\(\Rightarrow m=m_{BaSO_4}=7.10^{-3}.233=1,631\left(g\right)\)
Ta có:
\(n_{H^+}=0,4.0,0175.2=0,014\left(mol\right)\)
\(n_{OH^-}=0,1.0,1.2+0,1.0,1=0,03\left(mol\right)\)
Trong dung dịch X:
\(n_{OH^-}=0,03-0,014=0,016\left(mol\right)\)\(\Rightarrow\left[OH^-\right]=\dfrac{0,016}{0,1+0,4}=0,032\left(M\right)\)
\(n_{Ba^{2+}}=0,01-7.10^{-3}=3.10^{-3}\left(mol\right)\Rightarrow\left[Ba^{2+}\right]=\dfrac{3.10^{-3}}{0,1+0,4}=6.10^{-3}\left(M\right)\)
\(n_{Na^+}=0,1.0,1=0,01\left(mol\right)\Rightarrow\left[Na^+\right]=0,02\)
\(pOH=-lg\left(0,032\right)\approx1,5\Rightarrow pH=14-1,5=12,5\)

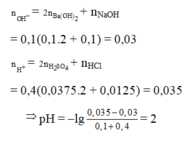
Gọi lượng Al(OH)3 kết tủa là x mol
Trong 36 gam: n N a O H = 3 x
Suy ra, số mol NaOH trong 148 gam:
n N a O H = 148 . 3 x 36 = 37 . 3 x 9 ⇒ n A l ( O H ) 4 = 0 , 04 - x ⇒ 37 . 3 x 9 = 3 x + 4 ( 0 , 04 - x ) ⇒ x = 0 , 012 ⇒ C = 0 , 012 . 3 . 40 36 = 4 %
Đáp án D