Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
F e 2 S O 4 3 0 , 1 m o l F e S O 4 0 , 1 m o l C u S O 4 0 , 1 m o l + H 2 S → m g a m S C u S
nCuS = 0,1 mol; Theo bảo toàn electron: 2 × nS = 1 × nFe3+
→ nS = 0,1 × 2 : 2 = 0,1 mol.
→ m↓ = mS + mCuS = 0,1 × 32 + 0,1 × 96 = 12,8 gam

Đáp án A.
nAl(OH)3= 7 , 8 78 = 0 , 1
2NaOH + H2SO4 à Na2SO4 + 2H2O (1)
0,2 ß 0,1
Để NaOH phản ứng nhiều nhất thu được 0,1 mol kết tủa Al(OH)3 thì Al2(SO4)3 phải phản ứng hết tạo kết tủa tối đa, sau đó kết tủa tan một phần sao cho lượng kết tủa cuối cùng thu được bằng 0,1 mol.
6NaOH + Al2(SO4)3 à 3Na2SO4 + 2Al(OH)3 (2)
0,6 ß 0,1 à 0,2
NaOH + Al(OH)3 à NaAlO2 + 2H2O (3)
0,1 ß 0,1
Từ (1), (2) và (3) ta có:
nNaOH pư = 0,6 + 0,1 + 0,2 = 0,9 mol
è → Vdd NaOH = 0,9 : 2 = 0,45 M

Đáp án D
V có giá trị lớn nhất vậy có các phương trình

Vậy nNaOH = 0,9 ⇒ V = 0,45

Chọn đáp án C
● Gọi số mol NaOH dùng ở lần 1 là a mol ta có sơ đồ.
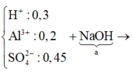
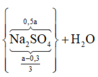
● ⇒ Với nNaOH = (a + 0,45) mol thì nAl(OH)3 = a - 0 , 3 6
+ Ta có sơ đồ:

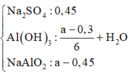
⇒ Ta có nAl(OH)3 = 4nAl(OH)3 – (nNaOH – nH+)
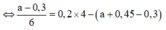
a = 0,6 mol ⇒ VNaOH = 0,6 lít = 600 ml ⇒ Chọn C

Đáp án C
nOH- = 1,5.0,5 = 0,75 mol
nAl3+ = 0,2 mol
nAl(OH)3 = 4nAl3+ - nNaOH = 4.0,2 – 0,75 = 0,05 mol
=>mAl(OH)3 = 0,05.78 = 3,9 gam

Giải thích:
nOH- = 1,5.0,5 = 0,75 mol
nAl3+ = 0,2 mol
nAl(OH)3 = 4nAl3+ - nNaOH = 4.0,2 – 0,75 = 0,05 mol
=>mAl(OH)3 = 0,05.78 = 3,9 gam
Đáp án C

Đáp án C
nOH- = 1,5.0,5 = 0,75 mol
nAl3+ = 0,2 mol
nAl(OH)3 = 4nAl3+ - nNaOH = 4.0,2 – 0,75 = 0,05 mol
=>mAl(OH)3 = 0,05.78 = 3,9 gam
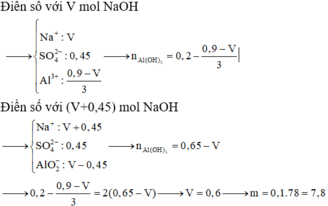
Đáp án :C