Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(n_{MgO}=\dfrac{4}{40}=0,1\left(mol\right)\)
\(n_{HCl}=4.100:1000=0,4\left(mol\right)\)
a. PTHH: MgO + 2HCl ---> MgCl2 + H2O
Ta thấy: \(\dfrac{0,1}{1}< \dfrac{0,4}{2}\)
Vậy HCl dư.
=> \(n_{dư}=\dfrac{0,1.2}{0,4}=0,5\left(mol\right)\)
=> \(m_{dư}=0,5.36,5=18,2\left(g\right)\)
b. Ta có: \(V_{dd_{MgCl_2}}=V_{HCl}=\dfrac{100}{1000}=0,1\left(lít\right)\)
Theo PT: \(n_{MgCl_2}=n_{MgO}=0,1\left(mol\right)\)
=> \(C_{M_{MgCl_2}}=\dfrac{0,1}{0,1}=1M\)

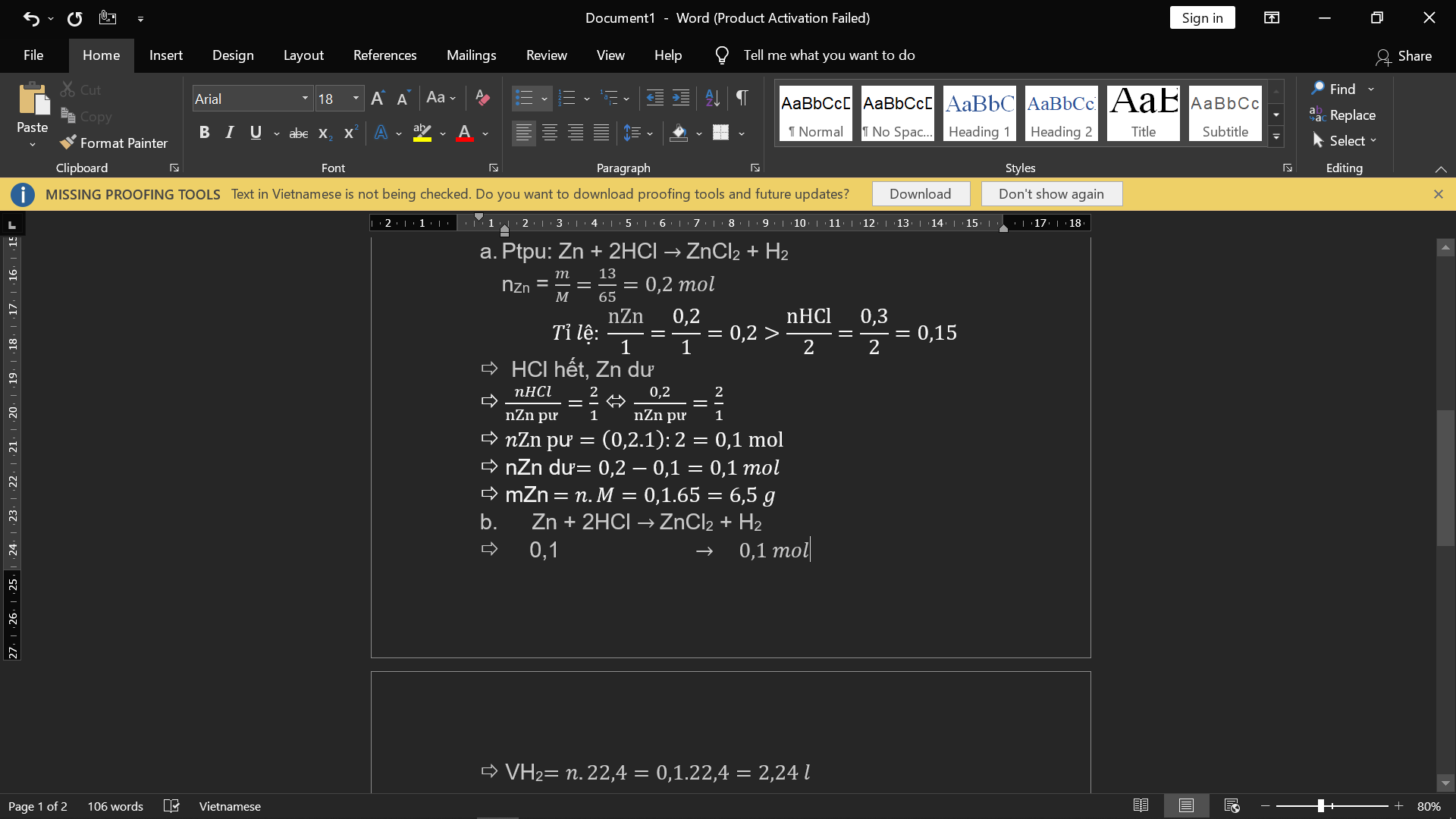
\(a,PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ b,n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ n_{HCl}=2\cdot0,15=0,3\left(mol\right)\)
Vì \(\dfrac{n_{Zn}}{1}>\dfrac{n_{HCl}}{2}\) nên sau p/ứ Zn dư
\(\Rightarrow n_{Zn}=\dfrac{1}{2}n_{HCl}=0,15\left(mol\right)\\ \Rightarrow m_{Zn}=0,15\cdot65=9,75\\ \Rightarrow m_{Zn\left(dư\right)}=13-9,75=3,25\left(g\right)\\ c,n_{H_2}=n_{Zn}=0,15\left(mol\right)\\ \Rightarrow V_{H_2}=0,15\cdot22,4=3,36\left(l\right)\)

\(n_{Zn}=\dfrac{9,75}{65}=0,15\left(mol\right)\)
\(n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2|\)
1 2 1 1
0,15 0,4 0,15
a) Lập tỉ số so sánh : \(\dfrac{0,15}{1}< \dfrac{0,4}{2}\)
⇒ Zn phản ứng hết , HCl dư
⇒ Tinsht toán dựa vào số mol của zn
\(n_{HCl\left(dư\right)}=0,4-\left(0,15.2\right)=0,1\left(mol\right)\)
⇒ \(m_{HCl\left(dư\right)}=0,1.36,5=3,65\left(g\right)\)
b) \(n_{H2}=\dfrac{0,15.1}{1}=01,5\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,15.24,79=3,1875\left(l\right)\)
Chúc bạn học tốt

PTHH: \(Fe_3O_4+8HCl\rightarrow FeCl_2+2FeCl_3+4H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\\n_{HCl}=\dfrac{300\cdot3,65\%}{36,5}=0,3\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,3}{8}\) \(\Rightarrow\) Fe3O4 còn dư, HCl p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe_3O_4\left(dư\right)}=0,0625\left(mol\right)\\n_{FeCl_2}=0,0375\left(mol\right)\\m_{FeCl_3}=0,075\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe_3O_4\left(dư\right)}=0,0625\cdot232=14,5\left(g\right)\\m_{muối}=0,0375\cdot127+0,075\cdot162,5=16,95\left(g\right)\end{matrix}\right.\)
nFe3O4= 23,2/232=0,1(mol); nHCl = (300.3,65%)/36,5= 0,3(mol)
a) PTHH: Fe3O4 + 8 HCl -> 2 FeCl3 + FeCl2 + 4 H2O
b) Ta có: 0,3/8 < 0,1/1
=> Fe3O4 dư, HCl hết, tính theo nHCl.
=> nFe3O4(p.ứ)= nFeCl2= nHCl/8=0,3/8= 0,0375(mol)
=> mFe3O4(dư)= (0,1- 0,0375).232=14,5(g)
c) nFeCl3= 2/8. 0,3= 0,075(mol)
=> mFeCl3= 0,075.162,5=12,1875(g)
mFeCl2= 0,0375. 127=4,7625(g)
=>m(muối)= 12,1875+ 4,7625= 16,95(g)

\(n_{Al_2O_3}=\dfrac{30,6}{102}=0,3(mol)\\ n_{HCl}=\dfrac{100.21,9}{100.36,5}=0,6(mol)\\ a,PTHH:Al_2O_3+6HCl\to 2AlCl_3+3H_2O\)
\(b,\)Vì \(\dfrac{n_{Al_2O_3}}{1}>\dfrac{n_{HCl}}{6}\) nên \(Al_2O_3\) dư
\(n_{Al_2O_3(dư)}=0,3-\dfrac{1}{6}.0,6=0,2(mol)\\ \Rightarrow m_{Al_2O_3(dư)}=0,2.102=20,4(g)\\ c,n_{AlCl_3}=\dfrac{1}{3}.0,6=0,2(mol)\\ \Rightarrow C\%_{AlCl_3}=\dfrac{0,2.133,5}{100+30,6}.100\%=20,44\%\\ C\%_{Al_2O_3(dư)}=\dfrac{20,4}{100+30,6}.100\%=15,62\%\)

Bài 1:
a) nP=6,2/31=0,2(mol); nO2= 6,72/22,4=0,3(mol)
PTHH: 4P + 5 O2 -to-> 2 P2O5
Ta có: 0,2/4 < 0,3/5
=> P hết, O2 dư, tính theo nP
=> nO2(p.ứ)= 5/4. nP= 5/4. 0,2=0,25(mol)
=> mO2(dư)=0,3- 0,25=0,05(mol)
=> mO2(dư)=0,05.32=1,6(g)
b) nP2O5= nP/2= 0,2/2=0,1(mol)
=>mP2O5=0,1.142=14,2(g)

\(300(ml)=0,3(l)\\ n_{HCl}=1.0,3=0,3(mol);n_{Fe}=\dfrac{5,6}{56}=0,1(mol)\\ a,PTHH:Fe+2HCl\to FeCl_2+H_2\\ \text{LTL: }\dfrac{n_{Fe}}{1}<\dfrac{n_{HCl}}{2}\Rightarrow HCl\text{ dư}\\ \Rightarrow n_{HCl(dư)}=0,3-0,1.2=0,1(mol)\\ \Rightarrow m_{HCl(dư)}=0,1.36,5=3,65(g)\\ b,n_{FeCl_2}=n_{Fe}=0,1(mol)\\ \Rightarrow \begin{cases} C_{M_{FeCl_2}}=\dfrac{0,1}{0,3}=0,33M\\ C_{M_{HCl(dư)}}=\dfrac{0,1}{0,3}=0,33M \end{cases}\)

PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\\n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Fe còn dư
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2}=0,25\left(mol\right)\\n_{Fe\left(dư\right)}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,25\cdot22,4=5,6\left(l\right)\\m_{Fe\left(dư\right)}=0,15\cdot56=8,4\left(g\right)\end{matrix}\right.\)
Số mol của sắt
nFe = \(\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
Số mol của axit sunfuric
nH2SO4 = \(\dfrac{m_{H2SO4}}{M_{H2SO4}}=\dfrac{24,5}{98}=0,25\left(mol\right)\)
Pt : Fe + H2SO4 → FeSO4 + H2\(|\)
1 1 1 1
0,4 0,25 0,25
a) Lập tỉ số so sánh : \(\dfrac{0,4}{1}>\dfrac{0,25}{1}\)
⇒ Fe dư , H2SO4 phản ứng hết
⇒ Tính toán dựa vào số mol của H2SO4
Số mol của khí hidro
nH2 = \(\dfrac{0,25.1}{1}=0,25\left(mol\right)\)
Thể tích của khí hidro
VH2 = nH2 . 22,4
= 0,25 . 22,4
= 5,6 (l)
b) Số mol dư của sắt
ndư = nban đầu - nmol
= 0,4 -(0,25 . 1)
= 0,15 (mol)
Khối lượng dư của sắt
mdư = ndư . MFe
= 0,15 . 56
= 8,4 (g)
Chúc bạn học tốt

Vì đồng không tác dụng với HCl loãng :
1) Chất rắn không tan là đồng nên :
\(m_{Al}=11,8-6,4=5,4\left(g\right)\)
\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
Pt : \(2Al+6HCl\rightarrow2AlCl_3+3H_2|\)
2 6 2 3
0,2 0,3
\(n_{H2}=\dfrac{0,2.3}{2}=0,3\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,3.22,4=6,72\left(l\right)\)
2) Có : \(m_{Cu}=6,4\left(g\right)\)
\(n_{Cu}=\dfrac{6,4}{64}=0,1\left(mol\right)\)
Pt : \(2Al+6H_2SO_{4đặc}\underrightarrow{t^o}Al_2\left(SO_4\right)_3+3SO_2+6H_2O|\)
2 6 1 3 6
0,2 0,3
\(Cu+2H_2SO_{4đặc}\underrightarrow{t^o}CuSO_4+SO_2+2H_2O|\)
1 2 1 1 2
0,1 0,1
\(n_{SO2\left(tổng\right)}=0,3+0,1=0,4\left(mol\right)\)
\(V_{SO2\left(dktc\right)}=0,4.22,4=8,96\left(l\right)\)
Chúc bạn học tốt
\(n_{Al}=\dfrac{081}{27}=0.03\left(mol\right)\)
\(n_{HCl}=\dfrac{2.19}{36.5}=0.06\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(2.........6\)
\(0.03.......0.06\)
\(LTL:\dfrac{0.03}{2}>\dfrac{0.06}{6}\Rightarrow Aldư\)
\(m_{Al\left(dư\right)}=\left(0.03-0.02\right)\cdot27=0.27\left(g\right)\)
\(m_{AlCl_3}=0.02\cdot133.5=2.67\left(g\right)\)
\(m_{H_2}=0.03\cdot2=0.06\left(g\right)\)
a, Ta có: \(n_{Al}=\dfrac{0,81}{27}=0,03\left(mol\right)\)
\(n_{HCl}=\dfrac{2,19}{36,5}=0,06\left(mol\right)\)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Xét tỉ lệ: \(\dfrac{0,03}{2}>\dfrac{0,06}{6}\), ta được Al dư.
Theo PT: \(n_{Al\left(pư\right)}=\dfrac{1}{3}n_{HCl}=0,02\left(mol\right)\)
\(\Rightarrow n_{Al\left(dư\right)}=0,01\left(mol\right)\)
\(\Rightarrow m_{Al\left(dư\right)}=0,01.27=0,27\left(g\right)\)
b, Theo PT: \(\left\{{}\begin{matrix}n_{AlCl_3}=\dfrac{1}{3}n_{HCl}=0,02\left(mol\right)\\n_{H_2}=\dfrac{1}{2}n_{HCl}=0,03\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{AlCl_3}=0,02.133,5=2,67\left(g\right)\)
\(m_{H_2}=0,03.2=0,06\left(g\right)\)
mAl (dư) = 0,27 (g)
Bạn tham khảo nhé!