Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cái chỗ M đó suy ra là \(M_X< 83,13< M_Y\)
Thì có 2 chất liên tiếp là Br (80) và I (127)

Nếu AgX và AgY đều kết tủa thì ta có:
NaX + AgNO3 -> AgX ↓ + NaNO3 (1)
a...........................a (mol)
NaY + AgNO3 -> AgY ↓ + NaNO3 (2)
Ta có hệ pt: \(\left\{{}\begin{matrix}\left(23+X\right)a+\left(23+Y\right)b=31,84\left(I\right)\\\left(108+X\right)a+\left(108+Y\right)=57,34\left(II\right)\end{matrix}\right.\)
Giải hệ pt ta đc: a + b = 0,3 (III)
Từ (I) => aX + bY = 24,94 (IV)
Gọi \(\overline{X}\) là khối lượng nguyên tử trung bình của X, Y, ta có:
\(\overline{X}\)=\(\dfrac{m_{hh}}{n_{hh}}=\dfrac{24,94}{0,3}=83,13\)
Vì X < \(\overline{X}\) < Y => X < 83,13 < Y
X = 80 < 83,13 nên X là brom và Y = 127 > 83,13 nên Y là iot
Vậy công thức của hai muối là NaBr và NaI
Đặt công thức hóa học 2 muối là NaZ.
Trong đó X<Z<Y
PHƯƠNG TRÌNH LÀ:
NaZ+AgNO3===>NaNO3+AgZ
Theo bài:
31,84/( 23+Z)=57,34/(108+Z)
Giải pt ta được Z=83,3333
Vì X,Y 2 chu kì liên tiếp=> X=Br Y=I.

NaX + AgNO 3 → NaNO 3 + AgX
a mol a mol a mol a mol
NaY + AgNO 3 → NaNO 3 + AgY
b mol b moi b mol b mol
n AgNO 3 = 0,2 x 150/1000 = 0,O3 mol
m AgNO 3 = 0,3 x 170 = 5,1g
n NaNO 3 = 0,O3 => m NaNO 3 = 0,03 x 85 = 2,55g
Áp dụng định luật bảo toàn khối lượng, ta có :
2,2 + 5,1 = 2,55 + m kết tủa → m kết tủa = 4,75 (gam)
(108 + X)a + (108 + Y)b = 4,75 ; a + b = 0,O3 (mol)
Xa + Yb + 15,1. Cho X > Y ; Xa + Xb > Xa + Yb > Ya + Yb
X > 1,51/0,03 > Y > X > 50,3 > Y
X và Y là các halogen liên tiếp, vậy đó là brom (80) và Cl (35,5).

Gọi công thức chung của 2 kim loại là X
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: X + 2H2O --> X(OH)2 + H2
0,3<-------------------0,3
=> \(M_X=\dfrac{8,8}{0,3}=29,33\left(g/mol\right)\)
Mà 2 kim loại thuộc 2 chu kì liên tiếp nhóm IIA
=> 2 kim loại là Mg(Magie) và Ca(Canxi)

Theo đlbtklg ta có:
mX=8,04-2,72=5,32(g)
nX=5,32/X(mol)
Theo đlbtntố ta có:
nAgX=nX=5,32/X(mol)
Ta có:
5,32/X(108+X)=21,525
X=35,5(g/mol)
X là Cl
K hiểu j cứ hỏi lại nha

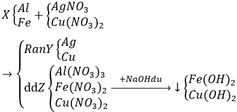
Pt:
Al + 3AgNO3 → Al(NO3)3 + 3Ag↓
2Al + 3Cu(NO3)2 → 2Al(NO3)2 + 3Cu↓
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag↓
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu↓
Al(NO3)3 + 3NaOH → Al(OH)3↓ + 3NaNO3
Al(OH)3 + NaOH → NaAlO2 + 2H2O
Fe(NO3)2 + 2NaOH → Fe(OH)2↓ + 2NaNO3
Cu(NO3)2 + 2NaOH → Cu(OH)2↓ + 2NaNO3

Để dễ tính ta chia đôi lun tổng hỗn hợp : là \(\frac{5,33}{2}\)=2,665g ,
Xét phần 2: kết tủa chắc chắn chỉ có BaSO4 :0.005mol.→mol BaCl2: 0,005mol →mol(Cl-):0.005\(\times2=0,01\)
Xét p1 : mol AgNo3: 0,05mol mà mol(AgCl)↓=0,04 →2 muối hết ,Ag dư →bảo toàn ng tố Cl→mol(Cl-trong RCln)=0,04-0,01=0,03mol
m(BAcl2)=0,005\(\times208=1,04\) →m(RCln)=2,665-1,04=1,625g ,
Đặt mol RCLn :x mol →x\(\times n=0,03\)→x=\(\frac{0,03}{n}\) Ta có M(RCln)\(\times\frac{0,03}{n}\)=1,625 →Giải ra đk : R=\(\frac{56}{3}\)n → n=3,R=56 tm
Cthh : FeCl3

PTHH:
BaCl2 + 2AGNO3 2AgCl + Ba(NO3)2
x 2x
CaCl2 + 2AGNO3 2AgCl + Ca(NO3)2
y 2y
Gọi x,y lần lượt là số mol của BaCl2 và CaCl2
Ta có n_AgCl \(=\frac{86,1}{143,5}=0,6\left(mol\right)\)
Lập hệ pt: 208x + 111y = 43 (*)
2x + 2y = 0,6 (**)
Giải hệ ta có : x = 0,1 mol , y = 0,2 mol
=> m_BaCl2 = 0,1 . 208 = 20,8 (g)
=> m_CaCl2 = 0,2 . 111 = 22,2 (g)
=> %BaCl2 = 20,8 . 100 : 43 = 48,37%
=> %CaCl2 = 22,2.100 : 43 = 51,63%
Gọi x,y lần lượt là số mol của BaCl2 và CaCl2
n AgCl= 86,1/143,5=0,6(mol)
BaCl2 + 2AgNO3 ----> Ba(NO3)2 +2AgCl
x 2x
CaCl2 + 2AgNO3 ----> Ca(NO3)2 + 2AgCl
y 2y
208x+ 111y=43
ta có hệ phương trình
2x + 2y= 06
giải hệ phương trình ta được x= 0,1 , y=0,2
%m BaCl2 = ((0,1 . 208) / 43) . 100=48.37%
%m CaCl2 = 100% - 48,37% = 51,63 %


(Bài này giải như bình thường thôi. Nhưng lưu ý với bạn là nếu có 1 muối là NaF thì muối này ko tạo kết tủa với AgNO3 đâu)
* Trường hợp 1: Ko có muối NaF
Gọi công thức tổng quát chung hai muối là: NaX.
Phương trình hoá học viết được:
NaX + AgNO3 = AgX + NaNO3
(23+X) (108+X) (g)
31,84 57,34
=> X=83,13 => Hai halogen là: Bx và I.
* Trường hợp 2: ! trong hai muối là NaF (giả sử là NaX)
Lúc đó chỉ có NaY phản ứng (chỉ có 3 khả năng: Cl, Br hoặc I thôi nên thử từng khả năng cũng được) => đáp án: Cl
Vậy 2 muối là NaF và NaCl hoặc NaBr và NaI.