Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2.
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{m_{H_2SO_4}}{200}.100\%=14,7\%\)
=> \(m_{H_2SO_4}=29,4\left(g\right)\)
=> \(n_{H_2SO_4}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}.n_{H_2SO_4}=\dfrac{1}{3}.0,3=0,1\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=0,1.342=34,2\left(g\right)\)

\(CaCl_2+Na_2SO_4\rightarrow CaSO_4+2NaCl\)
\(n_{CaCl_2}=\dfrac{22,2}{111}=0,2\left(mol\right)\)
a) Đề sai
b) \(m_{ddNa_2SO_4}=200.1,55=310\left(g\right)\)
CaSO4 ít tan, coi như không tan, là kết tủa
\(m_{CaSO_4}=0,2.136=27,2\left(g\right)\)
Muối sau phản ứng là NaCl
\(m_{ddsaupu}=22,2+310-27,2=305\left(g\right)\)
\(C\%_{NaCl}=\dfrac{0,2.2.58,5}{305}.100=7,67\%\)

Khối lượng riêng \(d=\frac{m}{V}\Rightarrow m=dV\Rightarrow m_{ddNa_2SO_4}=1,55.200=310\left(g\right)\) (*)
\(\begin{cases}m_{CaCl2}=41,6\left(g\right);M_{CaCl2}=111\\mol_{CaCl2}.n_{CaCl2}=\frac{n}{M}=\frac{22,2}{111}=0,2\left(mol\right)\end{cases}\)
Phương trinh:
\(CaCl2+Na_2SO_4\rightarrow CaSO_4\downarrow+2NaCl\)
\(0,02mol\) \(\rightarrow0,02mol\rightarrow0,04mol\)
\(\begin{cases}n_{NaCl}=0,4\left(mol\right);M_{NaCl}=58,5\\m_{CaCl}=m_{dd}=nM=23,4\left(g\right)\end{cases}\) (**)
\(\Rightarrow m_{dd}=m_{ddN\text{à}S\text{\text{O4 } }}+m_{CaCl2}-m_{CaS\text{O4}}\)
Giải hệ thu được: \(m_{CaS\text{O4}}=27,2\left(g\right)\)
Thay (*) (**) (***) \(\Rightarrow m_{dd}=324,4\left(g\right)\)
Vậy nồng độ là" \(7,21\%\)

Sửa: \(14,7\%\)
\(n_{H_2SO_4}=\dfrac{200.14,7\%}{100\%.98}=0,3(mol)\\ a,PTHH:2Al+3H_2SO_4\to Al_2(SO_4)_3+3H_2\\ \Rightarrow n_{H_2}=0,3(mol)\\ \Rightarrow V_{H_2}=0,3.22,4=6,72(l)\\ b,n_{Al}=\dfrac{2}{3}n_{H_2SO_4}=0,2(mol)\\ \Rightarrow m_{Al}=0,2.27=5,4(g)\\ c,n_{Al_2(SO_4)_3}=\dfrac{1}{2}n_{Al}=0,1(mol)\\ \Rightarrow C\%_{Al_2(SO_4)_3}=\dfrac{0,1.342}{200+5,4-0,3.2}.100\%=16,7\%\\ c,m_{Al_2(SO_4)_3}=0,1.342=34,2(g)\)

Giả sử có 1 mol Fe tác dụng
PTHH: 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
1---->3----------->0,5------->1,5
Giả sử khối lượng dd H2SO4 78,4% là m (gam)
=> \(m_{H_2SO_4\left(bđ\right)}=\dfrac{m.78,4}{100}=0,784m\left(g\right)\)
=> \(m_{H_2SO_4\left(dư\right)}=0,784m-3.98=0,784m-294\left(g\right)\)
mdd sau pư = 1.56 + m - 1,5.64 = m - 40 (g)
Do C% của Fe2(SO4)3 và H2SO4 dư là bằng nhau
=> \(m_{Fe_2\left(SO_4\right)_3}=m_{H_2SO_4\left(dư\right)}\)
=> 400.0,5 = 0,784m - 294
=> m = \(\dfrac{30875}{49}\left(g\right)\)
mdd sau pư = \(\dfrac{28915}{49}\left(g\right)\)
=> \(C\%_{Fe_2\left(SO_4\right)_3}=C\%_{H_2SO_4\left(dư\right)}=\dfrac{200}{\dfrac{28915}{49}}.100\%=33,89\%\)

BaO+H2O -> Ba(OH)2
0,02 0,02
a) CM = n/V = 0,02/0,02 = 1M
b) Ba(OH)2 + H2SO4 -> BaSO4 +2H2O
0,02 0,02
=> m = 0,392 g
D = m/V = 1,14
=> 0,392/V = 1,14 => V = 0,34l

Bài 2 :
\(V_{dd}=V_{\text{dung dịch sau phản ứng}}\) khi và chỉ khi sản phẩm không tạo ra kết tủa hay lượng khí thoát ra.
Nếu : trong TH có kết tủa hoặc khí thoát ra dẫn đến khối lượng dung dịch sau phản ứng thay đổi nên thể tích dung dịch sau phản ứng thay đổi theo
\(m_{\text{dung dịch sau phản ứng}}=m_{\text{dung dịch đầu}}-\left(m_{khí}+m_{\downarrow}\right)\left(\text{nếu có}\right)\)

mH2SO4 = 9,8%.200=19,6(g) -> nH2SO4=0,2(mol)
nAl=0,1(mol)
PTHH: 2Al +3 H2SO4 -> Al2(SO4)3 + 3H2
Ta có: 0,1/2 < 0,2/3 => H2SO4 dư, Al hết, tính heo nAl
nAl2(SO4)3=mAl/2=0,1/2=0,05(mol)
mAl2(SO4)3 (LT)= 0,05.342=17,1(g)
Vì: H=75%
=>mAl2(SO4)3 (TT)=75%. 17,1=12,825(g)

\(1.a.Na_2CO_3+2HCl->2NaCl+H_2O+CO_2\\ 2n_{CO_2}=n_{HCl}=\dfrac{0,448}{22,4}=0,04mol\\ C\%_{HCl}=\dfrac{0,04\cdot36,5}{200}\cdot100\%=0,73\%\\ b.m_{Na_2CO_3}=0,02\cdot106=2,12g\\ m_{NaCl}=2,88g\)
a. Theo phương trình phản ứng, 1 mol Na2CO3 phản ứng với 2 mol HCI. Do đó, nếu nHCI là số mol của HCl cần dùng thì theo đề bài ta có:
nHCI = 2 x nNa2CO3 = 2 x 0.02 = 0.04 mol
Khối lượng của CO2 sinh ra trong phản ứng là:
m(CO2) = n(CO2) x MM(CO2) = n(Na2CO3) x 1 x MM(CO2) = 0.02 x 44 = 0.88 g
Theo đó, % khối lượng của HCl trong dung dịch HCl ban đầu là:
% HCI = m(HCI) / m(HCI)ban đầu x 100% = n(HCI) x MM(HCI) / m(HCI)ban đầu x 100% với MM(HCI) = 36.5 g/mol
Từ đó suy ra:
m(HCI)ban đầu = n(HCI) x MM(HCI) / % HCI
m(HCI)ban đầu = 0.04 x 36.5 / 0.73 = 2 g
b. Tổng khối lượng của Na2CO3 và HCl ban đầu là:
m(Na2CO3 + HCl)ban đầu = m(Na2CO3) + m(HCI)ban đầu = 0.02 x 106 + 2 = 4.12 g
Khối lượng của NaCl tạo thành là:
m(NaCl) = n(NaCl) x MM(NaCl) = n(HCI) x MM(NaCl) / 2 = 0.04 x
58.5/2 = 1.17 g
Khối lượng của H2O tạo thành là:
m(H2O) = n(H2O) x MM(H2O) = n(Na2CO3) x 2 x MM(H2O) = 0.02
x 2 x 18 = 0.72 g
Vậy khối lượng của sản phẩm tạo thành là:
m(NaCl + H2O) = m(NaCl) + m(H2O) = 1.17 +0.72 = 1.89 g
Kiểm tra:
m(Na2CO3 + HCl)ban đầu - m(NaCl + H2O) = 4.12 - 1.89 = 2.23 g
Khối lượng CO2 sinh ra tính được từ phần a cũng bằng 0.88 g, nên kết quả tính toán là chính xác.
Câu 1:
Khối lượng CaO:
Số mol CaO:
Pt:
Vậy khối lượng Ca(OH)2tạo thành: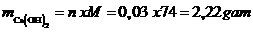
Vậy mct = 2,22 gam
Vậy nồng độ phần trăm Ca(OH)2:
Câu 2:
+ Khối lượng riêng khối lượng dd H2SO4 là
khối lượng dd H2SO4 là 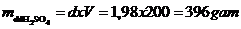
+
Số mol CuO: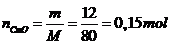
Vậy khối lượng chất tan: mct = 24 gam
Mà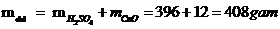
Vậy nồng độ phần trăm: