Viết phương trình hoá học của phản ứng tạo thành muối KCl và MgSO4.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án:
Niken có thể phản ứng được với các dung dịch muối của kim loại đứng sau nó trong dãy điện hóa:
Ni+CuSO4→NiSO4+Cu↓Ni+CuSO4→NiSO4+Cu↓
Ni+Pb(NO3)2→Ni(NO3)2+Pb↓Ni+Pb(NO3)2→Ni(NO3)2+Pb↓
Ni+2AgNO3→Ni(NO3)2+2Ag↓

Niken có thể phản ứng được với các dung dịch muối sau đây:
Ni + CuSO4 → NiSO4 + Cu↓
Ni + Pb(NO3)2 → Ni(NO3)2 + Pb↓
Ni + 2AgNO3 → Ni(NO3)2 + 2Ag↓

- Viết phương trình hoá học của phản ứng giữa Mg với các dung dịch CuSO 4 , FeSO 4 và AgNO 3 .
Mg + FeSO 4 → MgSO 4 + Fe
Mg + CuSO 4 → MgSO 4 + Cu
Mg + AgNO 3 → Mg NO 3 2 + Ag
- Viết phương trình hoá học của phản ứng giữa Fe với các dung dịch CuSO 4 , AgNO 3
Fe + CuSO 4 → FeSO 4 + Cu
Fe + 2 AgNO 3 → Fe NO 3 2 + 2Ag
- Viết phương trình hoá học của phản ứng giữa Cu với dung dịch AgNO 3
Cu + AgNO 3 → Cu NO 3 2 + Ag

\(CH_3CH_2CH_2OH+CuO\rightarrow CH_3CH_2CHO+Cu+H_2O\)

Phương trình phản ứng:
4P + 5O2 → 2P2O5 (1)
P2O5 + 4NaOH → 2Na2HPO4 + H2O (2)

Trích mẫu thử
Cho mẫu thử vào nước :
- mẫu thử nào tan là $KCl,K_2CO_3$ - nhóm 1
- mẫu thử nào không tan là $CaCO_3,BaSO_4$ - nhóm 2
Cho dung dịch $HCl$ vào nhóm 1 :
- mẫu thử nào tạo khí không màu không mùi là $K_2CO_3$
$K_2CO_3 + 2HCl \to 2KCl + CO_2 + H_2O$
- mẫu thử không hiện tượng gì là $KCl$
Cho dung dịch $HCl$ vào nhóm 2 :
- mẫu thử nào tạo khí không màu không mùi là $CaCO_3$
$CaCO_3 + 2HCl \to CaCl_2 + CO_2 + H_2O$
- mẫu thử không hiện tượng gì là $BaSO_4$

a) PTHH : \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b) \(n_{H_2SO_4}=C_MV=1,2\cdot0,5=0,6\left(mol\right)\)
PTHH : \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,6 0,6 0,6
\(\Rightarrow m_{FeSO_4}=n_{FeSO_4}M_{FeSO_4}=0,6\cdot152=91,2\left(g\right)\)
c) Từ câu b \(\Rightarrow n_{H_2}=0,6\left(mol\right)\)
\(\Rightarrow V_{H_2}=n_{H_2}.22,4=0,6\cdot22,4=13,44\left(l\right)\)
d) PTHH : \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
0,6 0,6
\(\Rightarrow m_{Cu}=n_{Cu}M_{Cu}=0,6\cdot64=38,4\left(g\right)\)
a)\(PTHH:Fe+H_2SO_4\xrightarrow[]{}FeSO_4+H_2\)
b)Đổi 500ml = 0,5l
Số mol của H2SO4 là:
\(C_{MH_2SO_4}=\dfrac{n_{H_2SO_4}}{V_{H_2SO_{\text{4 }}}}\Rightarrow n_{H_2SO_4}=C_{MH_2SO_4}.V_{H_2SO_4}=1,2.0,5=0,6\left(mol\right)\)
\(PTHH:Fe+H_2SO_4\xrightarrow[]{}FeSO_4+H_2\)
Tỉ lệ : 1 1 1 1 (mol)
Số mol : 0,6 0,6 0,6 0,6(mol)
Khối lượng sắt(II)sunfat thu được là:
\(m_{FeSO_4}=n_{FeSO_4}.M_{FeSO_{\text{4 }}}=0,6.152=91,2\left(g\right)\)
c) Thể tích khí H2 thoát ra là:
\(V_{H_2}=n_{H_2}.22,4=0,6.22,4=13,44\left(l\right)\)
d)\(PTHH:CuO+H_2\xrightarrow[]{t^0}Cu+H_2O\)
tỉ lệ :1 1 1 1 (mol)
số mol :0,6 0,6 0,6 0,6 (mol)
Khối lượng CuO điều chế được là:
\(m_{CuO}=n_{CuO}.M_{CuO}=0,6.80=48\left(g\right)\)

\(2KClO_3\rightarrow3O_2+2KCl\)
\(m_{KClO_3}=m_{O_2}+m_{KCl}\)
\(\Rightarrow m_{KCl}=m_{KClO_3}-m_{KCl}=24,5-9,6=14,9\left(g\right)\)
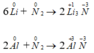
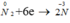
\(KOH+HCl\rightarrow KCl+H_2O\\ MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)