cho 16g hỗn hợp X gồm 2 kim loại Bari và R (có hoá trị không đổi) tác dụng hết với nước(dư) thu được 9.10^22 phân tử H2 . Mặt khác nếu đốt cháy 16g hỗn hợp X ở trên thì cần dùng V lít O2 (đktc).
a.Tính V
b.Tìm tên kim loại R . Biết rằng với cùng lượng kim loại R trong 16g trên cho tác dụng vừa đủ HCl(dư) thì tạo ra 1,12 lít H2(đktc)
ko chép mạng ạ

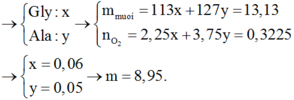
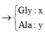
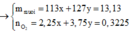
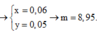

Tìm tên kim loại R - Lê Nhật Minh
Đừng trích dẫn bài từ nguồn khác vào , không hay đâu bạn.