Câu 5
A là dung dịch HCl. B là dung dịch Ba(OH)2.
Trộn 50 ml dung dịch A với 50 ml dung dịch B thu được dung dịch D có dư A. Để trung hòa hết lượng dư A trong D người ta phải dùng hết 50 ml dung dịch KOH 0,1M.
Trộn 50 ml dung dịch A với 150 ml dung dịch B thì thu được dung dịch E có dư B. Trung hòa hết lượng B dư trong E người ta phải dùng hết 350 ml dung dịch HNO3 0,1M. Tính nồng độ mol/lit của các dung dịch A, dung dịch B.
HELP ME!


Đặt nồng độ HCl trong dung dịch A là x
Đặt nồng độ Ba(OH)2 trong dung dịch B là y
- Khi trộn 50ml dung dịch A với 50ml dung dịch B thì HCl dư, ta có:
2HCl + Ba(OH)2 → BaCl2 + 2H2O (1)
0,1y← 0,05y mol
HCl + NaOH → NaCl + H2O (2)
0,005←0,005 mol
Ta có: 2.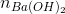 + nNaOH = nHCl
+ nNaOH = nHCl
0,1y + 0,005 = 0,05x
x– 2y = 0,1 (*)
- Khi trộn 50 ml dung dịch A với 150ml thì Ba(OH)2 dư, ta có:
2HCl + Ba(OH)2 → BaCl2 + 2H2O (3)
0,05x→0,025x mol
2HNO3 + Ba(OH)2 → Ba(NO3)2 + H2O (4)
0,035→ 0,0175 mol
Ta có: 2.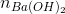 = (nHCl +
= (nHCl + 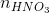 )
)
0,15y = 0,025x + 0,0175
x– 6y = - 0,7 (**)
Giải hệ pt:
x– 6y = -0,7
x– 2y = 0,1
=>x = 0,5; y= 0,2
=>CM của HCl = 0,5M
CM của Ba(OH)2 = 0,2M