Nhiệt phân hoàn toàn m gam Cu(OH)2 , thu được 4g một chất rắn màu đen. a.Tính khối lượng của Cu(OH)2 đem nhiệt phân. b.Hoà tan m gam Cu(OH)2 trên bằng 250g dung dịch H2SO4 9,8% thu được dung dịch X . Tính nồng độ phần trăm của các chất trong dung dịch X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, \(n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\)
PT: \(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
Theo PT: \(n_{Cu\left(OH\right)_2}=n_{CuO}=0,05\left(mol\right)\)
\(\Rightarrow m_{Cu\left(OH\right)_2}=0,05.98=4,9\left(g\right)\)
b, \(m_{H_2SO_4}=250.9,8\%=24,5\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\)
PT: \(Cu\left(OH\right)_2+H_2SO_4\rightarrow CuSO_4+2H_2O\)
Xét tỉ lệ: \(\dfrac{0,05}{1}< \dfrac{0,25}{1}\), ta được H2SO4 dư.
Theo PT: \(n_{CuSO_4}=n_{H_2SO_4\left(pư\right)}=n_{Cu\left(OH\right)_2}=0,05\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=0,25-0,05=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{CuSO_4}=\dfrac{0,05.160}{4,9+250}.100\%\approx3,14\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{0,2.98}{4,9+250}.100\%\approx7,69\%\end{matrix}\right.\)

a)
Cu(OH)2 ➝ CuO + H2O (2)
CuO + H2SO4➝ CuSO4 + H2O (1)
Đổi : 100ml= 0,1lít
Số mol axit sunfuric cần dùng là:
n= CM . V = 0,1 . 2=0,2 mol
Từ (1) ➜ nH2SO4= nCuO= 0,2mol
Khối lượng CuO đã nhiệt phân là:
m= n.M= 0,2. 80=16 (g)
Từ (2)➜nCu(OH)2= nCuO=0,2 mol
Khối lượng đồng hiđroxit đã dùng là:
m= n.M = 0,2.98=19,6 (g)
b)
Từ (1)➙ nCuSO4=nCuO= 0.2mol
Khối lượng muối thu được là:
m=n.M= 0,2 . 160=32 (g)
O

Cho m gam kim loại Mg vào dung dịch axit clohidric dư, phản ứng hoàn toàn tạo ra 6,72 lít khí hiđro (đktc). Giá trị của m là (biết Mg=24) *
7,2
3,6.
14,4.
6,72.
Nhiệt phân hoàn toàn 9,8 g Cu(OH)₂ thu được một chất rắn màu đen, dùng khí H₂ dư khử chất rắn màu đen đó thu được một chất rắn màu đỏ có khối lượng là (biết Cu=64, O=16, H=1) *
6,4 g
8 g.
12,8 g.
9,8 g.
Chất nào sau đây là muối *
KOH.
HCl.
CuSO4
MgO.
Nhúng 1 thanh kim loại đồng vào 100 ml dung dịch AgNO₃ 0,4 M. Sau khi phản ứng hoàn toàn thu được m gam kim loại bám trên thanh đồng. Giá trị của m là (biết Ag=108, Cu=64, N=14, O=16) *
4,32
21,6.
25,6.
12,8.
Phản ứng nào dưới đây là phản ứng trao đổi trong dung dịch? *
2Na + 2H₂O --> 2NaOH + H₂.
BaO + H₂O --> Ba(OH)₂.
Zn + H₂SO₄ --> ZnSO₄ +H₂.
BaCl2 + H2SO4 ---> BaSO4 + 2HCl
Cho 100ml dung dịch KOH 2M tác dụng với 200ml dung dịch H₂SO₄ 3M, sau phản ứng cho thêm một mảnh Mg dư vào sản phẩm thấy thoát ra một thể tích khí H₂ (đktc) là *
11,2 lít.
8,96 lít.
3,36 lít
6,72 lít
Hình như sai đề
Câu cuối đáp án là 11,2 lít nhé!
Câu kim loại đồng tính như nào ra 4,32 nhỉ?

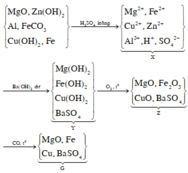
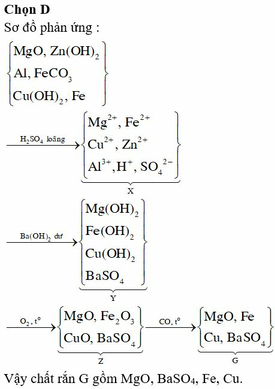
Chọn A
Để hỗn hợp tan hết thì số mol oxi sinh ra khi nhiệt phân phải ít nhất vừa đủ để oxit hóa kim loại tự do Þ nCu max = nCu(NO3)2 = 44/(252) =11/63 => mCu < 64x11/63 = 11,17 gam.

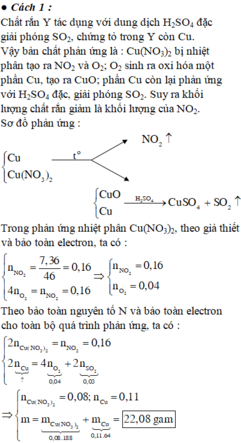
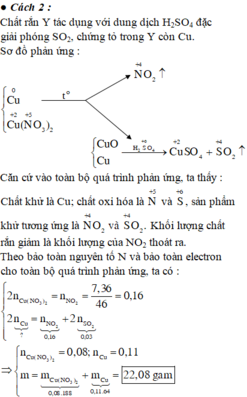
Do Y tác dụng với H 2 S O 4 tạo S O 2 nên Y có Cu.
Do đó khối lượng chất rắn giảm là khối lượng của N O 2

Đáp án là D
a) PTHH: \(Cu\left(OH\right)_2\xrightarrow[]{t^o}CuO+H_2O\)
Ta có: \(n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)=n_{Cu\left(OH\right)_2}\) \(\Rightarrow m_{Cu\left(OH\right)_2}=0,05\cdot98=4,9\left(g\right)\)
b) PTHH: \(Cu\left(OH\right)_2+H_2SO_4\rightarrow CuSO_4+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{Cu\left(OH\right)_2}=0,05\left(mol\right)\\n_{H_2SO_4}=\dfrac{250\cdot9,8\%}{98}=0,25\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Axit còn dư
\(\Rightarrow\left\{{}\begin{matrix}n_{CuSO_4}=0,05\left(mol\right)\\n_{H_2SO_4\left(dư\right)}=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C\%_{CuSO_4}=\dfrac{0,05\cdot160}{4,9+250}\cdot100\%\approx3,14\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{0,2\cdot98}{4,9+250}\cdot100\%\approx7,7\%\end{matrix}\right.\)