Nung không hoàn toàn 24,5 gam KClO3 một thời gian thu được 17,3 gam chất rắn A và khí B. Dẫn toàn bộ khí B vào bình 1 đựng 4,96 gam photpho đun nóng, phản ứng xong dẫn khí còn lại vào bình 2 đựng 0,3 gam cacbon để đốt cháy hoàn toàn.
a) Tính hiệu suất của phản ứng phân hủy.
b) Tính khối lượng của các chất trong mỗi bình sau phản ứng

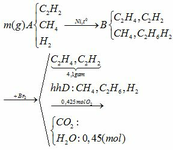

b.
4P + 5O2 → 2P2O5
0,16→ 0,2
Dư: 0,025
Sau pứ m(bình 1) = mP2O5 = 11,36 (g)
O2 + 2C → 2CO
0,025→ 0,05 0,05
Dư: 0,25
Sau pứ m(bình 2) = mCdư = 3 (g)