Đốt cháy hoàn toàn một lượng chất hữu cơ A (C,H,O) cần vừa đủ 5.376 lít khí Oxi (đktc). Cho toàn bộ sản phẩm tạo thành vào một lượng dung dịch nước vôi trong. Sau khi phản ứng kết thúc thu được 10 gam kết tủa và 350 ml một dung dịch muối có nồng độ 0.2M, khối lượng dung dịch muối này nặng hơn khối lượng dung dịch nước vôi trong đem dùng là 4.88 gam. Hãy xác định công thức cấu tạo của phân tử hợp chất hữu cơ A, biết 40 < MA < 74.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

X + O2 → CO2 + H2O (1)
CO2 + Ca(OH)2 → CaCO3 + H2O (2)
2 CO2 + Ca(OH)2 → Ca(HCO3)2 (3)
Áp dụng ĐLBTKL ta có
\(m_{CO_2}+m_{H_2O}+m_{ddCa\left(OH\right)_2}=m_{CaCO_3}+m_{Ca\left(HCO_3\right)_2}\)
mà \(m_{Ca\left(HCO_3\right)_2}=m_{ddCa\left(OH\right)_2}\)+ 8,6
=>\(m_{CO_2}+m_{H_2O}\)= 10 + 8,6=18,6(g)
Từ (2), (3) =>\(n_{CO_2}=\dfrac{10}{100}\)+ 2. 0,5 . 0,2 = 0,3 (mol)
=> m = 0,3 .12 = 3,6 (gam)
\(m_{H_2O}\)= 18,6 - 0,3 . 44 = 5,4 (gam) => mH=\(\dfrac{5,4}{18}.2\) = 0,6 (gam)
Áp dụng ĐLBTKL ta có : mX +mO2 = mCO2 + mH2O
mX = \(18,6-\dfrac{6,72}{22,4}.32\) = 9(g)
mO = 9 – (3,6 + 0,6) = 4,8 (g)
Vậy A chứa C, H, O có công thức CxHyOz
Ta có tỷ lệ x : y : z = \(\dfrac{3,6}{12}:\dfrac{0,6}{1}:\dfrac{4,8}{16}\) = 1: 2: 1
Công thức đơn giản nhất của X có dạng (CH2O)n

Đáp án : B
P1 : nCO2 = 0,05 mol = nX => Các chất trong X đều có 1 C
P2 : nAgNO3 = 0,08 mol
P3 : nH2 = 0,02 mol => nH linh động = 0,04 mol = nOH + nCOOH
=> X gồm : HCHO ; CH3OH ; HCOOH
=> nHCHO + nCH3OH + nHCOOH = 0,05
,4nHCHO + 2nHCOOH = 0,08
,nCH3OH + nHCOOH = 0,04
=> nHCHO = 0,01 ; nCH3OH = nHCOOH = 0,02 mol
=> Trong 0,15 mol X có : mX = 5,58g

Đáp án B
+ n 1 3 X = 0 , 05 n C t r o n g 1 3 X = n C O 2 = n C a C O 3 = 0 , 05 ⇒ C ¯ X = 0 , 05 0 , 05 = 1 X g ồ m C H 3 O H ; H C H O ; H C O O H + n C H 3 O H + n H C H O + n H C O O H = 0 , 05 B T E : 4 n H C H O + 2 n H C O O H = n A g = 0 , 08 B T N T H : n C H 3 O H + n H C O O H = 2 n H 2 = 0 , 04 ⇒ n C H 3 O H = 0 , 02 n H C H O = 0 , 01 n H C O O H = 0 , 02 ⇒ m 0 , 15 m o l X = 3 ( 0 , 02 . 32 + 0 , 01 . 30 + 0 , 02 . 46 ) = 5 , 58 g a m

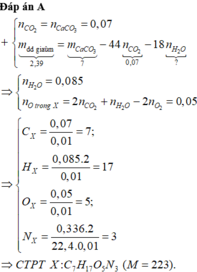
0 , 02 m o l X 0 , 06 m o l N a O H → t O 1 m u ố i c ủ a a x i t h ữ u c ơ đ ơ n c h ứ c 2 m u ố i c ủ a h a i a m i n o a x i t h ơ n k é m n h a u 14 đ v C p t c h ứ a m ộ t n h ó m – C O O H v à m ộ t n h ó m – N H 2 ,
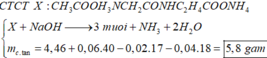

Đáp án : A
nN2 = 0,015 mol => nN(X) = 0,03 mol => trong X có 3 N
Khi sản phẩm cháy vào dung dịch nước vôi trong dư :
,nCaCO3 = nCO2 = 0,07 mol => X có 7C
,mdung dịch giảm = mCaCO3 – (mCO2 + mH2O) => nH2O = 0,085 mol
=> nH(X) = 2nH2O = 0,17 mol => số H trong X là 17
Bảo toàn O : nO(X) + 2nO2 = 2nCO2 + nH2O => nO(X) = 0,05 mol => Trong X có 5 Oxi
CTTQ : C7H17O5N3
Xét 4,46g X : nX = 0,02 mol => nNaOH = 3nX
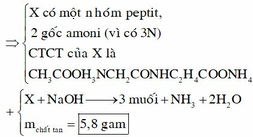
Mặt khác phản ứng tạo 1 muối axit hữu cơ và 2 muối của amino axit
=> X có : 1 gốc axit hữu cơ và 2 gốc amino axit đồng đẳng kế tiếp
Xét Công thức : CH3COO-NH3-CH2-CO-NH-CH(CH3)-COONH4
=> hỗn hợp muối gồm : 0,02 mol mỗi chất : CH3COONa ; H2N-CH2-COONa ; H2N-CH(CH3)-COONa
=> m = 5,8g

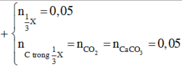
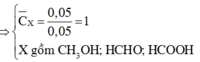
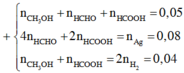
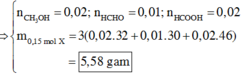


CxHyOz + O2 => CO2 + H2O
CO2 + Ca(OH)2 -> CaCO3 + H2O
2CO2+ Ca(OH)2 -> Ca(HCO3)2
nO2 = 0.24mol
nCaCO3 = 10/100 = 0.1 mol
nCa(HCO3)2 = 0.35*0.2=0.07mol
CO2 + Ca(OH)2 -> CaCO3 + H2O
(mol) 0.1 0.1
2CO2+ Ca(OH)2 -> Ca(HCO3)2
(mol) 0.14 0.07
nCO2 = 0.1 + 0.14 = 0.24 mol
mdd tăng = mCO2 + mH2O -mkt = 4.88g
=> mH2O = mdd tăng + mkt - mCO2 = 4.88 + 10-0.24*44 =4.32g
Ad định luật bảo toàn khối lượng
mA =mCO2 + mH2O -mO2 = 0.24*44 + 4,32 - 0.24*32=7.2g
nH2O =4.32/18= 0.24mol
nC = nCO2 = 0.24mol
mC = 0.24*12=2.88g
nH = 2nH2O = 0.48mol
mH = 0.48g
mO = 7.2 - 2.88-0.48=3.84
nO = 3.84/16= 0.24 mol
Gọi CTHH của A là CxHyOz
x:y:z = nC : nH : nO
x:y:z = 0.24 : 0.48 : 0.24
x:y:z = 1:2:1
CT đơn giản nhất của A là CH2O
CTPT có dangk (CH2O)n
40 <30n <74 => 1.3<n<2.4
=> n=2
Vậy CTPT của A là C2H4O2
Cảm ơn bạn!