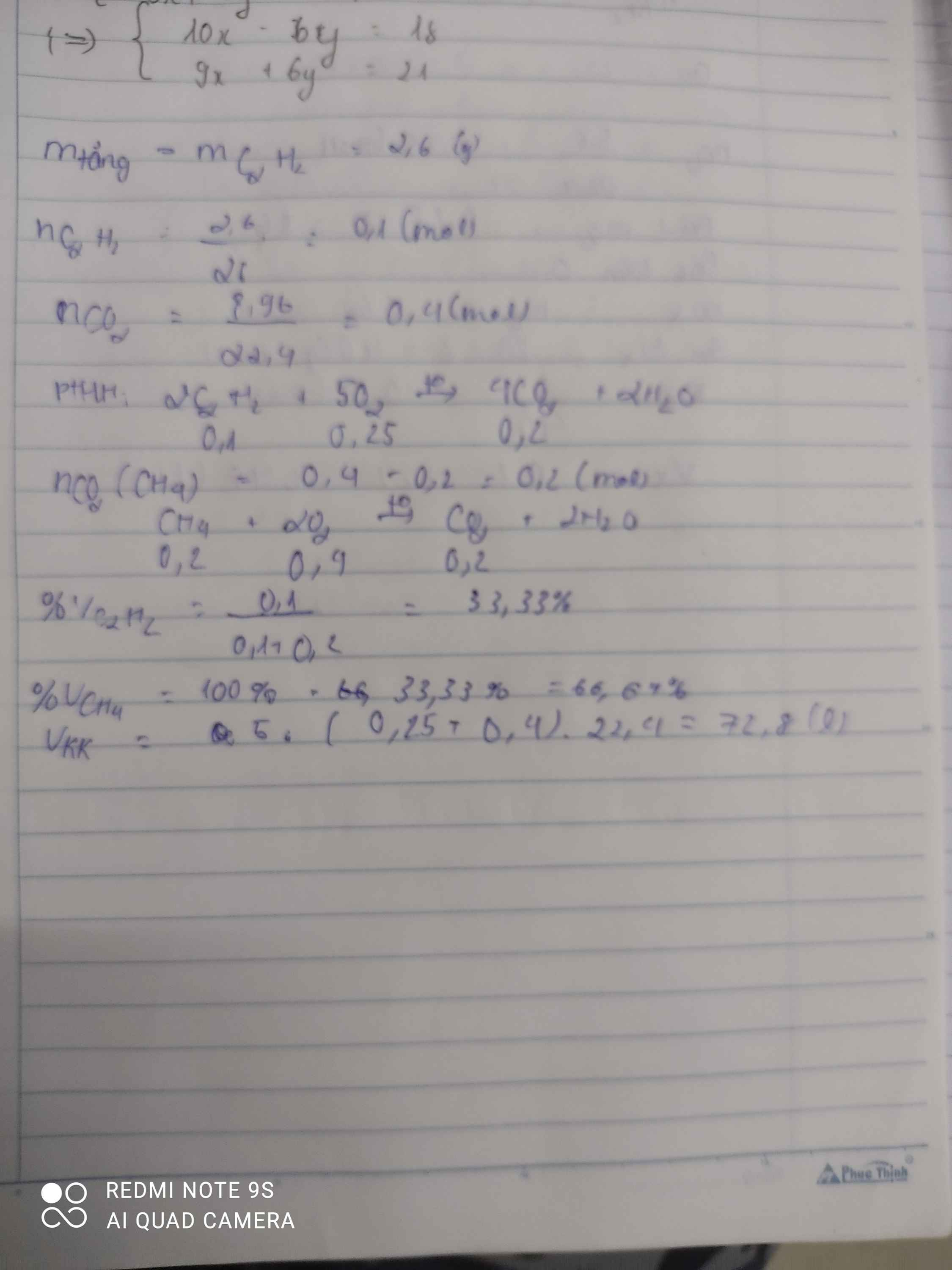Hidrocacbon (C2H2n+2) có TCHH tương tự axetilen. Cho A vào bình đựng dung dịch brom, sau phản ứng thấy có 0,06 mol brom phản ứng, thu được hai hợp chất hữu cơ và thấy khối lượng bình tăng 1,6 gam. Xác định CTPT của A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{CO_2}=\dfrac{8,96}{22,4}=0,4mol\)
\(m_{tăng}=m_{Br_2}=m_{C_2H_2}=2,6g\)
\(\Rightarrow n_{C_2H_2}=\dfrac{2,6}{26}=0,1mol\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
0,1 0,1
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_2+\dfrac{5}{2}O_2\underrightarrow{t^o}2CO_2+H_2O\)
0,1 0,25 0,2
\(\Rightarrow n_{CO_2\left(CH_4\right)}=0,4-0,2=0,2mol\)
\(\Rightarrow n_{CH_4}=0,2mol\Rightarrow n_{O_2}=0,4mol\)
a)\(\%V_{CH_4}=\dfrac{0,2}{0,4}\cdot100\%=50\%\)
\(\%V_{C_2H_2}=100\%-50\%=50\%\)
b)\(\Sigma n_{O_2}=0,4+0,25=0,65mol\)
\(\Rightarrow V_{O_2}=0,65\cdot22,4=14,56l\)
\(\Rightarrow V_{kk}=14,56\cdot5=72,8l\)

Vì sau phản ứng với dung dịch brom dư, có khí thoát ra khỏi bình nên trong hỗn hợp X ban đầu có ankan.

Do đó trong hỗn hợp X có 1 hidrocacbon có số nguyên tử C trong phân tử nhỏ hơn 1,67 và 1 hidrocacbon có số nguyên tử C trong phân tử lớn hơn 1,67.
Mà anken luôn có số nguyên tử C trong phân tử lớn hơn hoặc bằng 2.
Nên ankan trong X có số nguyên tử C nhỏ hơn 1,67.
Suy ra ankan đó là CH4.
Gọi công thức của anken trong X là CnH2n.
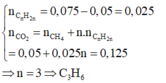
Do đó 2 hidrocacbon trong X là CH4 và C3H6.
Đáp án C.

\(n_{C_3H_3Ag}=\dfrac{7,35}{147}=0,05\left(mol\right)\)
=> \(n_{C_3H_4}=0,05\left(mol\right)\)
\(n_{Br_2}=\dfrac{6,4}{160}=0,04\left(mol\right)\)
=> \(n_{C_2H_4}=0,04\left(mol\right)\)
=> \(\left\{{}\begin{matrix}\%C_3H_4=\dfrac{0,05.40}{5,52}.100\%=36,23\%\\\%C_2H_4=\dfrac{0,04.28}{5,52}.100\%=20,29\%\\\%C_2H_6=100\%-36,23\%-20,29\%=43,48\%\end{matrix}\right.\)
=> A

Theo giả thiết, Y phản ứng được với dung dịch brom trong CC14. Do đó trong Y còn hidrocacbon không no và H2 phản ứng hết.
Ta có sơ đồ sau:

Áp dụng định luật bảo toàn nguyên tố cho C ta có:
![]()
Có 0,5 mol X

phản ứng vừa đủ với 0,4 mol Br2
Trong đó k là tỉ lệ giữa hỗn hợp X cho tác dụng với dung dịch brom và hỗn hợp X đem đốt cháy.
Ta có: 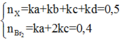
![]()
Nhân 2 vế của (1) với 4 rồi trừ đi (3) ta được:
4(a + 2c - d) - (a - 4b + 6c - 4d) = 4.0,15 - 0 <=> 3a + 4b + 2c = 0,6
Kết hợp với (2) có ![]()
Áp dụng định luật bảo toàn nguyên tố cho nguyên tố C ta có: ![]()
Khi đó khối lượng dung dịch giảm là: ![]()
![]()
Áp dụng định luật bảo toàn nguyên tố cho O, ta có:
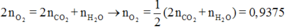
Vậy V = 0,9375.22,4 = 21 (lít)
Đáp án C

a, \(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\Rightarrow n_H=0,2.2=0,4\left(mol\right)\)
\(n_{CO_2}=n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)=n_C\)
⇒ mC + mH = 0,2.12 + 0,4.1 = 2,8 (g) < mA
→ A gồm C, H và O.
⇒ mO = 6 - 2,8 = 3,2 (g) \(\Rightarrow n_O=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Gọi CTPT của A là CxHyOz.
⇒ x:y:z = 0,2:0,4:0,2 = 1:2:1
→ CTPT của A có dạng (CH2O)n
Không biết đề có cho thêm dữ kiện liên quan đến MA không bạn nhỉ?

Chất A chứa C, H, O khi đốt cháy sẽ sinh ra CO 2 và H 2 O . Khi qua bình 1 đựng H 2 SO 4 đặc thì H 2 O bị hấp thụ. Vậy khối lượng H 2 O là 1,8 gam. Qua bình 2 có phản ứng :
Ca OH 2 + CO 2 → CaCO 3 ↓+ H 2 O
Theo phương trình : n CO 2 = n CaCO 3 = 10/100 = 0,1 mol
Vậy khối lượng cacbon có trong 3 gam A là 0,1 x 12 = 1,2 (gam).
Khối lượng hiđro có trong 3 gam A là 0,1 x 2 = 0,2 (gam).
Khối lượng oxi có trong 3 gam A là 3 - 1,2 - 0,2 = 1,6 (gam).
Gọi công thức phân tử của A là C x H y O z
Ta có :
60 gam A → 12x gam C → y g H → 16z gam O
3 gam → 1,2 gam → 0,2 gam → 1,6 gam
x = 1,2x60/36 = 2; y = 60x0,2/3 = 4
z = 1,6x60/48 = 2
→ Công thức phân tử của A là C 2 H 4 O 2

\(C_2H_2+2Br_2->C_2H_2Br_4\\ n_{hh}=\dfrac{3,36}{22,4}=0,15mol\\ n_{CH_4}=\dfrac{2,24}{22,4}=0,1mol\\ n_{C_2H_2}=0,05mol\\ n_{Br_2}=2.0,05=0,1mol\\ m_{Br_2}=0,1.160=16g\\ \%V_{CH_4}=\dfrac{0,1}{0,15}.100\%=66,67\%\\ \%V_{C_2H_2}=33,33\%\)

Chọn đáp án C
Ta có:
![]()
=> quy A về:
![]() .
.
Đặt n C 3 H 6 = x mol; n C 2 H 2 = y mol; n H 2 = z mol. Đốt A cũng như đốt B
![]()
![]()
mdung dịch giảm =
![]()
Thay số có:
100 x (3x + 2y) – [44.(3x + 2y) + 18.(3x + y + z)] = 21 gam.
Phản ứng xảy ra hoàn toàn mà B phản ứng với Br2/CCl4 ⇒ H2 phản ứng hết.
Bảo toàn liên kết π:
![]()
=> x + 2y = z + 0,15 mol.
Giả sử 0,5 mol A gấp k lần m gam A
⇒ 0,5 mol A chứa kx mol C3H6; ky mol C2H2; kz mol H2.
⇒ kx + ky + kz = 0,5 ⇒ k(x + y + z) = 0,5 mol (*). Lại có: kx + 2ky = 0,4 mol (**).
Lấy (*) chia (**) ⇒ (x + y + z) ÷ (x + 2y) = 0,5 ÷ 0,4 = 1,25.
Từ đó, giải hệ được: x = 0,1 mol; y = 0,15 mol; z = 0,25 mol.
=> m=0,1.42+0,15.26+0,25.2=8,6 gam.
∑ n C O 2 = 4 , 5 . 0 , 12 , 5 . 0 , 15 + 0 , 5 . 0 , 25 = 0 , 95 ( m o l )
=>V=21,28(l)