Tính khối lượng CaF2 cần dùng để điều chế 2,5 kg dung dịch axit flohidric nồng độ 40%. Biết hiệu suất phản ứng là 80%.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
m H F = 200 . 40 100 = 80 (gam) => n H F = 80 20 = 4 (mol)
m C a F 2 = 4 . 1 2 . 78 . 100 80 = 195 (gam)

Đáp án D
![]() .100 = 40% => mHF =160 (g) => n HF = 8 (mol)
.100 = 40% => mHF =160 (g) => n HF = 8 (mol)
CaF2 + H2SO4 → CaSO4 + 2HF
4 ← 8 (mol)
Do H% = 60%=> ![]() = 5 mol
= 5 mol
m = 5. (40+19.2) = 390 (g)

Chọn đáp án D
m H F = 400 . 40 100 = 160 (gam) → n H F = 160 20 = 8 (mol)
Bảo toàn F có: n H F = 2. n C a F 2 → n C a F 2 = 4 mol.
m C a F 2 = 4 , 78 80 % = 390 (gam)

mHF =\(\frac{40.2,5}{100}\) = 1kg
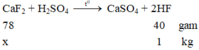
Phương trình phản ứng hóa học:
CaF2 + H2SO4 ---> CaSO4 + 2HF
78kg 40kg
X kg 1 kg
mCaF2 cần dùng: \(\frac{1.78}{40}.\frac{100}{80}\) = 2,4375 kg
mHF = = 1kg
Phương trình phản ứng hóa học:
CaF2 + H2SO4 CaSO4 + 2HF
78kg 40kg
X kg 1 kg
cần dùng:
= 2,4375 kg

\(1,n_{HF}=\dfrac{2,5.40\%}{100\%.20}=0,05(kmol)\\ PTHH:CaF_2+H_2SO_4\to CaSO_4+2HF\\ \Rightarrow n_{CaF_2}=0,025(kmol)\\ \Rightarrow m_{CaF_2}=0,025.78=1,95(kg)\\ 2,\text {Đặt }\begin{cases} n_{Fe}=x(mol)\\ n_{Al}=y(mol) \end{cases} \Rightarrow 56x+27y=11(1)\\ n_{H_2}=\dfrac{8,96}{22,4}=0,4(mol)\\ PTHH:Fe+2HCl\to FeCl_2+H_2\\ 2Al+6HCl\to 2AlCl_3+3H_2\\ \Rightarrow x+1,5y=0,4(2)\\ (1)(2)\Rightarrow \begin{cases} x=0,1(mol)\\ y=0,2(mol) \end{cases} \Rightarrow \begin{cases} \%_{Fe}=\dfrac{0,1.56}{11}.100\%=50,91\%\\ \%_{Al}=100\%-50,91\%=49,09\% \end{cases}\)
\(b,\Sigma n_{HCl}=2n_{Fe}+3n_{Al}=0,2+0,6=0,8(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,8}{2}=0,4(l)\)
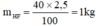
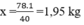
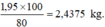


mHF = 40 x 2,5 / 100 = 1kg.
Phương trình hóa học của phản ứng:
CaF2 + H2SO4 \(\rightarrow\) CaSO4 + 2 HF
nHF = 1/20 mol.
nCaF2 = 1/40 mol.
mCaF2 = 1/40 x 78 = 1,95.
mCaF2 cần dùng = 1,95 x 100 / 80 = 2,4375kg.
CaF2 + H2SO4 \(\Rightarrow\) CaSO4 + 2HF theo phương trình ta có: nCaF2=1/2nHF=0,025mol nCaF2 Cần dùng =0,025/80%=0,03125mol mCaF2 cần dùng =0,03125.78=2,4375g