cho 11,2 g Fe phản ứng với Cl2 thu được FeCl3
a, viết phương trình phản ứng
b,tính thể tích khí Cl2
c,tính khối lượng của ản phẩm thu được.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Al}=\dfrac{5.4}{27}=0.2\left(mol\right)\)
\(4Al+3O_2\underrightarrow{^{^{t^0}}}2Al_2O_3\)
Ta có :
\(n_{Al_2O_3}=\dfrac{0.2\cdot2}{4}=0.1\left(mol\right)\)
\(m_{Al_2O_3}=0.1\cdot102=10.2\left(g\right)\)

\(n_{Fe}=\dfrac{m}{M}=\dfrac{28}{56}=0,5\left(mol\right)\\ PTHH:Fe+2HCl->FeCl_2+H_2\)
ti le 1 : 2 : 1 : 1
n(mol) 0,5-->1--------->0,5------>0,5
\(m_{FeCl_2}=n\cdot M=0,5\cdot\left(56+35,5\cdot2\right)=63,5\left(g\right)\\ V_{H_2\left(dktc\right)}=n\cdot22,4=0,5\cdot22,4=11,2\left(l\right)\)

\(n_{Fe}=\dfrac{28}{56}=0,5mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,5 1 0,5
\(V_{H_2}=0,5\cdot22,4=11,2l\)
\(m_{HCl}=1\cdot36,5=36,5g\)

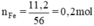
Phương trình hóa học của phản ứng:
Fe2O3 + 3H2 → 2Fe + 3H2O.
Khử 1 mol Fe2O3 cho 2 mol Fe.
x mol Fe2O3 → 0,2 mol.
x = 0,2 : 2 =0,1 mol.
m = 0,1 .160 =16g.
Khử 1 mol Fe2O3 cần 3 mol H2.
Vậy khử 0,1 mol Fe2O3 cần 0,3 mol H2.
V= 0,3 .22.4 = 6,72l.

\(n_{Al}=\dfrac{0,54}{27}=0,02\left(mol\right)\)
\(n_{Cl2\left(dktc\right)}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
a) Pt : \(2Al+3Cl_2\underrightarrow{t_o}2AlCl_3|\)
2 3 2
0,02 0,04 0,04
Lập tỉ số so sánh : \(\dfrac{0,02}{2}< \dfrac{0,04}{3}\)
⇒ Al phản ứng hết , Cl2 dư
⇒ Tính toán dựa vào số mol của Al
b) \(n_{AlCl3}=\dfrac{0,02.2}{2}=0,02\left(mol\right)\)
⇒ \(m_{AlCl3}=0,02.133,5=2,67\left(g\right)\)
\(n_{Cl2\left(dư\right)}=0,04-\left(\dfrac{0,02.3}{2}\right)=0,01\left(mol\right)\)
⇒ \(m_{Cl2}=0,01.71=0,71\left(g\right)\)
Chúc bạn học tốt

nCl2= 3,36/22,4=0,15(mol)
a) PTHH: 2 Fe + 3 Cl2 -to->2 FeCl3
b) nFe= 2/3. nCl2 = 2/3. 0,15=0,1(mol)
=>mFe=0,1.56=5,6(g)
=>m=5,6(g)
Số mol của khí clo ở dktc
nCl2= \(\dfrac{V_{Cl}}{22,4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) Pt : 2Fe + 3Cl2 → 2FeCl3\(|\)
2 3 2
0,1 0,15
b) Số mol của sắt
nFe = \(\dfrac{0,05.3}{2}=0,1\left(mol\right)\)
Khối lượng của sắt
mFe = nFe . MFe
= 0,1 . 56
= 5,6 (g)
Chúc bạn học tốt

\(n_{Fe}=\dfrac{5.6}{56}=0.1\left(mol\right)\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}FeCl_3\)
\(0.1.......0.15..........0.1\)
\(V_{Cl_2}=0.15\cdot22.4=3.36\left(l\right)\)
\(m_{FeCl_3}=0.1\cdot162.5=16.25\left(g\right)\)

\(n_{Zn}=\dfrac{13}{65}=0,2mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 0,4 0,2 0,2
\(m_{HCl}=0,4\cdot36,5=14,6g\)
\(a=m_{ddHCl}=\dfrac{14,6}{14,6\%}\cdot100\%=100g\)
\(V_{H_2}=0,2\cdot22,4=4,48l\)
\(m_{ZnCl_2}=0,2\cdot136=27,2g\)
PTHH: 2Fe + 3Cl2 → 2FeCl3
Số mol của Fe là: 11,2 : 56 = 0,2 mol
Số mol của Cl2 là: 0,2 . 3/2 = 0,3 mol
Thể tích của Cl2 là: 0,3 . 22,4 = 6,72 lít
Số mol của FeCl3 là : 0,2 . 2/2 = 0,2 mol
Khối lượng sản phẩm thu đc là: 0,2 . 162,5 gam
n Fe=0,2 mol
PTHH: 2Fe+3Cl2=>2FeCl3
0,2-> 0,3->0,2
=> V Cl2=0,3.22,4=6,72ml
mFeCl3=0,2.162,5=32,5g