Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có : CuxOy
x : y = \(\frac{m_{Cu}}{M_{Cu}}=\frac{m_O}{M_O}\)
= \(\frac{4}{64}:\frac{1}{16}\)= \(\frac{1}{1}\)
Suy ra CTHH của CuxOy là CuO
Ta có : CuxOy
x : y = \(\frac{m_{Cu}}{M_{Cu}}:\frac{m_O}{M_O}\)
= \(\frac{4}{64}:\frac{1}{16}\)= \(\frac{1}{1}\)
Suy ra CTHH của CuxOy là CuO

--> x /y = 64/ 64 = 1 / 1
--> x= 1 ; y= 1
Vậy CTHH là CuO

1)
Có mCu : mO = 4 : 1
=> 64.nCu : 16.nO = 4:1
=> nCu : nO = 1:1
=> CTHH: CuO
2) CTHH: MxOy
\(\dfrac{M_M.x}{16y}=\dfrac{7}{3}\)
=> \(M_M=\dfrac{112y}{3x}=\dfrac{2y}{x}.\dfrac{56}{3}\)
Xét \(\dfrac{2y}{x}=1\) => L
Xét \(\dfrac{2y}{x}=2\) => L
Xét \(\dfrac{2y}{x}=3\) => MM = 56(Fe) => \(\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTHH: Fe2O3
3)
\(m_O=\dfrac{47,06.102}{100}=48\left(g\right)=>n_O=\dfrac{48}{16}=3\left(mol\right)\)=> x = 3
=> MR2O3 = 102
=> MR = 27(Al)
4)
CTHH: R2O3
\(\dfrac{16.3}{2.M_R+16.3}.100\%=30\%=>M_R=56\left(Fe\right)\)
=> Fe2O3

a)\(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(S+O_2\underrightarrow{t^o}SO_2\)
\(C_4H_{10}+\dfrac{13}{2}O_2\underrightarrow{t^o}4CO_2+5H_2O\)
b)Gọi CTHH là \(Fe_xO_y\)
\(x:y=\dfrac{m_{Fe}}{56}:\dfrac{m_O}{16}=\dfrac{7}{56}:\dfrac{3}{16}=0,125:0,1875=2:3\)
\(\Rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\Rightarrow Fe_2O_3\)

\(a,\) Sắt + oxi ---to---> oxit sắt từ
\(b,PTHH:3Fe+2O_2\xrightarrow{t^o}Fe_3O_4\\ \text{Tỉ lệ: }3:2:1\\ c,\text{Bảo toàn KL: }m_{Fe}+m_{O_2}=m_{Fe_3O_4}\\ \Rightarrow m_{O_2}=m_{Fe_3O_4}-m_{Fe}=11,3-7,9=3,4(g)\)

\(a,\) Sắt + Oxi ----to----> Oxit sắt từ
\(b,3Fe+2O_2\xrightarrow{t^o}Fe_3O_4\)
Số nguyên tử Fe : Số phân tử O2 : Số phân tử Fe3O4 \(=3:2:1\)
\(c,\) Bảo toàn KL: \(m_{Fe}+m_{O_2}=m_{Fe_3O_4}\)
\(\Rightarrow m_{O_2}=11,3-7,9=3,4(g)\)

Phân tử khối của Đồng ôxit và Đồng sunfat có tỉ lệ 1/2
Mà phân tử khối của đồng sunfat (CUSO4) là 160 đvC
=> Phân tử khối của đồng oxit là :
160 * 1/2 = 80 (đvC)
Do đồng oxit gồm Cu và O nêncông thức hóa học của đồng oxit có dạng CuxOy
Ta có :
PTKđồng oxit = NTKCu * x + NTKO * y
=> 80 đvC = 64 * x + 16 * y
=> x < 2 vì nếu x = 2 thì 64 * 2 > 80
=> x = 1 , khi đó :
y = ( 80 - 64*1 ) : 16 = 1
Vậy công thức hóa học của đồng oxit là CuO
b) Gọi công thức của oxit là SxOy
x : y = nS : nO =
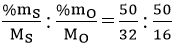
= 1,5625 : 3,125 = 1 : 2
Vậy công thức đơn giản của hợp chất M là: SO2

a).Phương trình chữ:
Kali + oxi ===> kali oxit
b). Phương trình hóa học:
K + O2 ===> K2O
4K + O2 ===> 2K2O
Tỉ lệ số nguyên tử, phân tử:
K : O2 : K2O=4 : 1 : 2
c). Công thức hóa học về khối lượng trong phản ứng:
\(m_K\) + \(m_{O_2}\) = \(m_{K_2O}\)
d). \(m_K\) + \(m_{O_2}\) = \(m_{K_2O}\)
7,8 + \(m_{O_2}\) = 9,4
=> \(m_{O_2}\) = 9,4 - 7,8 = 1,6 (g)
a/ PTHH chữ: kali + oxi ===> kali oxit
b/ PTHH: 4K + O2 ===> 2K2O
Tỉ lệ : 4 : 1 : 2
c/ Áp dụng định luật bảo toàn khối lượng
=> mK + mO2 = mK2O
d/ Theo phần c, ta có
mK + mO2 = mK2O
=> mO2 = mK2O - mK = 9,4 - 7,8 = 1,6 gam
Ta có: \(64x\div16y=4\div1\)
\(\Leftrightarrow x\div y=\dfrac{4}{64}\div\dfrac{1}{16}=1\div1\)
Vậy x=1 và y= 1
Vậy CTHH là CuO
PT điều chế đồng: 3CuO + 2Al → Al2O3 + 3Cu
PT điều chế đồng sunfat (CuSO4): CuO + H2SO4 → CuSO4 + H2