Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Khi cho từ từ vài giọt dung dịch silver nitrate vào ống nghiệm chứa từng dung dịch potassium fluoride, hydrochloric acid, sodium bromide:
+ Ống nghiệm xuất hiện kết tủa trắng AgCl => Ống nghiệm đó chứa HCl
HCl + AgNO3 → AgCl↓ + HNO3
+ Ống nghiệm xuất hiện kết tủa vàng nhạt AgBr => Ống nghiệm đó chứa NaBr
NaBr + AgNO3 → AgBr↓ + NaNO3
+ Ống nghiệm không có sự biến đổi do không có phản ứng hóa học xảy ra => Ống nghiệm chứa KF

1/ AgNO3 + KBr → AgBr + KNO3
AgNO3 + NaCl ⟶ AgCl + NaNO3
2/ Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
3/ \(Al+\dfrac{3}{2}Cl_2-^{t^o}\rightarrow AlCl_3\)
\(Fe+\dfrac{3}{2}Cl_2-^{t^o}\rightarrow FeCl_3\)
4/ CO2 + NaOH → Na2CO3 + H2O
SO2 + NaOH → Na2SO3 + H2O

Khi cho \(CO_2\) tác dụng với dung dịch nước vôi trong kết tủa trắng tạo ra làm vẩn đục dung dịch. Sau đó, kết tủa tăng đến tối đa, nếu thêm tiếp \(CO_2\) vào thì kết tủa lại dần bị hòa tan.
\(PTHH:\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\\ CO_2+CaCO_3+H_2O\rightarrow Ca\left(HCO_3\right)_2\)

Bạn tham khảo ở đây nha:Câu hỏi của Lê Quang Hiếu - Hóa học lớp 12 | Học trực tuyến
vì K+ và Na+ nên viết p.tử không chuẩn
a) khi cho H+ từ từ vào CO32- và HCO3- thì H+ td với CO32- trước vì nộng độ H+trong dd mới tạo thành nhỏ nên sẽ tác dụng từng nấc(vì chỉ từng giọt).lượng H+ chưa dư khi tác dụng với CO32- nên không thể tác dụng tiếp với HCO3- dẫn đến không có hiện tượng
H++CO32- -->HCO3-
b) khi cho H+ từ từ vào CO32- và HCO3- thì H+ td với CO32- trước. H+ tác dụng với CO32- còn dư tác dụng với 1 phần HCO3- tạo CO2 khí ko màu dd còn HCO3- tác dụng với OH- tạo CO32- td Ba2+ tạo kt trắng BaCO3
CO32-+H+-->HCO3-
HCO3-+H+-->H2O+CO2
HCO3-+OH-+Ba2+-->BaCO3+H2O(dư nên khi vậy ko dư ghi tỉ lệ Ba2+:OH-=1:2)
c)cho từ từ CO32- và HCO3- vào H+ thì pứ xảy ra đồng thời tạo đều tạo khí CO2 vì khi cho vào thì mt có nồng độ H+ lớn nên pứ xảy ra theo 2 nấc đồng thời
CO32-+2H+-->H2O+CO2
HCO3-+H+-->H2O+CO2

a) dd chuyển màu xanh tím
\(2KI+Cl_2\rightarrow2KCl+I_2\) (I2 làm xanh hồ tinh bột)
b) Bình thủy tinh dần bị ăn mòn:
\(SiO_2+4HF\rightarrow SiF_4+2H_2O\)

- Màu vàng lục của khí clo nhạt dần, dung dịch có màu nâu đỏ :
\(Cl_2 + 2KBr \to 2KCl + Br_2\)
- Màu vàng lục của khí clo nhạt dần, có chất rắn màu đen tím không tan
\(Cl_2 + 2KI \to 2KCl + I_2\)

a)
SO2 + Br2 + 2H2O =.> 2HBr + H2SO4
SO2 đã khử Br2 có màu thành HBr không màu
Khi dẫn khí SO2 vào dung dịch axit H2S dung dịch bị vẩn đục màu vàng:
SO2 + 2H2S = 3S + 2H2O , SO2 đã oxi hóa H2S thành S
b)Khi cho clo vào nước thì: Cl2 + H2O --> HCl + HClO.
Khi cho flo vào nước thì flo do là chất oxi hóa mạnh sẽ bốc cháy trong nước nên không thể điều chế được nước clo:
2F2 + 2H2O --> 4HF + O2
c)dùng dd KI có lẫn hồ tinh bột
2KI + H20 +O3--->2 KOH +I2 + O2
a. + Cho SO2 vào dd Br2:
Ptpu: SO2 + Br2 + 2H2O \(\rightarrow\) H2SO4 + 2HBr
(chất khử)
Htg: dd Br2 bị mất màu
+ Cho SO2 vào dd H2S
Ptpu: SO2 + 2H2S \(\rightarrow\) 3S\(\downarrow\) + 2H2O
(chất oxi hóa)
Htg: dd bị vẩn đục màu vàng
b. + Điều chế được nước clo vì clo tan nhiều trong nước nhưng chỉ một phần khí clo tác dụng với nước theo ptpu:
Cl2 + H2O\(\leftrightarrow\) HCl + HClO
+ Còn Flo tan trong nước thì oxi hóa hoàn toàn nước ngay ở nhiệt độ thường theo ptpu:
4F2 + 4H2O \(\rightarrow\) 4HF + O2
Do đó F2 không thể tồn tại trong nước
c. Cho quỳ tím td với ozon và oxi, ta thấy khi quỳ tím td với ozon thì quỳ tím hóa xanh, còn oxi ko pư
pthh:
\(O_3+2KI+H_2O\rightarrow I_2+2KOH+O_2\) (oxi không có)
Do tạo ra KOH nên O3 làm xanh quỳ tím ẩm dd KI
\(2Ag+O_3\rightarrow Ag_2O+O_2\) ( oxi không có pư)

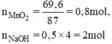
a) Phương trình hóa học của phản ứng:
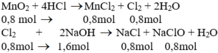
b) Theo pt (1): nCl2 = nMnCl2 = nMnO2 = 0,8 mol
Theo pt (2): nNaCl = nNaClO = nCl2 = 0,8 mol
nNaOH pư = 2. nCl2 = 2. 0,8 = 1,6 mol
⇒ nNaOH dư = 2 - 1,6 = 0,4 mol
Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM (NaCl) = CM (NaClO) = CM(MnCl2) = 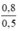 = 1,6 mol/ lit
= 1,6 mol/ lit
CM (NaOH)dư = 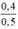 = 0,8 mol/ lit
= 0,8 mol/ lit
Xuất hiện kết tủa trắng
\(AlCl_3+3NH_3+3H_2O\rightarrow Al\left(OH\right)_3\downarrow+3NH_4Cl\)
Cho dd NH3 dư vào dd AlCl3 xuất hiện kết tủa trắng keo Al(OH)3
AlCl\(_3\) + 3NH\(_3\) + 3H\(_2\)O → Al(OH)\(_3\) + 3NH\(_4\)Cl