Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1.
a/ - Cho dd H2SO4 loãng t/d với Fe.
Fe + H2SO4 -> FeSO4 + H2O
=> H2SO4 có tính chất hóa học (tchh) của axit: t/d với KL đứng trước H sinh ra muối và khí H2.
- Cho dd H2SO4 l~t/d với CuO.
CuO + H2SO4 -> CuSO4 + H2O
=> H2SO4 có tchh của axit: t/d với oxit bazơ tạo ra muối và nước.
- Cho dd H2SO4 t/d với KOH.
2KOH + H2SO4 -> K2SO4 + 2H2O
=> H2SO4 có tchh của axit: t/d với dd kiềm cho ra muối và nước.
b/ - Cho H2SO4 đặc t/d với Cu.
Cu + 2H2SO4 đ --t*--> CuSO4 + SO2 + 2H2O
=> H2SO4 đặc có tchh riêng: t/d được với Cu, sinh ra khí SO2 (KL đứng sau H).
- Cho H2SO4 đặc t/d với Fe.
2Fe + 6H2SO4 đ --t*--> Fe2(SO4)3 + 6H2O + 3SO2
=> H2SO4 đặc có tchh riêng: t/d với KL sinh ra muối và giải phóng SO2; đẩy được Fe lên hóa trị cao nhất.
- Cho H2SO4 đặc vào C6H12O6.
C6H12O6 ----H2SO4 đ, t*---> 6C + 6H2O
=> H2SO4 đặc có tchh riêng: có tính háo nước.
2. Gọi số mol của CuO và ZnO lần lượt là a và b.
n HCl = Cm.V = 3.0,1 = 0,3 mol.
a/ CuO + 2HCl -> CuCl2 + H2O
_1_____2 (mol)
_a_____2a
ZnO + 2HCl -> ZnCl2 + H2O
_1______2 (mol)
_b_____2b
Theo đề bài, ta có hệ phương trình:
80a + 81b = 12,1 (m hh)
2a + 2b = 0,3 (n HCl)
Giải hệ, được: a = 0,05; b = 0,1.
b/ m CuO = n.M = 80a = 80.0,05 = 4 (g).
=> % mCuO = (mCuO / mhh) . 100% = 33,06 %.
=> % mZnO = 100% - 33,06% = 66,94 %.
c/ CuO + H2SO4 -> CuSO4 + H2O
___1______1 (mol)
___0,05__0,05
ZnO + H2SO4 -> ZnSO4 + H2O
_1_____1 (mol)
_0,1__0,1
Tổng số mol H2SO4 = 0,05 + 0,1 = 0,15 mol.
=> m H2SO4 = n.M = 0,15.98 = 14,7 g.
=> mdd H2SO4 = (mct.100%) / C% = (14,7.100)/20 = 73,5 g.

Có 3 yếu tố làm ảnh hưởng đến cân bằng hóa học
- Ảnh hưởng của nhiệt độ đến cân bằng hóa học
VD: N2(k) + 3H2(k) ⇔ 2NH3(k) ∆Ho = -92,6kJ.
Vì ∆H0 < 0, khi nhiệt độ tăng, cân bằng chuyển dịch theo chiều nghịch (chiều thu nhiệt), nếu nhiệt độ của hệ giảm xuống thì cân bằng chuyển dịch theo chiều thuận (chiều tỏa nhiệt).
- Ảnh hưởng của áp suất đến cân bằng hóa học
VD : N2(k) + 3H2(k) ⇔ 2NH3(k)
Có ∆n = 2 – (3 + 1) = -2
+ Nếu P tăng ⇒ cân bằng dịch chuyển theo chiều P giảm (giảm số mol khí ∆n < 0). => Cân bằng chuyển theo chiều thuận
+ Nếu P giảm ⇒cân bằng dịch chuyển theo chiều P tăng (tăng số mol khí ∆n > 0). => Cân bằng chuyển theo chiều nghịch
-Ảnh hưởng của nồng độ đến cân bằng hóa học
C(r)+CO2(k)⇌2CO(k)
- Khi tăng CO2 thì cân bằng chuyển dịch theo chiều thuận (chiều làm giảm CO2).
- Khi giảm CO2 thì cân bằng chuyển dịch theo chiều nghịch (chiều làm tăng CO2).

- Hóa học nghiên cứu về thành phần, cấu trúc, tính chất và sự biến đổi của chất cũng như ứng dụng của chúng.
- Vai trò của hóa học trong đời sống và sản xuất
+ Là nhiên liệu dùng cho động cơ đốt trong
+ Làm vật liệu xây dựng
+ Ngành y tế: thuốc phòng, chữa bệnh cho người, chỉ khâu tự tiêu dùng trong y khoa
+ Làm mĩ phẩm, phân bón cho cây trồng
+ Nghiên cứu trong phòng thí nghiệm
- Phương pháp học tập và nghiên cứu hóa học một cách hiệu quả
+ Phương pháp học tập: (1) Phương pháp tìm hiểu lí thuyết, (2) Phương pháp học tập thông qua thực hành thí nghiệm, (3) Phương pháp luyện tập, ôn tập, (4) Phương pháp học tập trải nghiệm
+ Phương pháp nghiên cứu hóa học: (1) Xác định vấn đề nghiên cứu, (2) Nêu giả thuyết khoa học, (3) Thực hiện nghiên cứu (lí thuyết, thực nghiệm, ứng dụng), (4) Viết báo cáo: thảo luận kết quả và kết luận vấn đề

Dung dịch H 2 SO 4 loãng có những tính chất hoá học chung của axit.
Thí nghiệm 1. Fe + H 2 SO 4
Thí nghiệm 2. ZnO + H 2 SO 4
Thí nghiệm 3. Na 2 SO 3 + H 2 SO 4
Thí nghiệm 4. NaOH + H 2 SO 4 (dùng giấy quỳ tím chứng minh có phản ứng hoá học xảy ra).

a) Phương trình hóa học: 2B + 3F2 → 2BF3
b) Trong phân tử BF3 có 2 liên kết đơn, 1 liên kết đôi (gồm 1 liên kết σ và 1 liên kết п)
=> Trong phân tử BF3 có 3 liên kết σ và 1 liên kết п

Dung dịch H 2 SO 4 đặc có những tính chất hoá học đặc trưng là tính oxi hoá mạnh và tính háo nước.
Thí nghiệm 5. H 2 SO 4 + Cu. Tính oxi hóa mạnh
Thí nghiệm 6. H 2 SO 4 đặc + C 12 H 22 O 11 . Tính háo nước và tính oxi hóa

Tính chất hóa học cơ bản của clo: Clo là chất oxi hóa mạnh.
- Tác dụng với kim loại : clo oxi hóa trực tiếp hầu hết các kim loại tạo muối clorua, phản ứng xảy ra ở nhiệt độ thường hoặc không cao lắm, tốc độ nhanh, tỏa nhiều nhiệt.
2Fe + 3Cl2 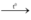 2FeCl3
2FeCl3
- Tác dụng với hiđro: Phản ứng xảy ra khi chiếu sáng bởi ánh sáng mặt trời:
H2 + Cl2 → 2HCl.
- Tác dụng với nước:
Trong phản ứng với nước, clo vừa là chất oxi hóa vừa là chất khử.
Cl2 + H2O ⇆ HCl + HClO
Sở dĩ có những tính chất hóa học cơ bản trên vì khi tham gia phản ứng, nguyên tử clo dễ nhận thêm 1 electron để thành ion Cl-. Vì vậy tính chất hóa học cơ bản của clo là tính oxi hóa mạnh.

Môn hóa học thuộc lĩnh vực khoa học tự nhiên, có sự kết hợp chặt chẽ giữa lí thuyết và thực nghiệm. Bên cạnh đó hóa học là cầu nối giữa các ngành khoa học tự nhiên khác như vật lí, sinh học, y dược, môi trường và địa chất học. Vì thế để việc học tập hóa học đạt hiệu quả cao nhất, em cần liên hệ nội dung bài học hóa học với nội dung những môn học khác cũng như các thí nghiệm, quá trình thực tiễn có liên quan.
Ví dụ: Liên hệ nội dung bài học về ảnh hưởng của chất xúc tác đến tốc độ phản ứng hóa học với sự phân hủy tinh bột trong nước bọt nhờ enzyme trong môn sinh học để giải thích vì sao chúng ta cần phải nhai kĩ thức ăn trước khi nuốt?
Giải thích: Enzyme amylase và lipase có trong nước bọt là chất xúc tác đẩy nhanh quá trình tiêu hóa tinh bột và chất béo. Khi nhai kĩ thức ăn được chia nhỏ hơn nhằm tăng diện tích tiếp xúc giữa thức ăn với các enzyme, khiến các phản ứng trong quá trình tiêu hóa chất béo và tinh bột xảy ra nhanh hơn, hiệu quả hơn.