Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Dung dịch H 2 SO 4 đặc có những tính chất hoá học đặc trưng là tính oxi hoá mạnh và tính háo nước.
Thí nghiệm 5. H 2 SO 4 + Cu. Tính oxi hóa mạnh
Thí nghiệm 6. H 2 SO 4 đặc + C 12 H 22 O 11 . Tính háo nước và tính oxi hóa

Dung dịch H 2 SO 4 loãng có những tính chất hoá học chung của axit.
Thí nghiệm 1. Fe + H 2 SO 4
Thí nghiệm 2. ZnO + H 2 SO 4
Thí nghiệm 3. Na 2 SO 3 + H 2 SO 4
Thí nghiệm 4. NaOH + H 2 SO 4 (dùng giấy quỳ tím chứng minh có phản ứng hoá học xảy ra).

1.
a/ - Cho dd H2SO4 loãng t/d với Fe.
Fe + H2SO4 -> FeSO4 + H2O
=> H2SO4 có tính chất hóa học (tchh) của axit: t/d với KL đứng trước H sinh ra muối và khí H2.
- Cho dd H2SO4 l~t/d với CuO.
CuO + H2SO4 -> CuSO4 + H2O
=> H2SO4 có tchh của axit: t/d với oxit bazơ tạo ra muối và nước.
- Cho dd H2SO4 t/d với KOH.
2KOH + H2SO4 -> K2SO4 + 2H2O
=> H2SO4 có tchh của axit: t/d với dd kiềm cho ra muối và nước.
b/ - Cho H2SO4 đặc t/d với Cu.
Cu + 2H2SO4 đ --t*--> CuSO4 + SO2 + 2H2O
=> H2SO4 đặc có tchh riêng: t/d được với Cu, sinh ra khí SO2 (KL đứng sau H).
- Cho H2SO4 đặc t/d với Fe.
2Fe + 6H2SO4 đ --t*--> Fe2(SO4)3 + 6H2O + 3SO2
=> H2SO4 đặc có tchh riêng: t/d với KL sinh ra muối và giải phóng SO2; đẩy được Fe lên hóa trị cao nhất.
- Cho H2SO4 đặc vào C6H12O6.
C6H12O6 ----H2SO4 đ, t*---> 6C + 6H2O
=> H2SO4 đặc có tchh riêng: có tính háo nước.
2. Gọi số mol của CuO và ZnO lần lượt là a và b.
n HCl = Cm.V = 3.0,1 = 0,3 mol.
a/ CuO + 2HCl -> CuCl2 + H2O
_1_____2 (mol)
_a_____2a
ZnO + 2HCl -> ZnCl2 + H2O
_1______2 (mol)
_b_____2b
Theo đề bài, ta có hệ phương trình:
80a + 81b = 12,1 (m hh)
2a + 2b = 0,3 (n HCl)
Giải hệ, được: a = 0,05; b = 0,1.
b/ m CuO = n.M = 80a = 80.0,05 = 4 (g).
=> % mCuO = (mCuO / mhh) . 100% = 33,06 %.
=> % mZnO = 100% - 33,06% = 66,94 %.
c/ CuO + H2SO4 -> CuSO4 + H2O
___1______1 (mol)
___0,05__0,05
ZnO + H2SO4 -> ZnSO4 + H2O
_1_____1 (mol)
_0,1__0,1
Tổng số mol H2SO4 = 0,05 + 0,1 = 0,15 mol.
=> m H2SO4 = n.M = 0,15.98 = 14,7 g.
=> mdd H2SO4 = (mct.100%) / C% = (14,7.100)/20 = 73,5 g.

Điều chế axit HCl từ NaCl, H2SO4 đặc, H2O:
NaCl + H2SO4 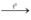 NaHSO4 + HCl
NaHSO4 + HCl
Hấp thụ khí hidro clorua vào nước được dung dịch axit HCl.
- Từ axit HCl và MnO2 điều chế Cl2:
MnO2 + 4HCl → MnCl2 + 2H2O + Cl2
- Từ Cl2 và dung dịch NaOH điều chế nước Gia – ven.
Cl2 + 2NaOH → NaCl + NaClO + H2O.

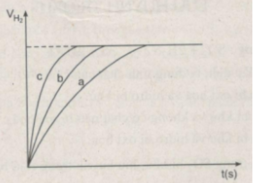
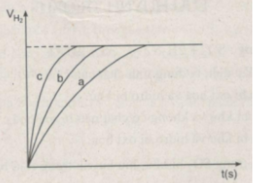
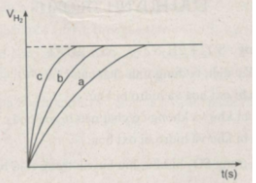
Đồ thị biểu diễn các phản ứng :
Đường cong c biểu diễn cho thí nghiệm 1, phản ứng xảy ra nhanh nhất
Đường cong b biểu diễn cho thí nghiệm 3, phản ứng xảy ra nhanh trung bình.
Đường cong a biểu diễn cho thí nghiệm 2, phản ứng xảy ra chậm nhất.

Thể tích khí hiđro :
Sau các thí nghiệm, kẽm còn dư. Như vậy, thể tích khí hiđro được sinh ra phụ thuộc vào lượng H 2 SO 4 tham gia phản ứng
n H 2 = n H 2 SO 4 = 2.50/1000 = 0,1 mol
Thể tích khí hiđro ở điều kiện phòng là :
V H 2 = 0,1 x 24 = 2,4l = 2400 cm 3
Ta ghi số 2400 cm 3 trên trục y, nơi giao điểm giữa trục y và đường ngang của 3 đường cong kéo dài (nét chấm trên đồ thị).

Đáp án B
Muốn pha loãng H2SO4 đặc, người ta phải cho từ từ axit vào nước và khuấy đều

Đáp án D
Muốn pha loãng H 2 SO 4 đặc, người ta rót từ từ axit vào nước và khuấy nhẹ bằng đũa thủy tinh mà không được làm ngược lại

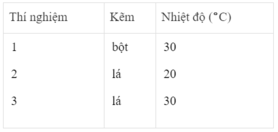
Nhận xét:
- Khí hiđro được giải phóng ở thí nghiệm 1 nhiều, nhanh hơn ở thí nghiệm 3. Vì diện tích tiếp xúc của Zn với H 2 SO 4 ở thí nghiệm 1 lớn hơn. trong khi đó nhiệt độ của dung dịch axit là như nhau.
- Khí hiđro được giải phóng ở thí nghiệm 3 nhiều, nhanh hơn ở thí nghiệm 2. Vì nhiệt độ của dung dịch H 2 SO 4 ở thí nghiệm 3 cao hơn, trong khi đó diện tích tiếp xúc giữa Zn và axit là như nhau.
1 đứa không tang được là ..........
là ..........
Để xác định nồng độ chính xác của 1 chất dựa vào 1 chất khác, đây được gọi là phương pháp "chuẩn độ".
- Dụng cụ: Bình tam giác, cốc, buret, công tơ hút, bình định mức.
(Bình định mức: bình biết rõ thể tích;
Buret:dụng cụ có thể cho một lượng chính xác thể tích của 1 dung dịch)
- Thiết bị: cân điện tử.
Cách tiến hành.
- B1: Cần 1 lượng chính xác NaOH rắn. Hoà tấn NaOH rắn vào cốc rồi chuyển vào bình định mức. Xác định chính xác nồng độ mol của dd NaOH trong bình định mức, kí hiệu aM. Cho dung dịch NaOH lên buret.
- B2: Lấy 1 lượng chính xác V ml dd H2SO4 cho vào bình tam giác, thêm 2 giọt chỉ thị quỳ tím. Dung dịch ban đầu có màu đỏ.
- B3: Chuẩn độ dung dịch H2SO4 bằng dung dịch NaOH. Thêm từ từ dung dịch NaOH trên buret xuống bình tam giác đến khi dung dịch trong bình tam giác chuyển sang màu tím, ghi lại giá trị thể tích NaOH đã dùng trên buret, kí hiệu V'.
- B4: Tính toán nồng dung dịch H2SO4
PTHH: H2SO4 + 2NaOH --> Na2SO4 + H2O
=> nH2SO4 = 1/2nNaOH
<=> CM(H2SO4)*V = 1/2*V'*a
<=> CM(H2SO4) = \(\dfrac{V'\times a}{2V}\)