Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Hiện tượng: Chất rắn màu trắng tan ra, tạo thành dung dịch
- Nhiệt độ chất lỏng trong cốc tăng lên, từ 20 oC lên 50 oC
- Giải thích: Sự hòa tan CaO trong nước sinh ra nhiệt, làm nhiệt độ chất lỏng trong cốc tăng lên

1.
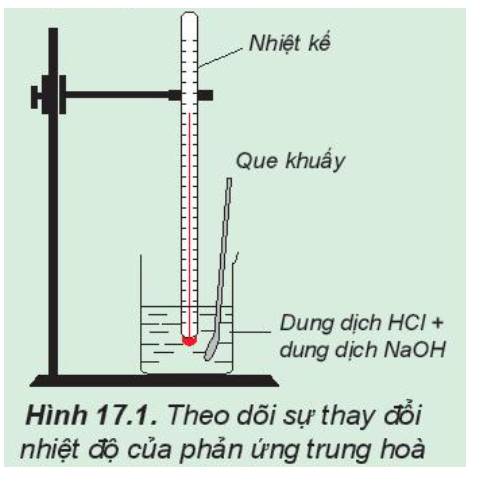
Phản ứng hóa học: NaOH + HCl → NaCl + H2O
Nhiệt độ đo được (HCl) lúc ban đầu thấp hơn so với nhiệt độ sau phản ứng
=> Phản ứng trung hòa là phản ứng tỏa nhiệt
2.
Trong thí nghiệm trên, nếu thay các dung dịch HCl và NaOH bằng các dung dịch loãng hơn thì nhiệt độ sau phản ứng vẫn tăng nhưng tăng ít hơn so với thí nghiệm trên.

Thí nghiệm 1:
2HCl + MgO → MgCl2 + H2O
=> Cốc thí nghiệm nguội dần ( HCl ban đầu hơi ấm) => Phản ứng thu nhiệt.
Thí nghiệm 2:
CH3COOH + NaHCO3 → CH3COONa + CO2 + H2O
=> Cốc thí nghiệm nóng lên => Phản ứng tỏa nhiệt.

Đáp án B
Tốc độ phản ứng tỷ lệ thuận với nồng độ của chất phản ứng: v = k A a * B b

Thể tích dung dịch Na2S2O3 càng nhiều => Nồng độ Na2S2O3 càng cao => Thời gian xuất hiện kết tủa càng nhanh

1. So sánh tính kim loại của sodium và magnesium
1. Phương trình hóa học2Na + 2H2O -> 2NaOH + H2
2. Ở điều kiện thường:
- Sodium phản ứng mãnh liệt với nước, tạo dung dịch màu hồng và tỏa nhiệt.
- Magnesium không phản ứng với nước.
2. So sánh tính phi kim của chlorine và iodine
- Hiện tượng: Dung dịch không màu chuyển thành màu nâu của Iodine
=> Cl đẩy được I ra khỏi dung dịch KI => Tính phi kim của iodine yếu hơn chlorine

9): n(CO2) = 4,48/22,4 = 0,2mol
Số mol mỗi chất trong hỗn hợp dung dịch ban đầu:
n(Na2CO3) = 0,5.0,2 = 0,1mol; n(NaOH) = 0,75.0,2 = 0,15mol
Khi cho CO2 vào dung dịch chứa Na2CO3 và NaOH thứ tự các phản ứng xảy ra:
2NaOH + CO2 → Na2CO3 + H2O
0,15 0,075 0,075
CO2 + Na2CO3 + H2O → 2NaHCO3
0,125 0,125 0,25
Số mol Na2CO3 có trong dung dịch X:
n(Na2CO3) = 0,1 + 0,075 - 0,125 = 0,05mol
Cho dung dịch BaCl2 dư vào dung dịch X:
Na2CO3 + BaCl2 → BaCO3 + 2NaCl
0,05 0,05
Khối lượng kết tủa thu được: m(BaCO3) = 0,05.197 = 9,85gam
1) Dung dịch A chứa CO32- (x mol) và HCO3- (y mol)
CO32- + H+ —> HCO3-
x…………x………….x
HCO3- + H+ —> CO2 + H2O
x+y…….0,15-x
Dung dịch B tạo kết tủa với Ba(OH)2 nên HCO3- dư, vậy nCO2 = 0,15 – x = 0,045 —> x = 0,105
HCO3- + OH- + Ba2+ —> BaCO3 + H2O
—> nBaCO3 = (x + y) – (0,15 – x) = 0,15 —> y = 0,09
—> m = 20,13 gam



Chọn A
Nồng độ các chất phản ứng ở cốc (1) lớn hơn ở cốc (2) → Thời gian xuất hiện kết tủa trắng đục của cốc (1) ít hơn cốc (2).