Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Thí nghiệm 1:
\(PTHH:Zn+2HCl--->ZnCl_2+H_2\)
Theo PT: \(n_{H_2}=\dfrac{1}{2}.n_{HCl}=\dfrac{1}{2}.0,2=0,1\left(mol\right)\)
\(\Rightarrow V_1=V_{H_2}=0,1.22,4=2,24\left(lít\right)\)
- Thí nghiệm 2:
Gọi x, y lần lượt là số mol của Na và Ca.
PTHH:
\(2Na+2HCl--->2NaCl+H_2\left(1\right)\)
\(Ca+2HCl--->CaCl_2+H_2\left(2\right)\)
Theo PT(1): \(n_{HCl}=n_{Na}=x\left(mol\right)\)
Theo PT(2): \(n_{HCl}=2.n_{Ca}=2y\left(mol\right)\)
\(\Rightarrow x+2y=0,1\) (*)
Theo đề, ta có: \(23x+40y=4,7\) (**)
Từ (*) và (**), ta có hệ phương trình:
\(\left\{{}\begin{matrix}x+2y=0,1\\23x+40y=4,7\end{matrix}\right.\)
Ra số âm, bạn xem lại đề.
1,Người ta thực hiện 2 thí nghiệm sau
Thí nghiệm 1 : | Hòa tan hoàn toàn 6,5g kẽm vào dung dịch axit có chứa 0,2 mol HCl, thu được V1 lit khí ( đktc )
|
Thí nghiệm 2 : | Hòa tan hoàn toàn 4,7g hỗn hợp 2 kim loại natri và canxi vào dung dịch có chứa 0,1 mol HCl thu được V2 lit khí ( đktc )
|

\(TN_1:n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\ PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ \text{Vì }\dfrac{n_{Zn}}{1}=\dfrac{n_{HCl}}{2}\text{ nên phản ứng xảy ra hoàn toàn}\\ \Rightarrow n_{H_2}=0,1\left(mol\right)\\ \Rightarrow V_1=V_{H_2\left(đktc\right)}=0,1\cdot22,4=2,24\left(l\right)\)
\(TN_2:\text{Đặt }\left\{{}\begin{matrix}x=n_{Na}\left(mol\right)\\y=n_{Ca}\left(mol\right)\end{matrix}\right.\\ PTHH:2Na+2HCl\rightarrow2NaCl+H_2\\ Ca+2HCl\rightarrow CaCl_2+H_2\\ \text{Từ đó ta có HPT: }\left\{{}\begin{matrix}23x+40y=4,7\\x+0,5y=0,1\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=\dfrac{11}{190}\\y=\dfrac{8}{95}\end{matrix}\right.\\ \Rightarrow n_{H_2}=\dfrac{1}{2}x+y=\dfrac{11}{380}+\dfrac{8}{95}\approx0,113\left(mol\right)\\ \Rightarrow V_2=V_{H_2\left(đktc\right)}\approx0,113\cdot22,4=2,5312\left(l\right)\\ \Rightarrow V_1< V_2\)

a) \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2--->0,4--->0,2--->0,2
=> V = 0,2.22,4 = 4,48 (l)
b) \(C_{M\left(dd.HCl\right)}=\dfrac{0,4}{0,5}=0,8M\)
c) \(m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)

Này tính số mol H2 bằng 1/2 số mol HCl rồi tính thể tích là được!

a) Lập công thức hóa học của muối kẽm clorua: Z n C l 2
b) Khối lượng muối Z n C l 2 = 6,5 + 7,3 – 0,2 = 13,6 (gam)
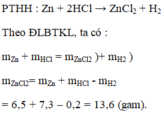
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\ n_{HCl}=0,2\left(mol\right)\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ V\text{ì}:\dfrac{0,1}{1}=\dfrac{0,2}{2}\\ \Rightarrow Ph\text{ả}n.\text{ứn}g.h\text{ết}\\ n_{H_2}=n_{Zn}=0,1\left(mol\right)\\ V_1=V_{H_2\left(\text{đ}ktc\right)}=0,1.22,4=2,24\left(l\right)\)