Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Mỗi năm cả thế giới cần đến hàng trăm triệu tấn sulfuric acid. Trong đó, gần \(50\%\) lượng acid được dùng để sản xuất phân bón như ammonium sulfate, calcium dihydrogenphosphate \(\left(Ca\left(H_2PO_4\right)_2\right),...\) Acid này còn được sử dụng trong sản xuất chất tẩy rửa, sơn, phẩm màu, thuốc trừ sâu, giấy, chế hoá dầu mỏ,…
Sulfuric acid là một hoá chất công nghiệp rất quan trọng, sản lượng sulfuric acid của mỗi quốc gia là một chỉ số tốt về sức mạnh công nghiệp của quốc gia đó vì thế sulfuric acid là hoá chất có tầm quan trọng bậc nhất.

- Tính chất của sulfuric acid loãng:
Dung dịch sulfuric acid loãng có đầy đủ tính chất của một acid mạnh:
+ Đổi màu quỳ tím thành đỏ.
+ Tác dụng với kim loại hoạt động trong dãy hoạt động hoá học.
+ Tác dụng với basic oxide và base.
+ Tác dụng với nhiều muối.
- Tính chất của sulfuric acid đặc: Ngoài tính acid, dung dịch sulfuric acid đặc còn có tính oxi hoá và tính háo nước.
- Cách bảo quản sulfuric acid:
+ Sulfuric acid được bảo quản trong chai, lọ có nút đậy chặt, đặt ở vị trí chắc chắn.
+ Đặt chai, lọ đựng dung dịch sulfuric acid đặc tránh xa các lọ chứa chất dễ gây cháy, nổ như chlorate, perchlorate, permanganate, dichromate.
- Cách sử dụng sulfuric acid để đảm bảo an toàn:
Sulfuric acid gây bỏng khi rơi vào da, do vậy cần tuân thủ các nguyên tắc:
(1) Sử dụng găng tay, đeo kính bảo hộ, mặc áo thí nghiệm.
(2) Cầm dụng cụ chắc chắn, thao tác cẩn thận.
(3) Không tì, đè chai đựng acid lên miệng cốc, ống đong khi rót acid.
(4) Sử dụng lượng acid vừa phải, lượng acid còn thừa phải thu hồi vào lọ đựng.
(5) Không được đổ nước vào dung dịch acid đặc.

Tham khảo:
a) 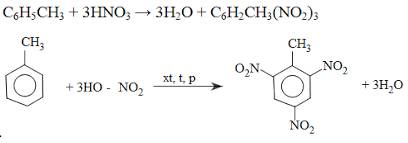
b) PTHH :
C6H5CH3 + 3HNO3 → C6H2(NO2)3CH3 + 3H2O
gam 92 227
kg 1000.62% x
Từ 1 tấn toluene có thể điều chế được số kilôgam 2,4,6-trinitrotoluene, biết hiệu suất của phản ứng là 62% là:
x = 1000*0,62.227 : 92 = 1530 kg

CTCT của acetic acid: \(CH_3-COOH\)
Một số tính chất hóa học:
- Hợp chất hữu cơ có tính axit mạnh, làm quỳ chuyển sang màu đỏ.
- Tác dụng được với kim loại trước H, oxit bazo, bazo, muối trung hòa, muối axit, rượu.
Ứng dụng của acetic acid:
- dung môi hòa tan các chất hóa học, sản xuất thuốc nhuộm, bảo quản thực phẩm...

CH3OH \(\underrightarrow{H_2SO_{4đ}}\) CH3-O-CH3 + H2O
2C2H5OH \(\underrightarrow{H_2SO_{4đ}}\) C2H5-O-C2H5 + H2O
CH3OH + C2H5OH\(\underrightarrow{H_2SO_{4đ}}\) CH3-O-C2H5 + H2O

- Trong Thí nghiệm 1, chất lỏng xuất hiện ở đáy cốc không phải là benzene (benzene không màu).
- Vì benzene phản ứng với dung dịch nitric acid tạo nitrobenzene có màu vàng nhạt .
PTHH: C6H6 + HNO3 → C6H5NO2 + H2O

(1) \(4FeS_2+11O_2\underrightarrow{t^o}2Fe_2O_3+8SO_2\)
(2) \(2SO_2+O_2\xrightarrow[_{V_2O_5}]{^{t^o}}2SO_3\)
(3) \(nSO_3+H_2SO_4\rightarrow H_2SO_4.nSO_3\)
(4) \(H_2SO_4.nSO_3+nH_2O\rightarrow\left(n+1\right)H_2SO_4\)
a) 4FeS2 + 11O2 → 2Fe2O3 +8SO2 (1)
Phản ứng (1) là phản ứng oxi hoá - khử; chất oxi hoá: O2; chất khử: FeS2
2SO2 + O2 →𝑡𝑜,𝑉2𝑂5 2SO3 (2)
Phản ứng (2) là phản ứng oxi hoá - khử; chất oxi hoá: O2; chất khử: SO2
SO3 + H2O → H2SO4 (3)
Phản ứng (3) không là phản ứng oxi hoá - khử
b) 1 tấn quặng chứa 60% FeS2 (M = 120 g/𝑚𝑜𝑙−1)
Số mol FeS2 trong 1 tấn quặng trên là: 106120.60100= 5000 mol
Sơ đồ phản ứng: FeS2 → 2SO2 → 2SO3 → 2H2SO4
Dựa trên sơ đồ có số mol H2SO4 là 2.5000 = 10 000 mol.
Khối lượng H2SO4 thu được là:
98 × 10 000 = 980 000 gam = 980 kg = 0,98 tấn.
Khối lượng H2SO4 98% thu được là: 0,9898.100=1tấn.
Do hiệu suất cả quá trình là 80% nên khối lượng H2SO4 98% thực tế thu được là:
1.80100=0,8 tấn.
c) Trong FeS2 nguyên tố S có số oxi hóa -1, đề xuất công thức cấu tạo là:

\({{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}{\rm{ = }}\frac{{\rm{6}}}{{{\rm{60}}}}{\rm{ = 0,1 (mol); }}{{\rm{n}}_{{{\rm{C}}_2}{{\rm{H}}_5}{\rm{OH}}}}{\rm{ = }}\frac{{{\rm{5,2}}}}{{46}}{\rm{ }} \approx {\rm{ 0,113 (mol)}}\)
Phương trình hóa học:
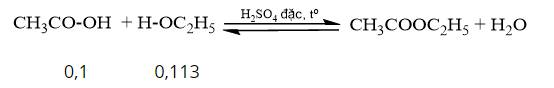
Ta có: \(\frac{{0,1}}{1} < \frac{{0,113}}{1}\) => acetic acid hết, ester tính theo acetic acid.
\(\begin{array}{l}{{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COO}}{{\rm{C}}_2}{{\rm{H}}_5}}}{\rm{ = }}{{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}{\rm{ = 0,1 (mol) }}\\ \Rightarrow {{\rm{m}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COO}}{{\rm{C}}_2}{{\rm{H}}_5}}} = {\rm{0,1}} \times {\rm{88 = 8,8 (g)}}\\ \Rightarrow {\rm{H = }}\frac{{5,28}}{{8,8}} \times 100\% = 60\% \end{array}\)

- Tính chất của sulfuric acid:
+ Tính chất vật lí: chất lỏng sánh như dầu, không màu, không bay hơi, nặng gần gấp hai lần nước (H2SO4 98% có khối lượng riêng là 1,84 g/mL),
+ Tính chất hóa học:
• Dung dịch sulfuric acid loãng là một trong các acid mạnh và có đầy đủ tính chất của acid:
Đổi màu quỳ tím thành đỏ.
Tác dụng với kim loại hoạt động trong dãy hoạt động hoá học.
Tác dụng với basic oxide và base.
Tác dụng với nhiều muối.
• Dung dịch sulfuric acid đặc có tính oxi hoá mạnh và tính háo nước.
- Ứng dụng: dùng trong sản xuất phân bón, thuốc trừ sâu, chất tẩy rửa tổng hợp, tơ sợi hoá học, chất dẻo, sơn màu,...