Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, mFe2(SO4)3= 55,97.2+ 3. (32+ 16.4) = 399,94 (g/mol )
=> tỉ lệ đồng vị của56Fe chứa trong muối sắt (III) sunfat Fe2(SO4)3 là
\(\dfrac{56.91,68}{399,94}\) . 100% = 12. 83%
b. mFe(OH)2= 55,97 + 2. (16+1) = 89,97 (g/ mol)
=> tỉ lệ đồng vị của 55Fe chứa trong muối sắt (II) hidroxit Fe(OH)2 là
\(\dfrac{55.5,84}{89,97}\) .100% = 3,57%
Giúp mình với ạ ! Ghi cụ thể hộ mình luôn nhea ! Thân !

Đáp án A
• Khối lượng nguyên tử trung bình của Fe là
MFe = 0,058 x 54 + 0,9172 x 56 + 0,022 x 57 + 0,0028 x 58 = 55,9116.
Khối lượng trung bình của Br là
MBr = 0,5069 x 79 + 0,4931 x 81 = 79,9862.
Phần trăm khối lượng của 56Fe trong FeBr3 là
![]()

Đáp án C
Gọi phần trăm khối lượng của đồng vị 55Fe, 56Fe lần lượt là x, y
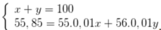
=>

ChọnC
Nguyên tử khối trung bình của Cl là :
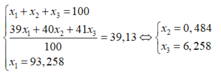
Giả sử có 1 mol K C l O 4 → Số mol Cl = 1; số mol C 35 l là 0,75.
Phần trăm khối lượng của C 35 l trong K C l O 4 là
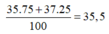

\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\\ n_{HCl}=\dfrac{73.10\%}{36,5}=0,2\left(mol\right)\\ Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\\ Vì:\dfrac{0,1}{1}>\dfrac{0,2}{6}\\ \Rightarrow Fe_2O_3dư\\ a.Muối.tạo.thành:FeCl_3\\ n_{FeCl_3}=\dfrac{2}{6}.0,2=\dfrac{1}{15}\left(mol\right)\\ m_{FeCl_3}=\dfrac{1}{15}.162,5=\dfrac{65}{6}\left(g\right)\\ b.Chất.tan.ddA:FeCl_3\\ m_{ddFeCl_3}=m_{Fe_2O_3\left(p.ứ\right)}+m_{ddHCl}=\dfrac{1}{6}.0,2.160+73=\dfrac{235}{3}\left(g\right)\\ C\%_{ddFeCl_3}=\dfrac{\dfrac{65}{6}}{\dfrac{235}{3}}.100=13,83\%\)

mHCl = \(\dfrac{146.20\%}{100\%}\)= 29,2 (g)
=> nHCl = \(\dfrac{29,2}{36,5}\)= 0,8 (mol)
Gọi x,y lần lượt là số mol của Fe2O3, MgO
Fe2O3 + 6HCl ----> 2FeCl3 + 3H2O
x 6x 2x 3x (mol)
MgO + 2HCl ----> MgCl2 + H2O
y 2y y y (mol)
Theo PT, ta có:
6x + 2y = 0,8
160x + 40y = 18
=> x = 0,05
y = 0,25
=> mFe2O3 = 0,05.160 = 8 (g)
=> %Fe2O3 = \(\dfrac{8.100\%}{18}\)= 44,4%
=> % MgO = 100 - 44,4 = 55,6%
b,
mdd sau phản ứng = 18 + 146 = 164 (g)
mFeCl3 = 0,1.162,5 = 16,25 (g)
mMgCl2 = 0,25.95 = 23,75 (g)
=> %FeCl3 = \(\dfrac{16,25.100\%}{164}\)= 10%
=> %MgCl2 = \(\dfrac{23,75.100\%}{164}\)= 14,48%

Đáp án C
Gọi x là phần trăm số nguyên tử 35Cl => Phần trăm số nguyên tử 37Cl là (100 – x)


a,\(3Fe+2O_2\rightarrow Fe_3O_4\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Fe_3O_4+8HCl\rightarrow2FeCl_3+FeCl_2+4H_2O\)
\(n_{H2}=\frac{0,448}{22,4}=0,02\left(mol\right)\)
\(\Rightarrow n_{Fe}=n_{H2}=0,02\left(mol\right)\)
\(\Rightarrow\%_{Fe}=\frac{6,72-0,02.56}{6,72}.100\%=83,33\%\)
b,\(n_{Fe3O4}=\frac{1}{30}\left(mol\right)\)
\(m_{FeCl3}=\frac{1}{15}.162,5=10,83\left(g\right)\)
\(\Rightarrow m_{FeCl2}=\left(\frac{1}{30}+0,02\right).127=6,773\left(g\right)\)
\(\overline{Fe}=\dfrac{5,84.55+56.91,68+57.2,17+58.0,31}{100}=55,9695\)
%56Fe trong oxit sắt từ Fe3O4 là
\(\%^{56}Fe=\dfrac{56.3.91,68\%}{55,9695.3+16.4}.100=65,42\%\)