Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
nH2SO4 = 0,18(mol)
Đặt x, y,z là số mol Fe(NO3)2, FeCO3 và Fe(OH)2
Các phản ứng trao đổi xảy ra
H+ + OH- → H2O (1)
2H+ + CO32- → CO2 ↑+ H2O (2)
Các bán phản ứng oxi hóa khử xảy ra:
Fe2+ → Fe3+ +1e (3)
4H+ + NO3- +3e → NO + 2H2O (4)
Bảo toàn electron: ne ( Fe2+ nhường) = ne ( N+5 nhận)
=> x + y + z = 2x (*)
Bảo toàn nguyên tố H: ∑ nH+ (1)+(2)+(4) = nOH- + 2nCO32- + 4nNO
=> 2z + 2y + 4nNO = 0,18.2
=> nNO = 0,09 – ( y + z)/2
Bảo toàn nguyên tố N: => nNO3- trong muối = 2nFe(NO3)2 – nNO = 2x – 0,09 + (y+z)/2
mmuối = 56 ( x+ y + z) + 0,18.96 + 62[ 2x – 0,09 + (y+z)/2] = 38,4 (**)
Từ (*) và (**) => x = y + z = 0,1
=> a = 2x + y + z = 0,3

Đáp án C
Sơ đồ quá trình:
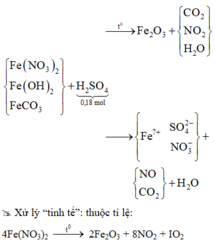
Vì nung X trong chân không, Y không chứa O2 chứng tỏ toàn bộ lượng O2 sinh ra này đã phản ứng ”vừa đẹp” với lượng FeO do nung Fe(OH)2 và FeCO3: 4FeO + IO2 → t ° 2Fe2O3.
Theo đó, gọi số mol Fe(NO3)2 trong X là 2x mol thì tương ứng hỗn hợp X có 4x mol.
“Tinh tế” tiếp, rút gọn thí nghiệm 2:
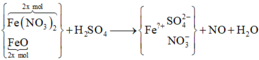
Ghép cụm NO3 hoặc bảo toàn electron mở rộng đều tìm ra ngay:


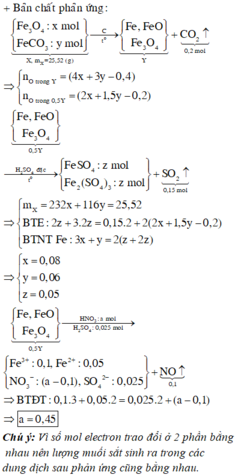
Quy đổi Y thành Fe và O ta có sơ đồ:
Sơ đồ ta có:
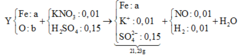
+ Bảo toàn khối lượng muối ta có nFe = a = 0,115 mol.
+ PT theo H+: 0,3 = 2nO + 4nNO + 2nH2.
⇒ nO = 0,12 mol.
● Quy đổi X thành Fe, NO3 và CO3 ta có:
Nung X ta có sơ đồ:
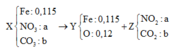
+ Từ MZ = 45 ⇒ nNO2 = nCO2
Û a = b Û a – b = 0 (1)
⇒ Bảo toàn oxi ta có: a + b = 0,12 mol (2)
+ Giải hệ (1) và (2) ⇒ nNO3 = nCO3 = 0,06 mol.
⇒ m = 0,115×56 + 0,06×(62+60) = 13,76
Đáp án A

Đáp án D
Hỗn hợp khí có M = 2.8 = 16
=> có H2 và NO
=> nH2 = nNO, vì có H2
=> 0,01 mol KNO3 hết cho 0,01 mol NO
=> nH2 = 0,01
Trong muối có:
Fe x mol, K+ 0,01 mol, SO4 2- 0,15 mol
m Muối = 56x + 39.0,01 + 96.0,15 = 21,23
=> x = 0,115
=> mFe = 6,44
=> Khí Z gồm NO2 và CO2 có M = 45
=> nNO2 = nCO2 = a
=> trong X có: Fe 0,115 mol, NO3- a mol , CO32- a mol
=> nO = 6a mol ( bảo toàn mol O trong CO3 và NO3)
=> trong Y có 0,115 mol Fe và 2a mol O ( giảm 4a do tạo khí NO2 và CO2)
NO3-+3e+4 H+->NO + 2 H2O
0,01 0,04 0,01
2 H+ + 2e -> H2
0,02 0,01
2 H+ + O -> H2O
4a 2a
nH+ = 0,04 + 0,02 + 4a = 2.0,15
=> a = 0,06
m X = mFe + mNO3 + mCO3
= 6,44 + 62.0,06 + 60.0,06
= 13,76



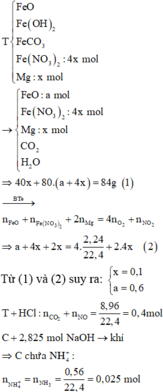


nH2SO4 = 0,18(mol)
Đặt x, y,z là số mol Fe(NO3)2, FeCO3 và Fe(OH)2
Các phản ứng trao đổi xảy ra
H+ + OH- → H2O (1)
2H+ + CO32- → CO2 ↑+ H2O (2)
Các bán phản ứng oxi hóa khử xảy ra:
Fe2+ → Fe3+ +1e (3)
4H+ + NO3- +3e → NO + 2H2O (4)
Bảo toàn electron: ne ( Fe2+ nhường) = ne ( N+5 nhận)
=> x + y + z = 2x (*)
Bảo toàn nguyên tố H: ∑ nH+ (1)+(2)+(4) = nOH- + 2nCO32- + 4nNO
=> 2z + 2y + 4nNO = 0,18.2
=> nNO = 0,09 – ( y + z)/2
Bảo toàn nguyên tố N: => nNO3- trong muối = 2nFe(NO3)2 – nNO = 2x – 0,09 + (y+z)/2
mmuối = 56 ( x+ y + z) + 0,18.96 + 62[ 2x – 0,09 + (y+z)/2] = 38,4 (**)
Từ (*) và (**) => x = y + z = 0,1
=> a = 2x + y + z = 0,3
Đáp án C