Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b: \(n_{H2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(\Leftrightarrow n_{Al}=0.1\left(mol\right)\)
\(m_{Al}=n_{Al}\cdot M_{Al}=0.1\cdot27=2.7\left(g\right)\)

a) \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PTHH: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,2--->0,3-------->0,1----------->0,3
b) `V_{H_2} = 0,3.22,4 = 6,72 (l)`
c) `m_{H_2SO_4} = 0,3.98 = 29,4 9g)`
d) \(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
PTHH: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
Xét tỉ lệ: 0,2 < 0,3 => H2 dư

a) 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
b) nH2 =\(\dfrac{26,88}{22,4}\)=1,2 mol
Theo tỉ lệ phản ứng => nAl phản ứng = \(\dfrac{nH_2.2}{3}\)= 0,8 mol
=> mAl phản ứng = 0,8.27= 21,6 gam
c) nAl2(SO4)3 = 1/2 nAl = 0,4 mol
=> m Al2(SO4)3 = 0,4. 342 = 136,8 gam
a) 2Al+3H2SO4⟶Al2(SO4)3+3H2↑2Al+3H2SO4⟶Al2(SO4)3+3H2↑
b) mAl=21,6gmAl=21,6g
c) mAl2(SO4)3=136,8gmAl2(SO4)3=136,8g
Giải thích các bước giải:
a) Phương trình hoá học:
2Al+3H2SO4⟶Al2(SO4)3+3H2↑2Al+3H2SO4⟶Al2(SO4)3+3H2↑
b) Số mol H2H2 sinh ra sau phản ứng:
nH2=VH222,4=26,8822,4=1,2molnH2=VH222,4=26,8822,4=1,2mol
Dựa vào phương trình hóa học ta được:
nAl=23nH2=23⋅1,2=0,8molnAl=23nH2=23⋅1,2=0,8mol
Khối lượng AlAl tham gia phản ứng:
mAl=nAl.MAl=0,8.27=21,6gmAl=nAl.MAl=0,8.27=21,6g
c) Dựa vào phương trình hóa học ta được:
nAl2(SO4)3=13nH2=13⋅1,2=0,4molnAl2(SO4)3=13nH2=13⋅1,2=0,4mol
Khối lượng muối tạo thành:
mAl2(SO4)3=nAl2(SO4)3.MAl2(SO4)3=0,4.342=136,8gmAl2(SO4)3=nAl2(SO4)3.MAl2(SO4)3=0,4.342=136,8g

a) \(PTHH:2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b) Theo định luật bảo toàn khối lượng, ta có:
\(m_{Al}+m_{H_2SO_4}=m_{Al_2\left(SO_4\right)_3}+m_{H_2}\\ \Rightarrow27+m_{H_2SO_4}=171+3\\ \Rightarrow m_{H_2SO_4}=171+3-27=147\left(g\right)\)

Phương trình hóa học của phản ứng:
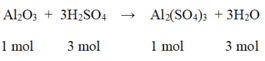
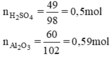
So sánh tỉ lệ 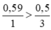 → Vậy Al2O3 dư
→ Vậy Al2O3 dư
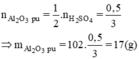
mAl2O3 (dư) = 60 - 17 = 43(g)
CHÚC BẠN HỌC TỐT!

Theo đề ra, ta có: \(n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
PTHH: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
pư...........0,3........0,45...................0,15.............0,45 (mol)
a) \(V_{H2}=22,4.0,45=10,08\left(l\right)\)
b) \(m_{H2SO4}=98.0,45=44,1\left(g\right)\)
c) Cách 1: \(m_{Al2\left(SO4\right)3}=342.0,15=51,3\left(g\right)\)
Cách 2: ADĐLBTKL, ta có:
\(m_{Al}+m_{H2SO4}=m_{Al2\left(SO4\right)3}+m_{H2}\)
\(\Rightarrow m_{Al2\left(SO4\right)3}=m_{Al}+m_{H2SO4}-m_{H2}\)
\(\Rightarrow27.0,3+44,1-2.0,45=51,3\left(g\right)\)
Vậy.......
nAl=\(\dfrac{8,1}{27}=0,3\left(mol\right)\)
nH2CO4=\(\dfrac{3}{2}\)nAl =>nH2CO4=0,45 (mol)
nAl2(SO4)3=>\(\dfrac{1}{2}\)nAl=0,15 (mol)
nH2=\(\dfrac{3}{2}\)nAl => nH2=0,45(mol)
PƯ: 2Al+3H2CO4 -> Al2(SO4)3+3H2
2 mol-----3 mol--------1 mol---------3mol
0,3 --------0,45----------0,15----------0,45
a,VH2=22,4.0,45=10,08(l)
b,m H2CO4= 0,45 . 98=44,1(g)
c,C1: mAl2(SO4)3=0,15.342=51,03(g)
C2: mAl+mH2CO4 -> mAl2(SO4)3+mH2
=>mAl2(SO4)3=mAl+mH2CO4 -mH2
=>mAl2(SO4)3=0,3.27+0,45.98-0,45.2
=>mAl2(SO4)3=8,1+35,1-0,9=51,3(g)