Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

TL:
Cấu hình electron đầy đủ của X: 1s22s22p63s23p31s22s22p63s23p3
→ X ở ô thứ 15 (z = 15), X là một phi kim (do có 5 electron lớp ngoài cùng), nguyên tử X có 9 electron p (6e trên phân lớp 2p; 3e trên phân lớp 3p)
→ Nguyên tử của nguyên tố X có 5 phân lớp: 1s, 2s, 2p, 3s, 3p.
( mk ko chép mạng nhé )
HT

Đáp án D
Xét đáp án A.
a = 0 → Cấu hình electron của nguyên tố X: [khí hiếm]ns1
X có số lớp electron = n → X thuộc chu kì n.
X có 1 electron hóa trị, electron cuối cùng điền vào phân lớp ns → X thuộc nhóm IA.
• Xét đáp án B.
a = 5 → Cấu hình electron của nguyên tố X: [khí hiếm](n - 1)d5ns1
X có số lớp electron = n → X thuộc chu kì n.
X có 6 electron hóa trị, electron cuối cùng điền vào phân lớp (n - 1)d → X thuộc nhóm VIB.
• Xét đáp án C.
a = 10 → Cấu hình electron của nguyên tố X: [khí hiếm](n - 1)d10ns1
X có số lớp electron = n → X thuộc chu kì n.
X có 1 electron hóa trị, electron cuối cùng điền vào phân lớp (n - 1)d → X thuộc nhóm IB.
→ Chọn D.

Nhận thấy hợp chất A có dạng X2Y.
Dễ nhận thấy X+ trong tất cả các đáp án là NH4+ hoặc lập luận như sau:
• Với ion X+ chứa 5 hạt nhân của 2 nguyên tố → X có dạng AaBb+ với a+ b = 5
Trong X+ có 10 electron → Ztb =
10
+
1
5
= 2,2 → trong X chắc chắn chứa H → X có dạng HaBb
Với a = 1, b= 4 → ZB =
11
-
1
4
= 2,5 loại
Với a = 2, b= 3 → ZB =
11
-
2
3
= 3 ( loại do B(Z= 3) không tạo được liên kết ion với H)
Với a = 3, b= 2 → ZB =
11
-
3
2
= 4 ( Loại do không tồn tại ion C2H3+)
Với a= 4, b= 1 → ZB =
11
-
4
1
= 7 (N) → X là NH4+ ( thỏa mãn)
•Trong ion Y2- có bốn hạt nhân → Y có dạng CcDd với c + d= 4 ( Loại C, D)
Trong ion Y2- có bốn hạt nhân thuộc hai nguyên tố trong cùng một chu kì và đứng cách một ô trong bảng hệ thống tuần hoàn. → ZD = ZC + 2
Với c=1, d= 3 → ZC + 3. (ZC +2) = 30 → ZC = 6 ( C) → ZD = 8(O). Vậy Y2- có công thức CO32-.
Với c= 2,d= 2 → 2ZC + 2. (ZC +2) = 30 → ZC = 6,5 ( loại)
Với c= 3, d= 1→ 3ZC + (ZC +2) = 30 → ZC = 7 (N), ZD = 9 (F) → loại do không tạo được ion N3F2-.
Công thức của A là (NH4)2CO3.
Đáp án A.

1. Cấu hình electron của ion nào dưới đây giống khí hiếm? (Biết: 13Al; 26Fe; 29Cu; 30Zn).
A. Zn2+. B. Fe3+. C. Al3+.(1s22s22p6 ) D. Cu2+.
2. Nguyên tử của nguyên tố X tạo ra ion X3-. Tổng số hạt (p, n, e) trong X3- bằng 49, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 17. Số nơtron của ion X3- là
A. 15. B. 18. C. 16. D. 17.
Gọi các hạt proton, nơtron và electron trong X lần lượt là p, n và e
Tổng số các loại hạt proton, nơtron và electron của X3- là 49
p+ n + e +3 = 49 hay 2p + n = 46 (1)
Tổng số hạt mang điện nhiều hơn hạt không mang điện là 17
p + e + 3 – n = 17 hay 2p -n = 14 (2)
Từ (1), (2) ta có p = e = 15, n =16
Vậy X là photpho.

ZX= 2+2+3=7 ; Cấu hình e ngoài cùng: 2s2 2p3
X thuộc ô số 7, là nguyên tố Nito (N), chu kì 2, nhóm VA
Vì X có 5e ngoài cùng nên X là phi kim

Cấu hình e đầy đủ của X : 1 s 2 2 s 2 2 p 6 3 s 2 3 p 1 → Z = 13 = STT, chu kì 3 (có 3 lớp e), nhóm IIIA, (có 3 lớp ngoài cùng, là nguyên tố p), kim loại.v

Đáp án D
Hợp chất Y được cấu tạo từ ion M+ và ion X- Hợp chất Y là MX
Theo giả thiết ta có:
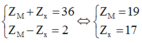
=> M là Kali và X là Cl
K có cấu hình electron là: 1s22s22p63s23p64s1
=> K thuộc chu kì 4; nhóm IA
Cl có cấu hình electron là: 1s22s22p63s23p5
=> Cl thuộc chu kì 3; nhóm VIIA
D
Cấu hình electron nguyên tử X: [ N e ] 3 s 2 3 p 4 .
X có 6 electron lớp ngoài cùng, để đạt cấu hình electron bền vững của khí hiếm, X có xu hướng nhận thêm 2electron.
X + 2 e → X 2 - .