
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


-Sơ đồ phản ứng: \(Al+O_2-->^{t^0}Al_2O_3\).
-Thêm hệ số 2 trước Al2O3 làm chẵn (nguyên tố nào là phi kim mà có chỉ số nguyên tố lẻ thì làm chẵn).
-6 chia 2 bằng 3, ghi hệ số 3 trước O2.
-4 chia 1 bằng 4, ghi hệ số 4 trước Al.
-Vì Al tác dụng với oxi ở nhiệt độ cao nên bị oxi hóa.

\(a,m_{CaCO_3}=m_{CO_2}+m_{CaO}\\ b,m_{CO_2}=m_{CaCO_3}-m_{CaO}=10,2-9=1,2(g)\\ \Rightarrow n_{CO_2}=\dfrac{1,2}{44}=\dfrac{3}{110}(mol)\\ \Rightarrow V_{CO_2(25^oC,1bar)}=\dfrac{3}{110}.24,79=0,676(l)\)

đề thi đou phải mỗi cân bằng , hóa 8 coi tính số mol , số gam chất dư kỹ vào á với chất nào không td chất nào á.



a. \(n_{Fe}=\dfrac{5.6}{56}=0,1\left(mol\right)\)
PTHH : 3Fe + 2O2 ----to----> Fe3O4
0,1 \(\dfrac{0.2}{3}\) \(\dfrac{0.1}{3}\)
b. \(m_{Fe_3O_4}=\dfrac{0.1}{3}.232=\dfrac{23.2}{3}\left(g\right)\)
c. \(V_{O_2}=\dfrac{0.2}{3}.22,4=\dfrac{4.48}{3}\left(l\right)\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(nFe=\dfrac{5,6}{56}=0,1\left(mol\right)\)
\(\Rightarrow nFe_3O_4=\dfrac{1}{3}.nFe=\dfrac{1}{3}.0,1=0,03\left(mol\right)\)
\(mFe_3O_4=0,03.232=6,96\left(g\right)\)
\(nO_2=\dfrac{2}{3}.nFe=\dfrac{2}{3}.0,1=0,07\left(mol\right)\)
\(VO_2=0,07.22,4=1,568\left(lít\right)\)

â) 4P +5 O2 -to-> 2 P2O5
b) nO2=5,6/22,4=0,25(mol)
=>nP=0,25 x 4/5 =0,2(mol)
=>mP=0,2.31=6,2(g)
c) nP=15,5/31=0,5(mol)
Ta có: 0,5/4 > 0,25/5
-> P dư, O2 hết, tính theo nO2.
=> nP2O5=2/5. 0,25=0,1(mol
=>mP2O5=142.0,1=14,2(g)

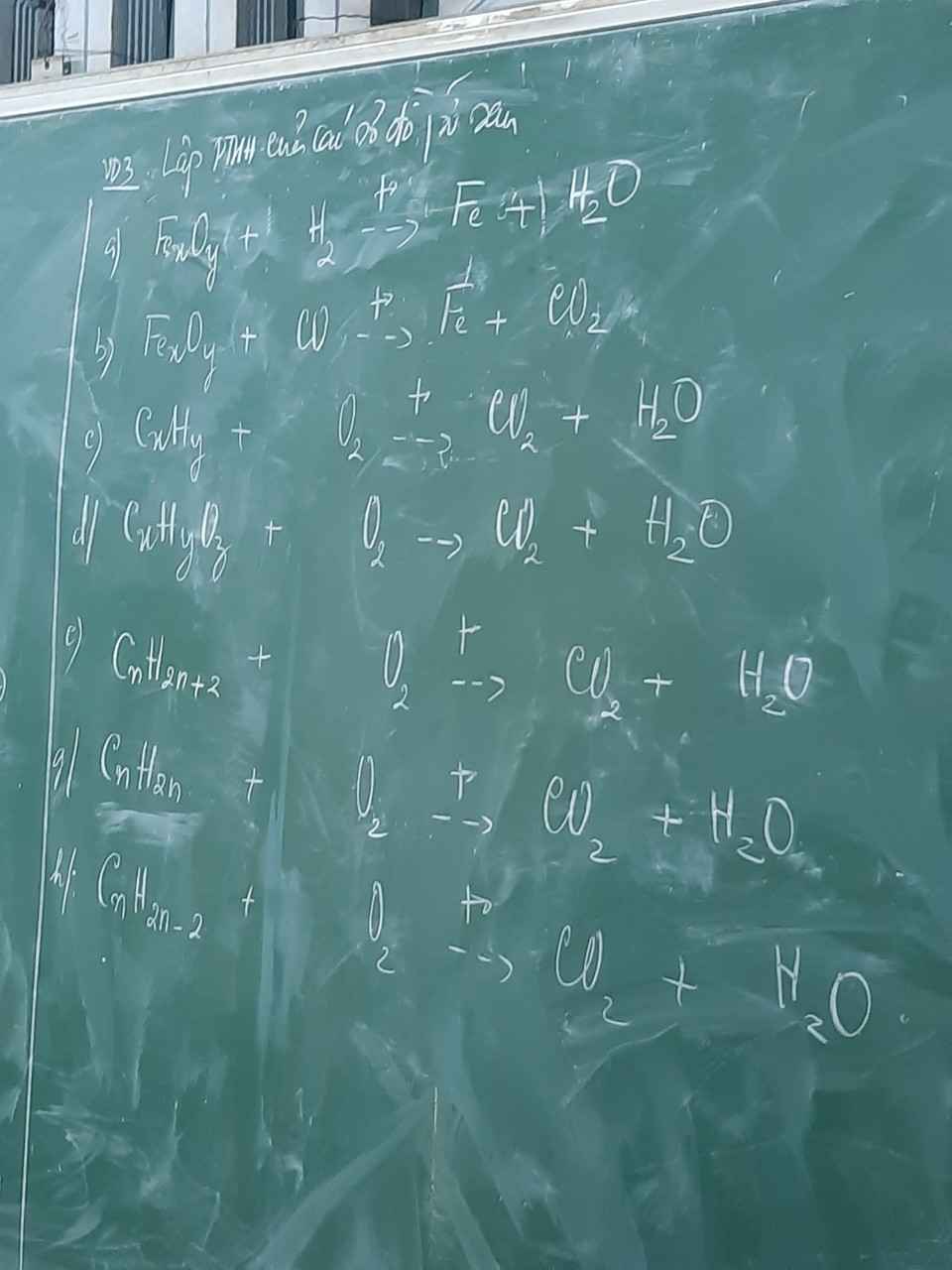

Tìm hệ số thích hợp sao cho số nguyên tử của mỗi nguyên tố hai bên bằng nhau
Thật ra anh nghĩ học căn bản thì đầu tiên:
- Em nắm chắc được các CTHH, biết CTHH nào tồn tại, CTHH nào không tồn tại. (Tránh trường hợp sáng tạo chất mới thành nhà phát minh vĩ đại của thế kỉ đấy)
- Sau đó em nắm chắc những mẹo để làm. VD như PTHH khử oxit kim loại với CO, H2 thì hệ số trước CO2, CO, H2O, H2 bằng chỉ số của O trong oxit, hệ số của kim loại bằng chỉ số của kim loại trong oxit. Rồi nhiều mẹo nữa.
- Sau này lên trên C3 em còn học thăng bằng electron, kĩ thuật hệ pt 4 ẩn cân bằng những pt 2 chất tg 2 chất sp đơn giản,..
- Chú ý là thà cân bằng sai còn hơn viết sai chất tham gia hay sp nhé!
Cố lên nào