Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Xét TN2: nH2= 0,2(mol)
PT: Fe + 2HCl -> FeCl2 + H2
=> nFe = nH2 = 0,2 (mol)=> nFe2O3 = 1/2nFe=0,1(mol)
=> mFe2O3 = 0,1.160=16(g)
=> mAl=42,8(g)
b) mFe = n.M = 0,2.56=11,2(g)
=> %mFe=19,05%
=> %mAl2O3 = 80,95%

a)
2Al + 6HCl → 2AlCl3 + 3H2↑
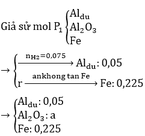
Pt: 2Al + 6H2SO4 → Al2(SO4)3 + 3SO2↑ + 6H2O
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Giả sử P2 = kP1
=> a=0.1
=> m = 128,8g
b)
2yAl + 3FexOy → yAl2O3 + 3xFe
0,1 0,225
=> 0,225y = 0,3x => 3y = 4x
=> Fe3O4

2Al + F e 2 O 3 → A l 2 O 3 + 2Fe
n H 2 (p1) = 3,08/22,4 = 0,1375 mol
n H 2 (p2) = 0,84/22,4 = 0,0375 mol
Thấy phần 2 tác dụng với NaOH sinh ra khí, suy ra sản phẩm có Al dư.
Vậy rắn Y gồm A l 2 O 3 , Fe và Al dư.
Phần 2:
2Al + 2NaOH + 2 H 2 O
→ 2 N a A l O 2 + 3 H 2
Theo PTPU ta có:
n A l (p2) = 2/3 n H 2 (p2)
= 2/3 . 0,0375 = 0,025 mol
⇒ n A l (p1) = n A l (p2) = 0,025 mol
Phần 1:
Fe + H 2 S O 4 → F e S O 4 + H 2 (*)
2Al + 3 H 2 S O 4
→ A l 2 S O 4 3 + 3 H 2 (**)
Theo (**) ta có:
n H 2 (**) = 3/2 n A l (p1)
= 3/2 . 0,025 = 0,0375 mol
⇒ n H 2 (*) = n H 2 (p1) - n H 2 (**)
= 0,1375 - 0,0375 = 0,1 mol
⇒ n F e (p1) = n H 2 (*)=0,1 mol
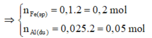
⇒ n A l pư = n F e sp = 0,2 mol
⇒ n F e 2 O 3 = 1/2 . n F e sp
= 1/2 . 0,2 = 0,1 mol
m h h = m F e 2 O 3 + m A l p u + m A l d u
= 0,1.160+0,05.27+0,2.27=22,75g
⇒ Chọn D.

PTHH: 3Fe3O4 + 8Al --to--> 4Al2O3 + 9Fe
=> \(\dfrac{n_{Fe}}{n_{Al_2O_3}}=\dfrac{9}{4}\)
P1: Gọi (nAl; nFe; nAl2O3) = (a;b;c)
PTHH: 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,04<---------------------------------0,06
=> a = 0,04 (mol)
Chất rắn không tan là Fe
\(b=\dfrac{20,16}{56}=0,36\left(mol\right)\)
Có: \(\dfrac{n_{Fe}}{n_{Al_2O_3}}=\dfrac{b}{c}=\dfrac{9}{4}\) => c = 0,16 (mol)
P2: Gọi (nAl; nFe; nAl2O3) = (ak;bk;ck)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
ak------------------>1,5ak
Fe + 2HCl --> FeCl2 + H2
bk------------------>bk
=> 1,5ak + bk = 0,63
=> k = 1,5
Bảo toàn Fe: \(n_{Fe_3O_4\left(X\right)}=\dfrac{b+bk}{3}=\dfrac{0,36+0,36.1,5}{3}=0,3\left(mol\right)\)
Bảo toàn Al: \(n_{Al\left(X\right)}=a+2c+ak+2ck=0,9\left(mol\right)\)
\(\left\{{}\begin{matrix}\%m_{Fe_3O_4}=\dfrac{0,3.232}{0,3.232+0,9.27}.100\%=74,12\%\\\%m_{Al}=\dfrac{0,9.27}{0,3.232+0,9.27}.100\%=25,88\%\end{matrix}\right.\)

Phần 2: do tác dụng với NaOH dư sinh ra H2 => Al dư
n H2 = 0,84 / 22,4 = 0,0375
Al + NaOH + H2O = NaAlO2 + 3/2 H2
0,025....................................
=> n Al dư = 0,025
Phần 1: n H2 = 3,08 / 22,4 = 0,1375
Al + 3H2SO4 = Al2(SO4)3 + 3H2
0,025_________________0,075
Fe + H2SO4 = FeSO4 + H2
0,0625..........................0,0625
* n Al2O3 = n Fe = 0,0625 => n Al phản ứng = 0,125
=> n Al = 0,125 + 0,025 = 0,15 => m Al = 4,05 (g)
* n Fe2O3 = n Fe/2 = 0,03125 => m Fe2O3 = 5 (g)
=> m hh = 2(m Fe + m Al) = 2(5 + 4,05) = 18,1 (g)
\(2Al+Fe_2O_3\rightarrow2Fe+Al_2O_3\)
Vậy chất rắn Y là \(Al_2O_3\) ;Fe và Al dư
Phần 1 \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\) (1)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\) (2)
\(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\) (3)
\(n_{H_2}=0,1375\left(mol\right)\)
Phần 2 \(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O\) (4)
\(2Al+2H_2O+2NaOH\rightarrow2NaAlO_2+H_2\uparrow\) (5)
\(n_{H_2}=\dfrac{0,84}{22,4}=0,0375\left(mol\right)\)
Theo (5) \(n_{Al}=0,025\left(mol\right)\)
Theo (2) và (1) \(n_{H_2}=0,1\left(mol\right)\Rightarrow n_{Fe}=0,1\left(mol\right)\)
\(\Rightarrow\)\(\sum n_{Fe}=0,1\left(mol\right)\rightarrow m_{Fe_2O_3}=0,1\times160=16\left(g\right)\)
\(\sum n_{Al}=\left(0,2+0,05\right)\times27=6,75\left(g\right)\)
Vậy \(m=16+6,75=22,75\left(g\right)\)